0 引 言
城市污泥是污水处理过程的副产物。我国城市污泥总量大,含有病原菌、重金属和有机污染物等有害物质,同时也含有丰富的营养成分,兼具废物性与资源性,亟待妥善处置[1]。目前,我国污泥处置存在3个突出问题:1)处置率低下:“十二五”期间我国城镇污泥无害化处置率仅为56%。2)资源化欠缺:我国60%以上的污泥都采用土地填埋的处置方式,未实现物质与能量的再利用。3)污泥高含水率的制约:污泥脱水减容等预处理能耗较大,处置成本高。综上所述,针对改良污泥处置工艺的研究非常必要。
近年来水热碳化被逐渐应用于废弃生物质的处置[2-5]。该反应是将生物质与水混合并在一定温度和自发压力下进行水解、脱水、脱羧、聚合、缩合、芳香化等过程[6-8]。反应可杀灭病原体、固定重金属、分解有机污染物,同时可将废弃生物质制成水热炭,具备应用于燃烧、催化、吸附、电容、土壤改良等领域的潜力[9-14]。该技术的优势在于反应快速、条件温和、操作简便、规模可调节,可同时实现固废的无害化与资源化,并且无需进行脱水预处理。
但是目前针对城市污泥水热碳化处理的研究较少,对水热反应条件的影响及最优条件的选择未进行充分探讨。因此,本文以污泥稳定化与资源化为目标,选择需求大、前景好的重金属吸附剂为应用方向,探究水热条件对炭产物性质的影响,确定最优条件,并探究改性水热炭对铜和镉的吸附性能,为我国城市污泥处置及其资源化利用提供参考。
1 实验部分
1.1 原料与设备
供试污泥为北京清河再生水厂的脱水泥饼,污泥取回后于4 ℃冷藏保存。根据CJ/T 221—2005《城市污水处理厂污泥检验方法》,测得原始污泥含水率为86.35%,pH=6.68,有机质含量为39.98%。水热炭的制备采用FG-1L磁力驱动反应釜(大连三灵电力电子设备厂),容积为1 L。
1.2 水热炭的制备与改性
水热炭的制备:向反应釜中加入100 g污泥和100 mL超纯水,搅拌转速为300 r/min,设定反应温度为180,200,220,240 ℃,反应时间为1,3,10 h,反应结束后立即通入循环冷却水降至室温,取出后进行真空过滤使固液分离,固相产物于105 ℃烘干后研磨过100目筛(0.15 mm),得到水热炭粉末。
水热炭的改性[15]:将2 g水热炭粉末加入500 mL 2 mol/L的KOH溶液中,于室温下磁力搅拌反应1 h后真空过滤并用去离子水冲洗数次后将pH调至中性。固相产物105 ℃烘干后研磨过100目筛(0.15 mm),得到改性的水热炭粉末。
1.3 批次吸附实验
选取铜和镉作为重金属污染物,用CuSO4·5H2O(AR)和Cd(NO3)2·4H2O(AR)配制1000 mg/L的重金属储备液,根据吸附实验需要稀释至相应浓度。将一定浓度的铜、镉以及铜镉混合溶液40 mL移至装有一定量水热炭的50 mL离心管中,于25 ℃条件下200 r/min转速振荡一定时间后离心,取上清液0.45 μm滤膜过滤后用电感耦合等离子体发射光谱仪ICP-OES测定溶液中铜和镉的质量浓度。每组实验平行3次。
1)溶液pH值的影响:溶液浓度为50 mg/L,用0.1 mol/L的NaOH/HNO3调节初始溶液pH值分别为1、3、5、7、9,水热炭投加量为1 g/L,振荡反应 24 h。同时设置不添加水热炭的空白实验组。
2)水热炭投加量的影响:溶液浓度为50 mg/L,水热炭投加量分别为0.5,1,1.5,2 g/L,根据实验1)的结果调节溶液pH值为最优值,振荡反应24 h。
3)吸附动力学实验:向50 mg/L重金属溶液中投加1 g/L的水热炭并调至最优pH值,吸附时间梯度为5,10,20,30,45,60,80,100,120,150,180,240,300,600,900,1600 min。
4)吸附等温实验:分别向浓度为5,10,20,50,100,200,300,400,500 mg/L的重金属溶液中投加1 g/L的水热炭并调至最优pH值,振荡反应24 h。
1.4 吸附过程分析
1)吸附动力学模型拟合:分别采用Lagergren准一级动力学模型(式(1))和准二级动力学模型(式(2))的非线性公式进行拟合。
q=qe(1-e-k1t)
(1)
![]()
(2)
式中:qe为吸附平衡时的单位吸附量,mg/g;q为各时刻的单位吸附量,mg/g;k1为准一级动力学模型吸附速率常数,min-1;k2为准二级动力学模型吸附速率常数,g/(mg·min)。
2)吸附等温模型拟合:分别采用Langmuir吸附模型(式(3))和Freundlich吸附模型(式(4))的非线性公式进行曲线拟合。
(3)
![]()
(4)
式中:qe为平衡吸附量,mg/g;ce为溶液平衡浓度,mg/L;qm为单分子吸附时的饱和吸附量,mg/g;b为Langmuir亲和力常数,L/mg;k为Freundlich平衡吸附常数;n代表吸附剂表面的异质性。
1.5 表征与分析方法
利用元素分析仪vario EL测定样品中C、H、N元素含量。O元素含量采用差减法求得,根据《Standard Test Method for Ash in Biomass》(ASTM E1755)测定灰分;利用场发射扫描电镜(Merlin Compact,ZEISS)测定样品的表面形貌特征;利用傅里叶变换红外光谱(nicolet is50,ThermoFisher)对样品进行表征分析,扫描范围为400~4000 cm-1;利用比表面积分析仪(ASAP2020,Micrometer)测定样品的比表面积和孔容孔径;根据Tessier连续提取法[16],测定原污泥和水热炭中不同形态的As、Cu、Cd、Mn、Pb、Zn浓度。F1为可交换态,F2为碳酸盐结合态,F3为Fe-Mn氧化态,F4为有机结合态,F5为残渣态。
2 结果与分析
2.1 水热反应条件的影响
水热温度与反应时间是影响水热炭性质的主要因素。如图1所示:随着温度的升高,水热炭H/C与O/C逐渐下降,表明脱水、脱羧反应随着温度的升高变得更加剧烈,氧和氢的脱除更加充分、煤化程度更高,有利于后续资源化应用;相比之下,反应时间的影响则较小且无明显规律。
重金属五态的分析结果如图2、3所示。结果表明:原污泥中的重金属经水热碳化后从不稳定的F1、F2、F3态向相对稳定的F4、F5态转化,分析认为,可能是在水热过程中重金属与污泥固相晶核间的物质发生了络合,使重金属得以转化重构并实现稳定化;另外,溶液中的阴离子如![]() 和
和![]() 可与重金属结合成为沉淀物,被污泥基质捕获并进一步稳定化。对于绝大部分重金属而言,温度越高、时间越长,其生态毒性越低;而反应时间影响的规律没有温度显著。
可与重金属结合成为沉淀物,被污泥基质捕获并进一步稳定化。对于绝大部分重金属而言,温度越高、时间越长,其生态毒性越低;而反应时间影响的规律没有温度显著。
扫描电镜结果如图4所示。原污泥呈较规整、致密的团状结构,表面没有明显孔洞;经水热处理后,污泥结构出现不同程度的破坏,逐渐产生了孔洞和凹槽。随着温度的升高,200 ℃时产生细小孔洞,表面结构变得粗糙、杂乱。220 ℃时孔洞更加密集,部分孔洞开始出现轻度的塌陷,但整体结构仍较为规整。这些形貌有利于提升水热炭的吸附性能。240 ℃时,因温度过高水热炭表面结构被破坏,大部分孔洞壁塌陷,形成不规则凹槽。反应时间对水热炭表面结构的影响远小于温度。

![]() —H/C;
—H/C; ![]() —O/C。
—O/C。
图1 反应温度、时间对水热炭H/C、O/C的影响
Fig.1 Effect of reaction temperature and time on H/C and O/C of hydrothermal char
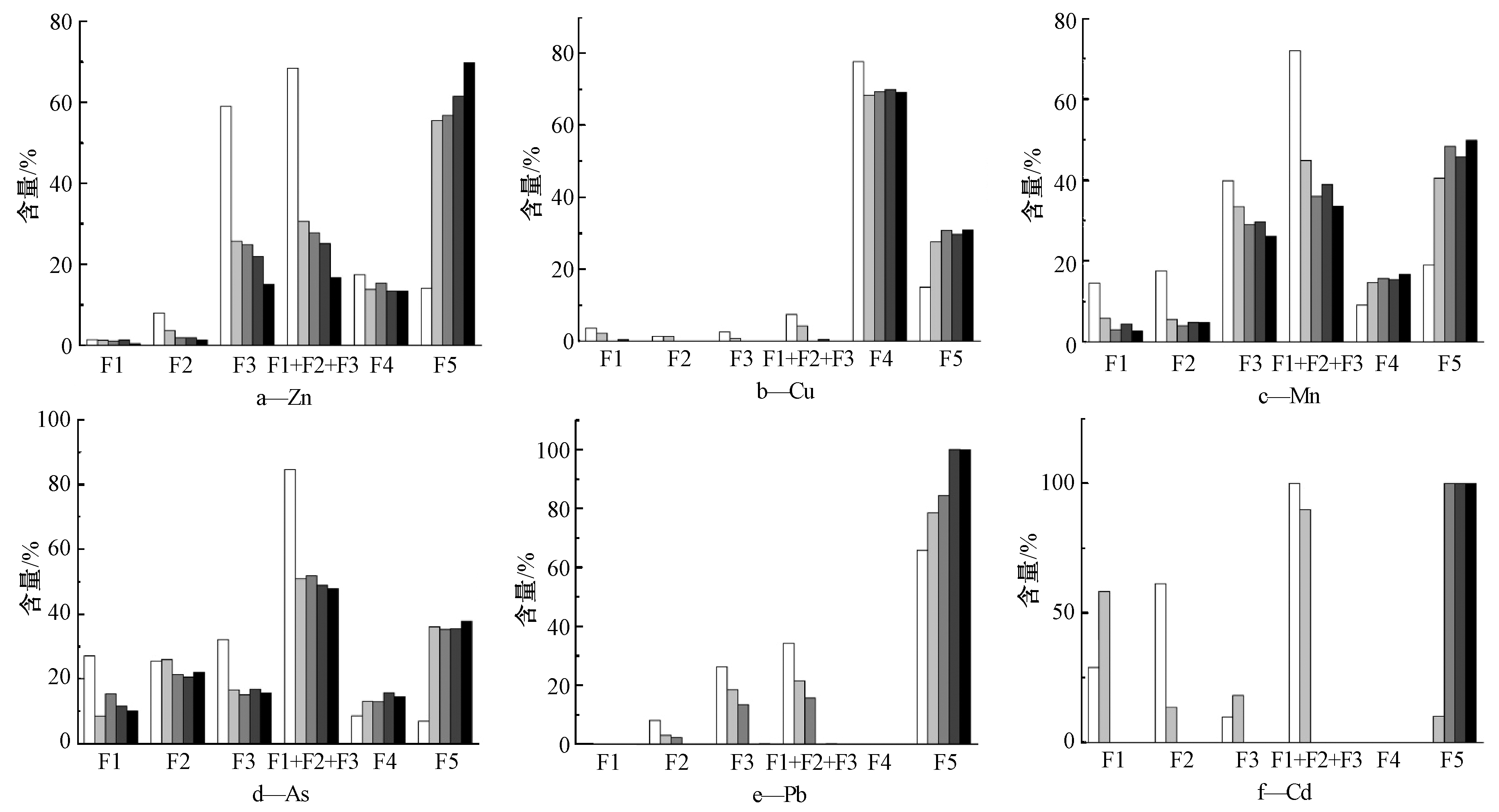
![]() 污泥;
污泥; ![]() 180 ℃;
180 ℃; ![]() 200 ℃;
200 ℃; ![]() 220 ℃;
220 ℃; ![]() 240 ℃。
240 ℃。
图2 反应温度对重金属形态的影响(反应时间3 h)
Fig.2 Effect of temperature on metal speciations of hydrothermal char (3 h)
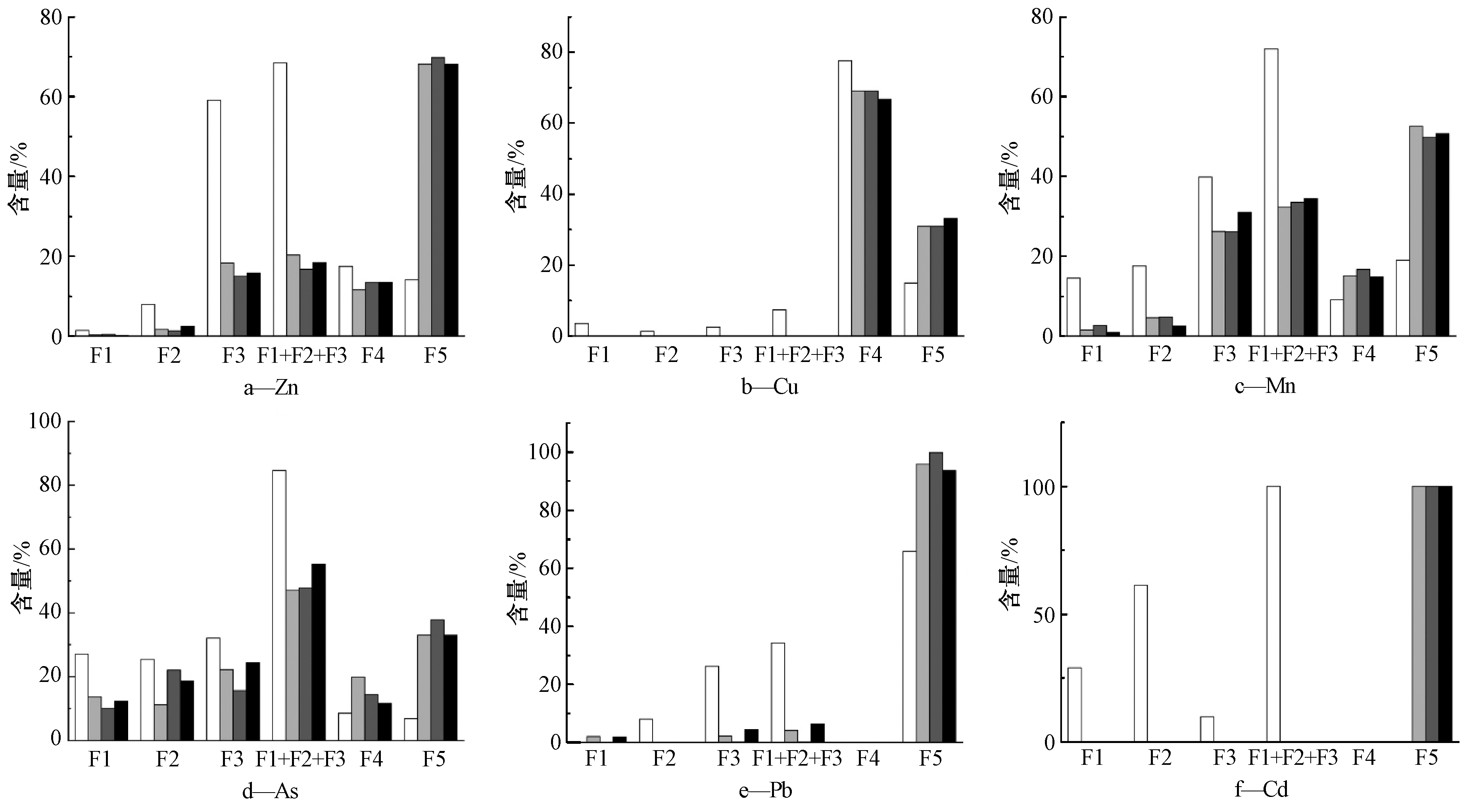
![]() 污泥;
污泥; ![]() 1 h;
1 h; ![]() 3 h;
3 h; ![]() 10 h。
10 h。
图3 反应时间对重金属形态的影响(反应温度为240 ℃)
Fig.3 Effect of reaction time on metal speciations of hydrothermal char (240 ℃)

图4 不同反应条件水热炭SEM照片
Fig.4 SEM images of hydrothermal char samples under different reaction conditions
污泥经水热碳化后,其比表面积、孔容与孔径均有显著提升(表1),展现出其在吸附、催化领域的应用潜力。比表面积和孔容随着温度的升高先上升后下降,在220 ℃达到峰值,说明在一定范围内升温可促使水热反应的充分进行,利于污泥中物质的溶出和表面孔洞的形成;若温度过高、反应过于剧烈,则会使水热炭的基本形态结构遭到较大程度的破坏,不利于形成稳定的多孔结构。因此,推断220 ℃是制备吸附用水热炭的相对最宜温度。而反应时间的影响则很小,1 h与10 h差异不大,与SEM分析结果相一致。
综上所述,权衡考量水热炭的吸附性能与制备经济性,推测220 ℃-1 h是制备水热炭吸附剂的相对最优条件。将不同条件制备的水热炭活化改性并进行重金属吸附预实验,220 ℃-1 h条件下的改性水热炭对Cu和Cd的吸附去除率高达98.98%和98.53%(溶液浓度为50 mg/L,吸附剂投加量为2.0 g/L),效果最好,印证了上述推断。
表1 水热炭的基本理化性质
Table 1 Basic physical properties of hydrothermal char

样品BET比表面积/(m2·g-1)孔体积/(cm3·g-1)平均孔径/nm原污泥3.60620.0172 19.1014180 ℃-1 h20.64940.1596 30.9118200 ℃-1 h24.38100.1868 30.6464220 ℃-1 h28.60530.2199 30.7453240 ℃-1 h22.52000.1826 32.4267200 ℃-10 h24.01020.178429.7265
2.2 改性水热炭的表征
水热炭改性前后SEM分析及物化性质分析如图5、表2所示。

图5 改性前后水热炭SEM照片
Fig.5 SEM images of hydrothermal char before and after modification
水热炭经KOH改性后,组成与性质发生较大变化。改性后其C、H、O、N含量上升,灰分含量下降,这是由于碱溶液可与水热炭中硅和铝等酸难溶物反应并将其从固相中浸提出来,从而降低灰分。研究表明,灰分的下降有助于煤质活性炭吸附性能的提升[17]。
表2 改性水热炭的基本物化性质
Table 2 Basic physical and chemical properties of modified hydrothermal char
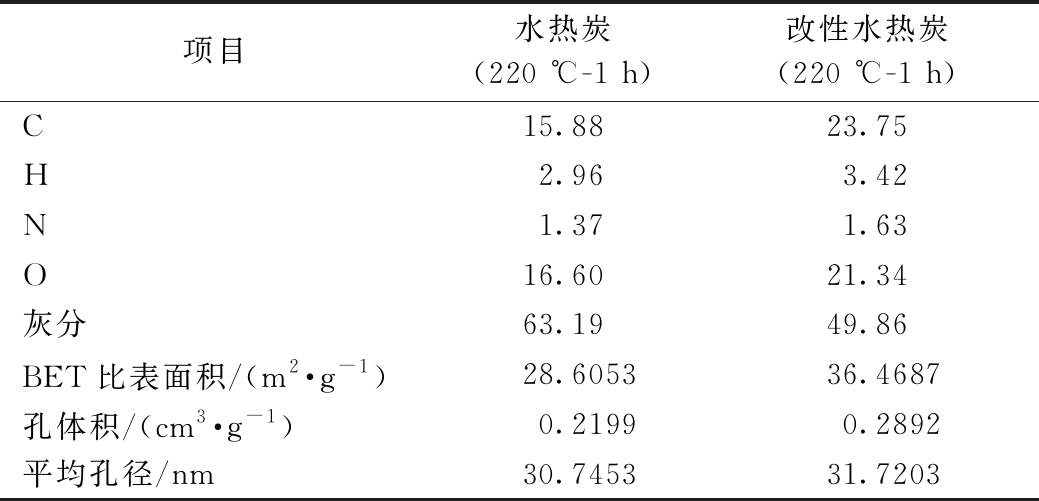
项目水热炭(220 ℃-1 h)改性水热炭(220 ℃-1 h)C15.8823.75H2.963.42N1.371.63O16.6021.34灰分63.1949.86BET比表面积/(m2·g-1)28.605336.4687孔体积/(cm3·g-1)0.21990.2892平均孔径/nm30.745331.7203
比表面积及孔分布结果显示:改性后水热炭的比表面积从28.6053 m2/g增至36.4687 m2/g,孔体积由0.2199 cm3/g增至0.2892 cm3/g。SEM分析结果表明:活化后水热炭表面刻蚀显著,结构变得凹凸不平,孔洞更加密集,产生了裂痕并出现团聚现象。这是由于碱可溶物被溶出,加大了孔洞和凹槽,同时KOH浓溶液具有扩孔效应,充分的浸渍腐蚀将产物表面部分微孔烧蚀成介孔,更有利于吸附。
水热炭的FT-IR图谱见图6。可知:3400 cm-1特征峰为—OH拉伸振动所致;2925,2850 cm-1为脂肪族C—H拉伸振动所致;1645 cm-1为酮或酰胺集团中C![]() O拉伸振动所致;1540 cm-1为羧基中不对称的C
O拉伸振动所致;1540 cm-1为羧基中不对称的C![]() O振动所致,活化后其强度显著提高,说明改性水热炭含有更多羧基,有利于重金属的化学吸附。1455 cm-1为芳香环中—C
O振动所致,活化后其强度显著提高,说明改性水热炭含有更多羧基,有利于重金属的化学吸附。1455 cm-1为芳香环中—C![]() C—拉伸,活化后强度提高,与KOH浸渍过程中的芳构化反应有关。1030 cm-1为酯、醚中的C—O拉伸所致;750,690 cm-1为苯环取代特征峰,由C—H面外弯曲振动所致,与活化过程中的芳构化有关。
C—拉伸,活化后强度提高,与KOH浸渍过程中的芳构化反应有关。1030 cm-1为酯、醚中的C—O拉伸所致;750,690 cm-1为苯环取代特征峰,由C—H面外弯曲振动所致,与活化过程中的芳构化有关。
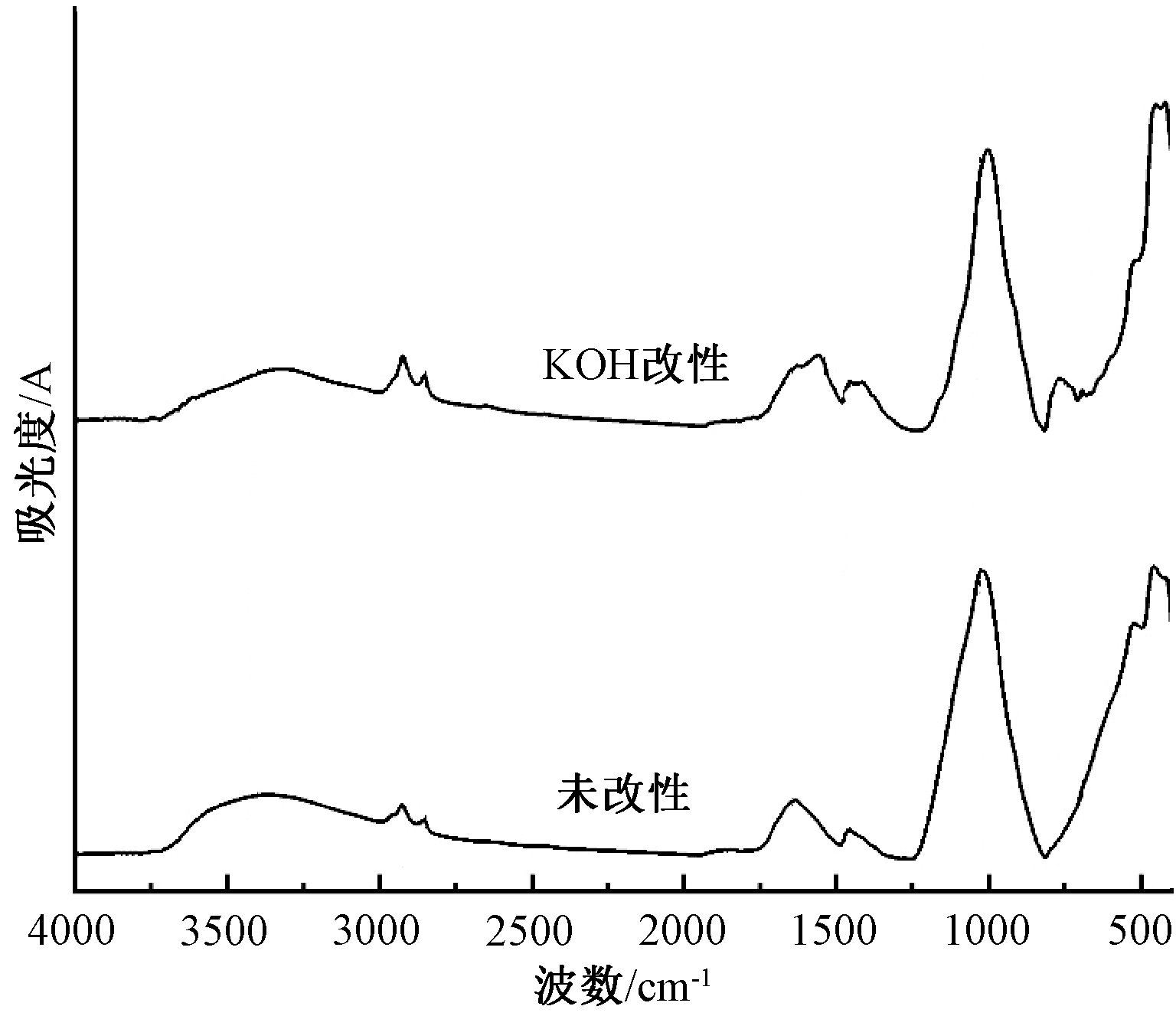
图6 改性前后水热炭FT-IR图谱
Fig.6 FI-IR spectrum of hydrothermal char before and after modification
综上所述,水热炭经过碱改性后,其比表面积、孔体积进一步增大,并且活化后产物的灰分更低、碳含量更高、含氧官能团更丰富,更有利于溶液重金属的吸附去除。
2.3 改性水热炭的吸附性能影响因素
2.3.1 溶液pH的影响
当Ca2+、Cd2+初始质量浓度为50 mg/L,改性水热炭投加量为1.0 g/L时,溶液pH对水热炭吸附重金属的影响如图7所示。未添加改性水热炭的空白实验组(图7a)表明:Cu在pH>5后开始沉淀,Cr在pH>7后开始沉淀;而当溶液pH≤5时,水热炭对Cu和Cd的吸附去除率随着pH的升高而增加。为了在最适条件下探究水热炭的吸附性能,同时排除重金属沉淀的干扰,控制溶液初始pH=5。
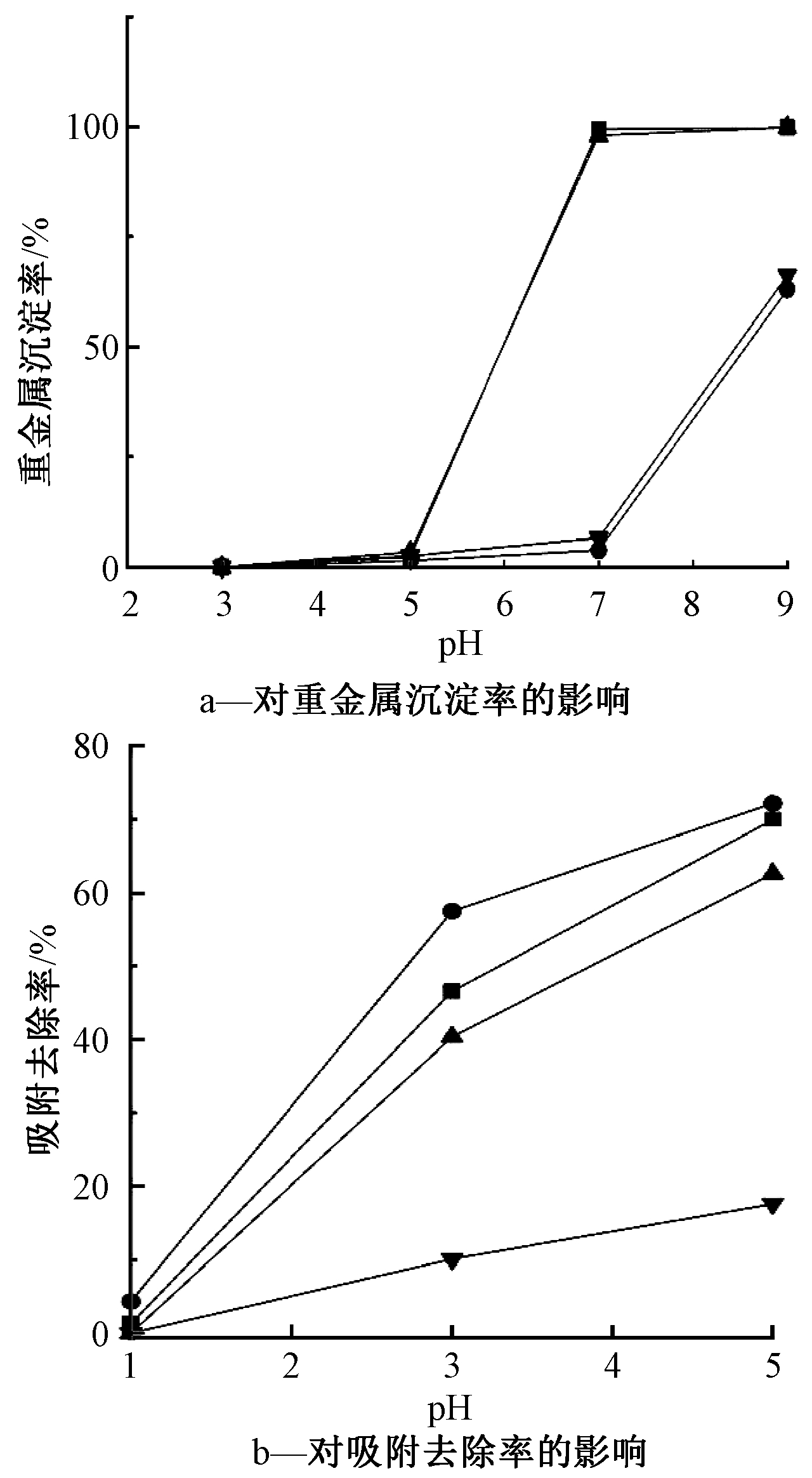
![]() —Cu;
—Cu; ![]() —Cd;
—Cd; ![]() —混合Cu;
—混合Cu; ![]() —混合Cd。
—混合Cd。
图7 溶液pH对水热炭吸附重金属的影响
Fig.7 Effect of pH on absorption of hydrothermal char for heavy metals
2.3.2 吸附剂投加量的影响
吸附剂投加量的影响如图8所示。可知:随着投加量的增加,重金属去除率逐渐提高,吸附剂吸附容量逐渐下降。为使重金属的去除率与吸附剂的吸附容量均维持在相对较高水平,最佳投加量约为1.0 g/L,此时Cu去除率为76.81%,吸附容量为38.17 mg/g;Cd去除率为89.57%,吸附容量为41.29 mg/g。
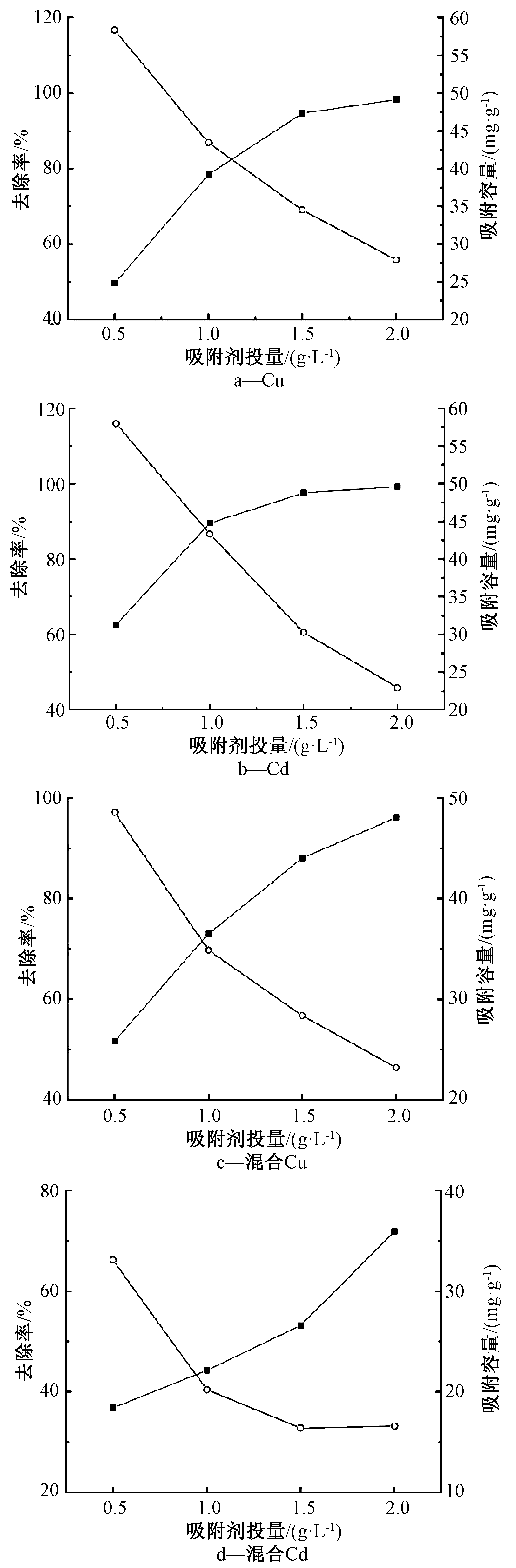
![]() —去除率;
—去除率; ![]() —吸附容量。
—吸附容量。
图8 水热炭投加量对重金属吸附的影响
Fig.8 Effect of absorbent dose on absorption for heavy metals
2.3.3 吸附动力学实验
吸附动力学实验结果如图9和表3所示。由图9可知:改性水热炭对Cu、Cd的吸附在前2 h速率较快,其后单位吸附量的增长随着时间的推移趋于平缓。改性水热炭对Cu和Cd的吸附更符合Lagergren伪二级动力学方程,说明吸附过程以化学吸附为主,与污泥水热炭表面以羧基为代表的各种含氧官能团有关。拟合结果显示:水热炭对Cu和Cd的平衡吸附量为47.48,51.05 mg/g,对混合溶液中Cu和Cd的平衡吸附量达到36.00,17.79 mg/g。
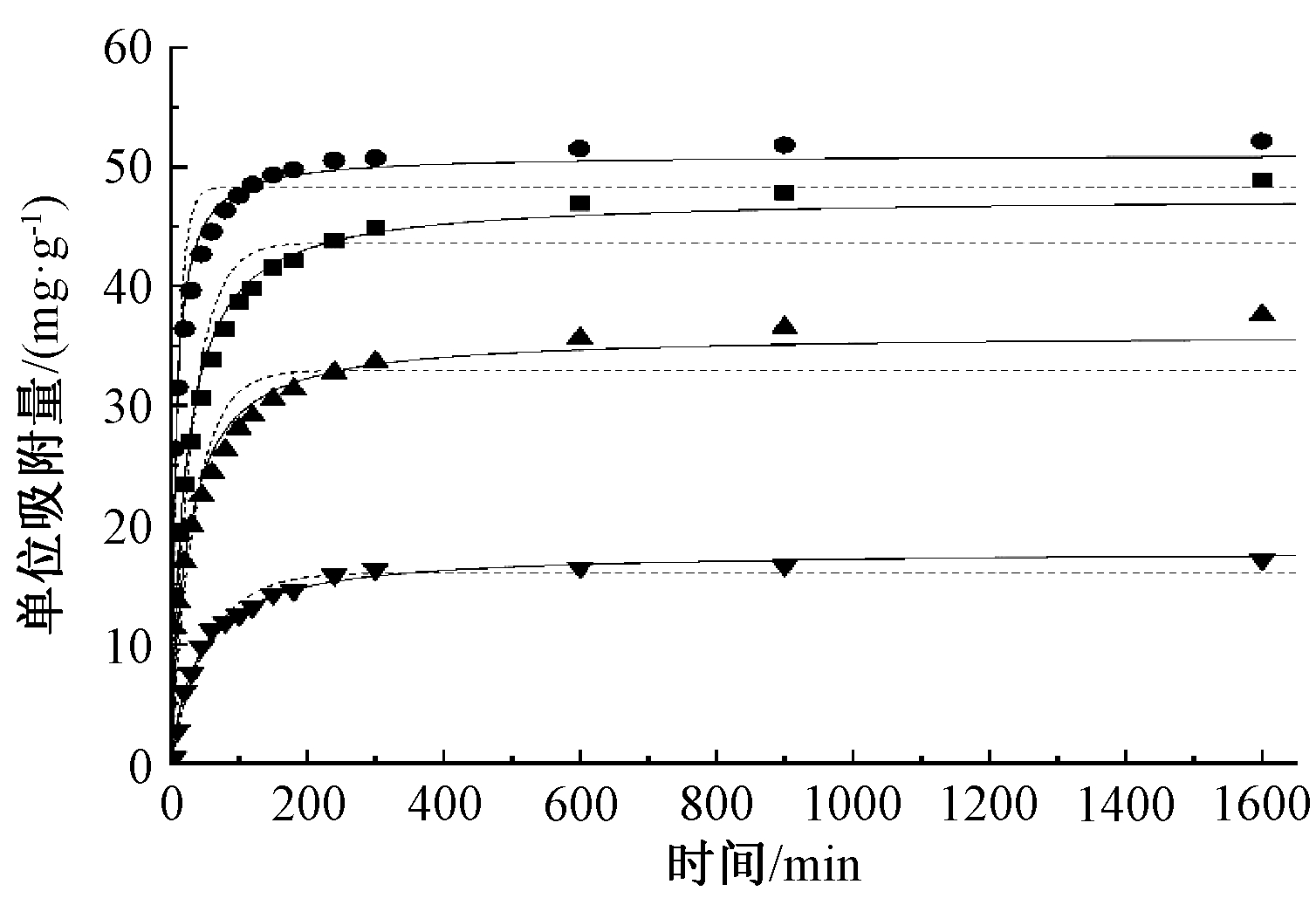
![]() Cu;
Cu;![]() Cd;
Cd;![]() 混合Cu;
混合Cu;![]() 混合Cd。
混合Cd。
------伪一级动力学模型拟合; ——伪二级动力学模型拟合。
图9 水热炭吸附Cu、Cd动力学曲线拟合
Fig.9 Kinetic fitting result of Cu, Cd adsorption by hydrothermal char
表3 水热炭吸附Cu,Cd动力学拟合参数
Table 3 Kinetic fitting parameters of Cu, Cd adsorption by hydrothermal char
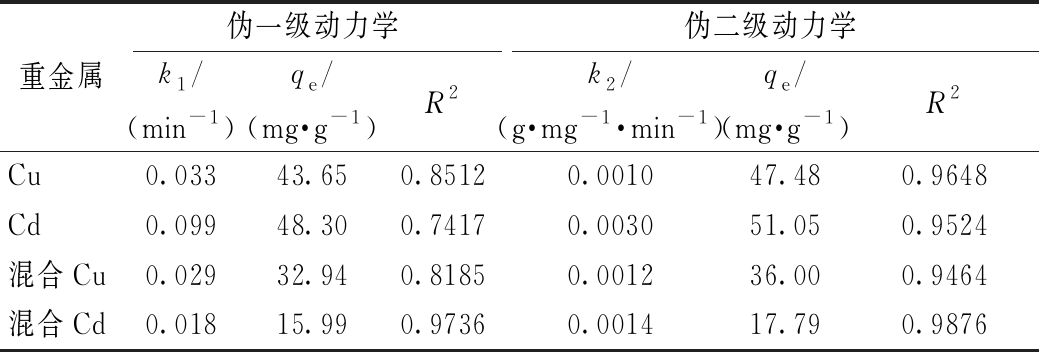
重金属伪一级动力学伪二级动力学k1/(min-1)qe/(mg·g-1)R2k2/(g·mg-1·min-1)qe/(mg·g-1)R2Cu0.03343.650.85120.001047.480.9648Cd0.09948.300.74170.003051.050.9524混合Cu0.02932.940.81850.001236.000.9464混合Cd0.01815.990.97360.001417.790.9876
2.3.4 吸附等温实验
吸附等温实验结果如图10和表4所示。可知:两种模型均可较好地拟合水热炭对Cu和Cd的吸附(拟合相关系数Cu为0.96,Cd为0.98),说明除了表面单分子层吸附以外,也存在一定的不均匀表面的非均相吸附。而混合溶液中对镉的吸附,2种模型拟合度均较差,可能是吸附剂投加量偏大,在低浓度溶液中吸附完全,导致低浓度区域缺少有效数据,也可能是Cu的吸附对Cd的影响较大,使低浓度区域Cd的吸附量不稳定,数据波动大、可重复性差,不具代表性,因而拟合准确度不高。
根据Langmuir模型拟合结果,水热炭对Cu的饱和吸附容量为49.89 mg/g,Cd为52.04 mg/g,混合溶液中二者之和为51.08 mg/g(Cu:38.22 mg/g,Cd:12.86 mg/g),三者大致相同,且混合溶液中Cu的吸
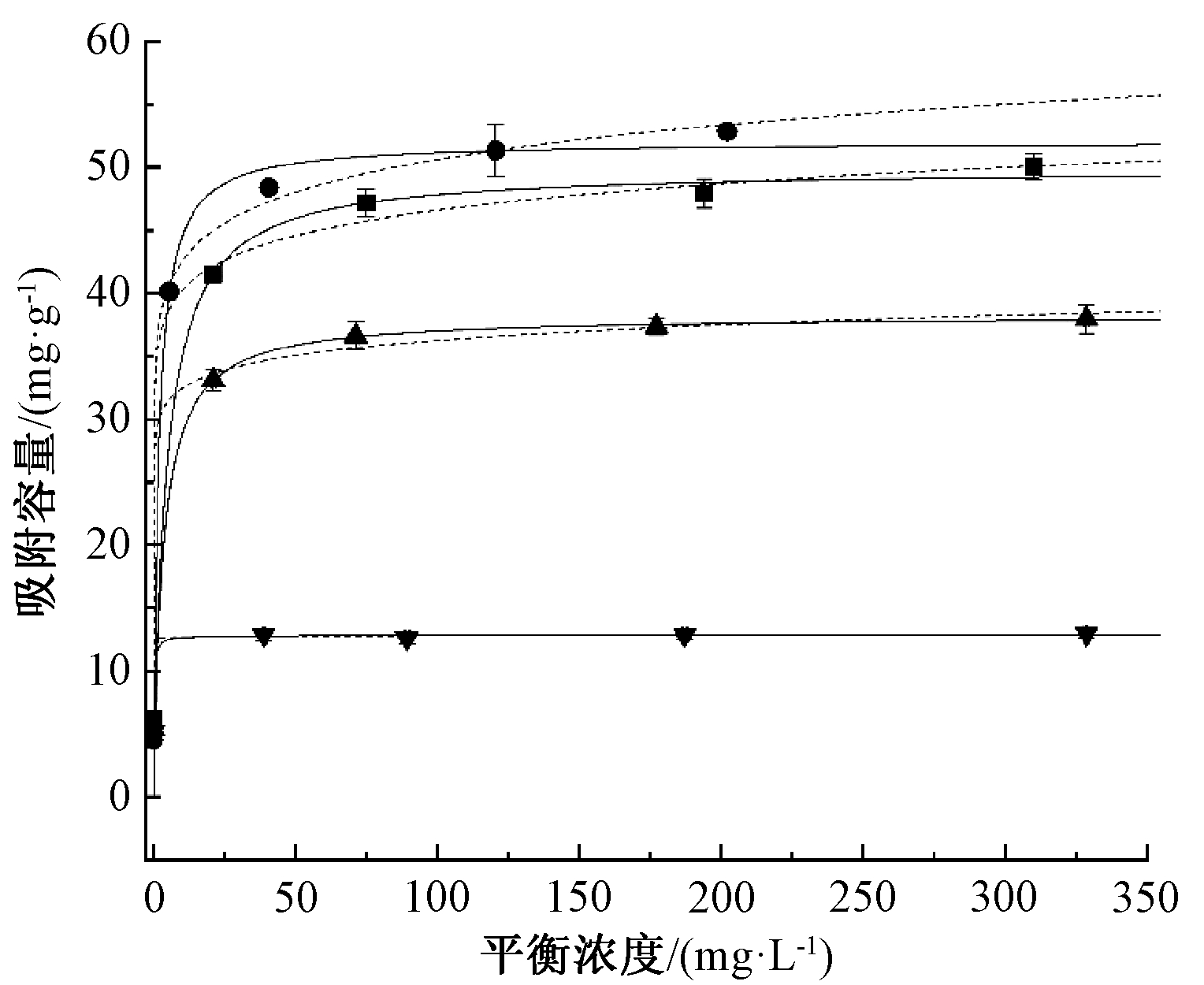
![]() Cu;
Cu;![]() Cd;
Cd;![]() 混合Cu;
混合Cu;![]() 混合Cd。
混合Cd。
——Fangmuir model; ------Freundlich model。
图10 水热炭吸附Cu、Cd的吸附等温线
Fig.10 Adsorption isotherm of Cu, Cd adsorption by hydrothermal char
表4 水热炭吸附Cu、Cd等温线拟合参数
Table 4 Isotherm fitting parameters of Cu,Cd adsorption by hydrothermal char
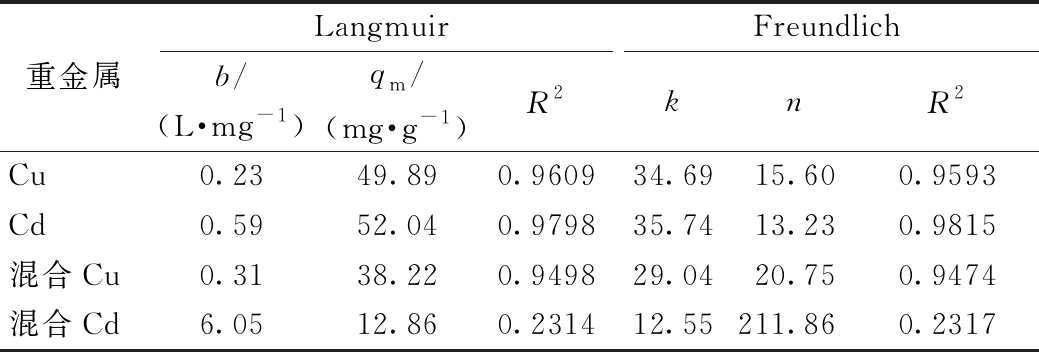
重金属LangmuirFreundlichb/(L·mg-1)qm/(mg·g-1)R2knR2Cu0.2349.890.960934.6915.600.9593Cd0.5952.040.979835.7413.230.9815混合Cu0.3138.220.949829.0420.750.9474混合Cd6.0512.860.231412.55211.860.2317
附容量明显大于Cd。由于水热炭以化学吸附为主,吸附位点的总量相对恒定,在单溶质溶液中全部与一种金属结合,故体现不出差异;而在混合溶液中,表面官能团与金属的结合存在选择性,使得混合溶液中Cu和Cd的吸附容量下降,但总吸附容量不变。由于Cu2+的水合半径(0.419 nm)小于Cd2+的水合半径(0.426 nm)[18],且Cu2+比Cd2+具有更高的电负性(Cu:1.90;Cd:1.69),可与水热炭表面官能团中氧、氮等原子的孤对电子形成更加稳定的复合物,因此水热炭表面位点更倾向于与Cu结合,表现为其对Cu的吸附效果优于Cd。
3 结 论
1)反应温度是影响污泥水热炭性质的最主要因素。随着温度的提高,水热炭煤化更充分、重金属稳定化程度更高、比表面积与孔容更大。220 ℃-1 h是制备吸附用途水热炭的最优条件,可在污泥稳定化、无害化的基础上实现资源化。
2)水热炭经过KOH浸渍改性后,比表面积增大、灰分降低、含氧官能团增多,对溶液重金属吸附性能良好。当溶液pH=5,改性水热炭最佳投加量约为1.0 g/L时,Cu2+、Cd2+初始质量浓度为50 mg/L的重金属溶液,Cu2+去除率为76.81%,吸附容量为38.17 mg/g;Cd2+去除率为89.57%,吸附容量为41.29 mg/g。
3)动力学研究表明,改性水热炭对铜和镉的吸附符合Lagergren伪二级动力学模型,吸附过程以化学吸附为主,这与污泥水热炭表面以羧基为代表的各种含氧官能团有关。
4)改性水热炭对溶液重金属的吸附等温线可用Langmuir、Freundlich吸附等温模型较好地拟合。铜和镉的饱和吸附容量分别为49.89,52.04 mg/g。而在混合溶液中改性水热炭优先吸附水合离子半径更小电负性更高的Cu。
[1] Huang R X, Tang Y Z. Speciation Dynamics of phosphorus during (Hydro) thermal treatments of sewage sludge[J]. Environmental Science & Technology, 2015, 49(24):14466-14474.
[2] Basso D, Patuzzi F, Castello D, et al. Agro-industrial waste to solid biofuel through hydrothermal carbonization[J]. Waste Management, 2016, 47:114-121.
[3] Minaret J, Dutta A. Comparison of liquid and vapor hydrothermal carbonization of corn husk for the use as a solid fuel [J]. Bioresource Technology, 2016, 200:804-811.
[4] Sabio E,  lvarez-Murillo A, Román, S, et al. Conversion of tomato-peel waste into solid fuel by hydrothermal carbonization: influence of the processing variables [J]. Waste Management, 2016, 47:122-132.
lvarez-Murillo A, Román, S, et al. Conversion of tomato-peel waste into solid fuel by hydrothermal carbonization: influence of the processing variables [J]. Waste Management, 2016, 47:122-132.
[5] Zhang H, Zhang F Y, Huang Q. Highly effective removal of malachite green from aqueous solution by hydrochar derived from phycocyanin-extracted algal bloom residues through hydrothermal carbonization[J]. Rsc Advances, 2017, 7:5790-5799.
[6] Sevilla M, Fuertes A B. The production of carbon materials by hydrothermal carbonization of cellulose [J]. Carbon, 2009, 47(9):2281-2289.
[7] Falco C, Baccile N, Titirici M M. Morphological and structural differences between glucose, cellulose and lignocellulosic biomass derived hydrothermal carbons [J]. Green Chemistry, 2011, 13(11):3273-3281.
[8] He C, Giannis A, Wang J. Conversion of sewage sludge to clean solid fuel using hydrothermal carbonization: hydrochar fuel characteristics and combustion behavior [J]. Applied Energy, 2013, 111:257-266.
[9] Zhou N, Chen H G, Xi J T, et al. Biochars with excellent Pb(Ⅱ) adsorption property produced from fresh and dehydrated banana peels via hydrothermal carbonization [J]. Bioresource Technology, 2017, 232:204-210.
[10] Kim D, Lee K, Park K Y. Hydrothermal carbonization of anaerobically digested sludge for solid fuel production and energy recovery [J]. Fuel, 2014, 130(15):120-125.
[11] Rehrah D, Bansode R R, Hassan O, et al. Physico-chemical characterization of biochars from solid municipal waste for use in soil amendment [J]. Journal of Analytical & Applied Pyrolysis, 2016, 118:42-53.
[12] Hu Z, Shen Z, Yu J C. Converting carbohydrates to carbon-based photocatalysts for environmental treatment [J]. Environmental Science & Technology, 2017, 51(12):7076-7083.
[13] Wang Y, Jiang L. Roles of graphene oxide in hydrothermal carbonization and microwave irradiation of distiller’s dried grains with solubles to produce supercapacitor electrodes [J]. Acs Sustainable Chemistry & Engineering, 2017, 5(6): 5588-5597.
[14] Zhu G T, Xing X J, Wang J Q, et al. Effect of acid and hydrothermal treatments on the dye adsorption properties of biomass-derived activated carbon [J]. Journal of Materials Science, 2017, 52(13):1-13.
[15] Regmi P, Moscoso J L G, Kumar S, et al. Removal of copper and cadmium from aqueous solution using switchgrass biochar produced via hydrothermal carbonization process[J]. Journal of Environmental Management, 2012, 109(17):61-69.
[16] Tessier A, Campbell P G C, Bisson M. Sequential extraction procedure for the speciation of particulate trace metals[J]. Analytical Chemistry, 1979, 51(7):844-851.
[17] 韩露,李开喜,高峰.工艺参数及灰分对煤基活性炭吸附性能的影响[J].煤炭转化,2008,31(3):71-76.
[18] Nightingale Jr E R. Phenomenological theory of ion solvation. Effective radii of hydrated ions[J]. Biochimica Et Biophysica Acta, 1959, 63(9):566-567.