0 引 言
随着现代工业化和城市化的快速发展,环境污染问题越来越严峻,特别是有机无机复合污染问题日益恶化[1-2]。在环境污染修复领域,TiO2被用于特定的光催化材料受到高度关注,然而TiO2材料带隙宽度较小,导致其可见光响应很差,同时光致电子及空穴复合较快,一定程度上制约了TiO2材料用于光催化领域[3-4]。除此之外,TiO2材料颗粒尺度小,应用于水污染修复后难进行固液分离,限制了其在实际水处理过程中的应用[5]。故制备高吸附、光催化能力和磁性分离性能的新型复合材料,一直是环境修复的热门领域。所以将吸附效果优良兼具光催化性能的TiO2材料作为壳层,内填充磁性Fe3O4,可实现修复性能和回收利用两者的有机复合。
据文献[6-7]报道,光催化与吸附活性取决于核壳结构材料的外壳厚度。Xin等[7]研究了15~120 nm范围内,TiO2外壳厚度对复合材料光催化活性的影响,结果显示,壳层厚度增大催化活性迅速下降。相反,Jing等[6]发现,随着n(TiO2)∶n(Fe3O4)增加,复合材料的光催化降解能力由73.45%增加到89.88%。基于相关研究,TiO2外壳厚度会影响复合材料的催化及分离效果,然而,TiO2外壳厚度对核壳材料催化效果影响的研究并不透彻, 且作用机理尚不清晰,这在一定条件下制约了TiO2复合材料在环境领域的进一步探索与应用。
本研究拟利用溶剂热法合成具有不同TiO2外壳厚度的Fe3O4@TiO2复合纳米材料,并将其用于砷及染料去除。旨在寻求一种结合了除砷和光催化降解染料的新型多功能材料,在环境污染修复领域具有较广阔的应用前景。
1 实验部分
1.1 材 料
试剂:钛酸四丁酯(TBOT,≥97%);氯化铁(FeCl3·6H2O,A.R.);醋酸铵(NH4Ac,A.R.);柠檬酸钠(Na3C6H5O7,A.R.);甲基橙(Methyl orange,A.R.);亚砷酸钠(NaAsO2,A.R.)。
仪器:YP2002 N型电子天平、干燥箱、DZS-706多参数分析仪、拉曼分析仪、H-800型电子显微镜。
1.2 方 法
1.2.1 Fe3O4@TiO2复合材料的制备
称取1.350 g FeCl3·6H2O、0.456 g Na3C6H5O7、3.854 g NH4Ac置于250 mL锥形瓶中,在磁力搅拌条件下,加入乙烯乙二醇70 mL,搅拌成黑色溶液,将其转移至高压反应釜后,于200 ℃的恒温烘箱中反应16 h,用乙醇清洗产物5次,真空烘干后即为合成的磁性Fe3O4材料。称取上述合成的Fe3O4溶于20 mL乙醇中,再加入75 mL乙醇与5 mL超纯水,超声20 min后倒入三口瓶中。在Fe3O4-APTMS 3-氨丙基三乙氧基硅烷溶液中逐滴加入不同量的TBOT钛酸四丁酯,使得n(TiO2)∶n(Fe3O4)=0.1,0.5,1.0分别记作FT-0.1、FT-0.5、FT-1.0。搅拌0.5 h后,再向溶液中加入15 mg CTAB十六烷基三甲基溴化铵,继续搅拌0.5 h,产物用乙醇清洗5次,烘干后在450 ℃煅烧2 h,得到Fe3O4@TiO2。
1.2.2 Fe3O4@TiO2复合材料表征
颗粒分散性分析:采用JS94H型微电泳仪测量,将反应池置于U型玻璃样品池中,将材料制成悬浮液,控制测定温度,自动测定并返回计算机。SEM分析:样品经由导电胶带粘到铜制样品台后,采用H-800型电子显微镜观测。HRTEM分析:样品滴加至超薄碳膜上后利用F20型透射电子显微镜观测。Raman分析:在激发光波长为532 nm的环境下,用HORIBA拉曼分析仪测量。
1.2.3 吸附等温线实验
称取Fe3O4@TiO2材料样品0.100 g于50 mL离心管中,分别添加40 mL浓度梯度为0,5,20,60,100,160,200 mg/L的As3+溶液,在25 ℃恒温干燥箱中维持24 h后,取上清液,在4000 r/min下离心15 min,用原子吸收分光光度计测量反应后溶液中的As浓度,计算吸附量后,用吸附量与吸附平衡浓度绘制吸附等温线。
1.2.4 光催化实验
称取0.100 g的 Fe3O4@TiO2材料置于表面皿中,加入2×10-5 mol/L甲基橙溶液20 mL,调节pH=7,在避光条件下吸附30 min至吸附饱和。在可见光源照射下,定时取样,通过分光光度计法测量甲基橙的浓度,计算降解量。
2 结果与讨论
2.1 Fe3O4@TiO2复合材料形貌表征
采用SEM表征外壳厚度不同的Fe3O4@TiO2复合纳米材料的形貌结构。经SEM观测(图1)发现,Fe3O4颗粒显现为均匀的球状,颗粒平均直径为(500±20) nm;当在Fe3O4悬液中加入TiO2前驱体TBOT后,纳米材料仍然是球形结构,且颗粒平均直径增加至550±17 nm(图1b)。随着TiO2/Fe3O4摩尔比由0.5增至1.0,Fe3O4@TiO2的颗粒平均直径分别为(564±30) nm(图1c), (968±15) nm(图1d)。当n(TiO2)∶n(Fe3O4)<1,通过DLS表征的颗粒大小与SEM测量的颗粒直径相近;当n(TiO2)∶n(Fe3O4)=1,通过DLS表征的颗粒远大于SEM测量的颗粒直径。当TiO2/Fe3O4摩尔比增大时,颗粒会发生团聚现象。根据已有研究报道[8],核壳结构的形成可分为3个阶段:当TiO2较少时,TiO2形成的外壳较薄且不均匀;当TiO2增加时,可形成均匀的TiO2外壳;当TiO2过多时,Fe3O4表面既会发生均相成核又会发生非均相成核,导致颗粒发生团聚现象。
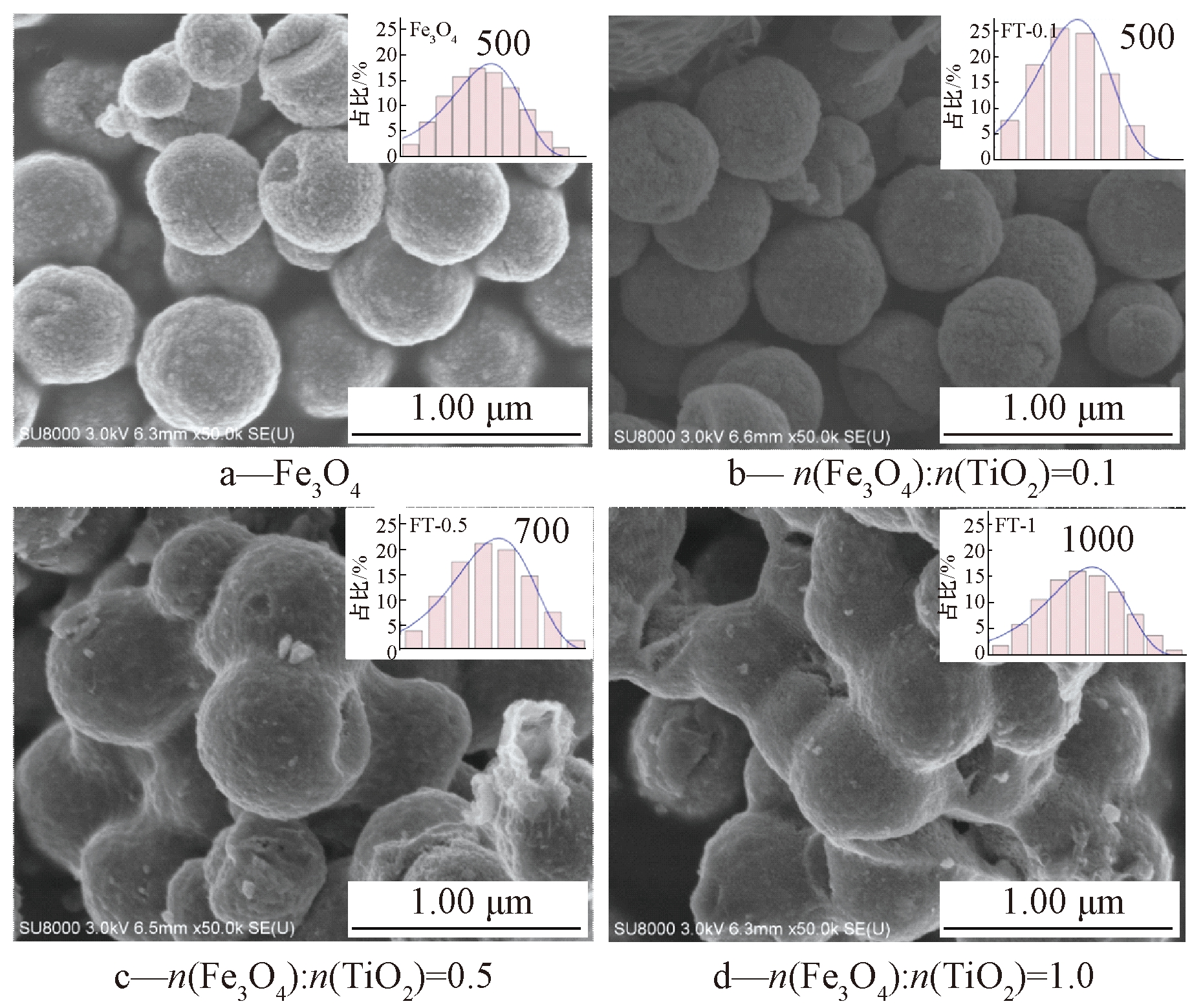
图1 Fe3O4@TiO2复合材料的SEM和DLS表征图
Fig.1 SEM and DLS images of Fe3O4@TiO2 composite
2.2 Fe3O4@TiO2复合材料结构表征
经TEM 观察(图2a),Fe3O4@TiO2复合材料显示出典型的核壳结构,内部深色为Fe3O4内核,外部较浅色部分为TiO2内核。使用HRTEM观察外部较浅色区域,外壳材料的晶格间距为0.35 nm,说明TiO2外壳由以(101)晶面为主的TiO2构成[9]。结合EDS能谱分析,复合材料构成元素中既有Fe元素也有Ti元素,且Ti占比为6.6%,可定量表征复合材料中TiO2的存在。通过EDX面扫分析探究FTG复合材料的晶体结构及表面特征(图2c—d),EDX面扫可直观地表征Fe3O4@TiO2复合材料结构,Fe元素主要集中在内核,而Ti元素主要集中在外壳,Fe3O4@TiO2复合材料是Fe3O4内核和TiO2外壳构成的核壳结构。与多数核壳材料的复杂制备过程相比,本文报道的Fe3O4@TiO2复合材料未使用SiO2作为中间架桥[10],合成方法简单且组成成分明确。
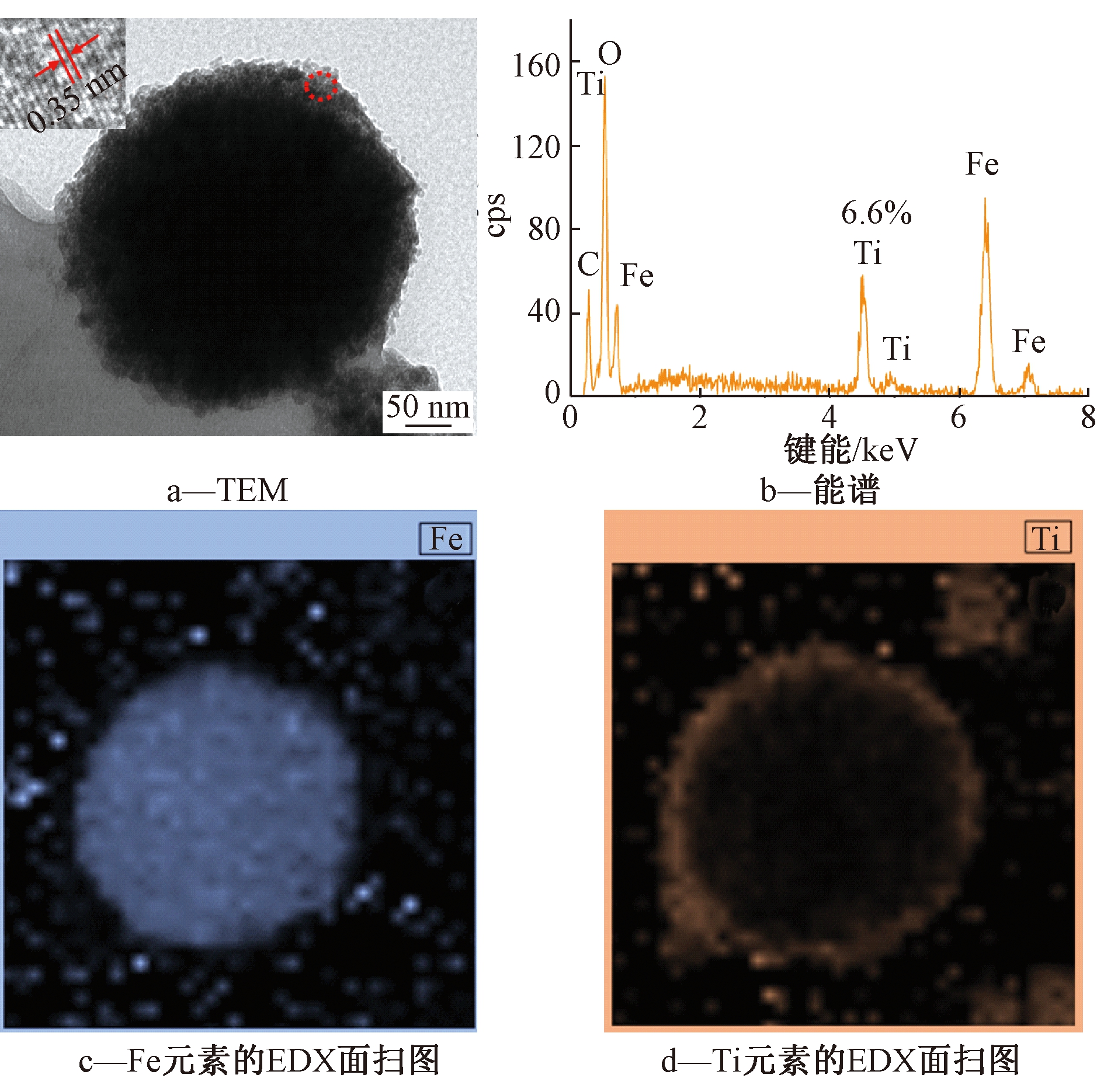
图2 Fe3O4@TiO2复合材料的TEM表征
Fig.2 TEM images of Fe3O4@TiO2, EDS spectra, the corresponding EDX mapping images of iron and titanium elements
2.3 Fe3O4@TiO2复合材料性质表征
采用XRD、Raman、XPS进一步表征Fe3O4@TiO2复合材料的2种组成成分Fe3O4和TiO2之间的结合作用(图3)。通过XRD表征,Fe3O4@TiO2光谱在不同位置处出现6个特征峰,依次对应锐钛矿TiO2的 (101)、(004)、(200)、(105)、(211) 和 (204)晶面 (JCPDS 21-1272),结合HRTEM表征结果,TiO2外壳由以(101)晶面为主的锐钛矿TiO2构成。除此之外,Fe3O4@TiO2光谱中仍然存在其他5个特征峰,依次对应的是Fe3O4晶体的 (220)、(311)、(400)、(511) 和 (440) 5个晶面(JCPDS 65-3107)。XRD实验结构证明:Fe3O4@TiO2复合材料是由Fe3O4和TiO2 2种组成成分构成的,在高温水热环境下,Fe3O4基本未被氧化,原因归结为一定厚度的TiO2外壳保护了Fe3O4内核。
Raman光谱分析结果(图3b)表明:Fe3O4纳米颗粒未出现尖细的特征峰,而TiO2材料则在145,395,521,638 cm-1处出现了4个特征峰。Fe3O4@TiO2复合材料的Raman谱中,形成了4个尖细的特征峰,然而,较之于初始的TiO2材料,4个峰的相对位置发生偏移,Fe3O4@TiO2复合材料中Fe3O4和TiO2的有机结合影响了TiO2特征峰的伸缩振动。
Fe3O4@TiO2复合材料的化学键合成情况用XPS光谱分析研究(图3c)。分峰分析Fe3O4@TiO2复合材料XPS谱图中Ti2p,结果表明:该复合材料中存在Ti3+。一方面,Ti3+的出现证明Fe3O4和TiO2 2种组成成分之间的化学结合,其形成过程中存在电子转移,使Ti在合成过程中发生还原。另一方面,Ti3+的存在利于该复合材料捕捉光生电子,能促进空穴与电子的分离[11]。
Fe3O4@TiO2复合材料的光学性质用UV-DRS进行分析(图3d)。TiO2纳米材料的带隙宽度为3.2 eV,较宽的带隙降低了TiO2的吸光范围,导致对可见光的响应不佳。Fe3O4纳米材料的带隙宽度为1.8 eV,说明Fe3O4自身也是一种良好的半导体材料,但是光生电子和空穴易复合的缺陷,致使光催化效率不高。Fe3O4@TiO2复合材料的带隙宽度为1.7 eV,带隙宽度的减小不仅提升了对可见光的响应,而且TiO2在受到光激发后产生光致电子与空穴的分离,电子进一步传递给内核的Fe3O4,有利于遏制光致电子与空穴的复合。
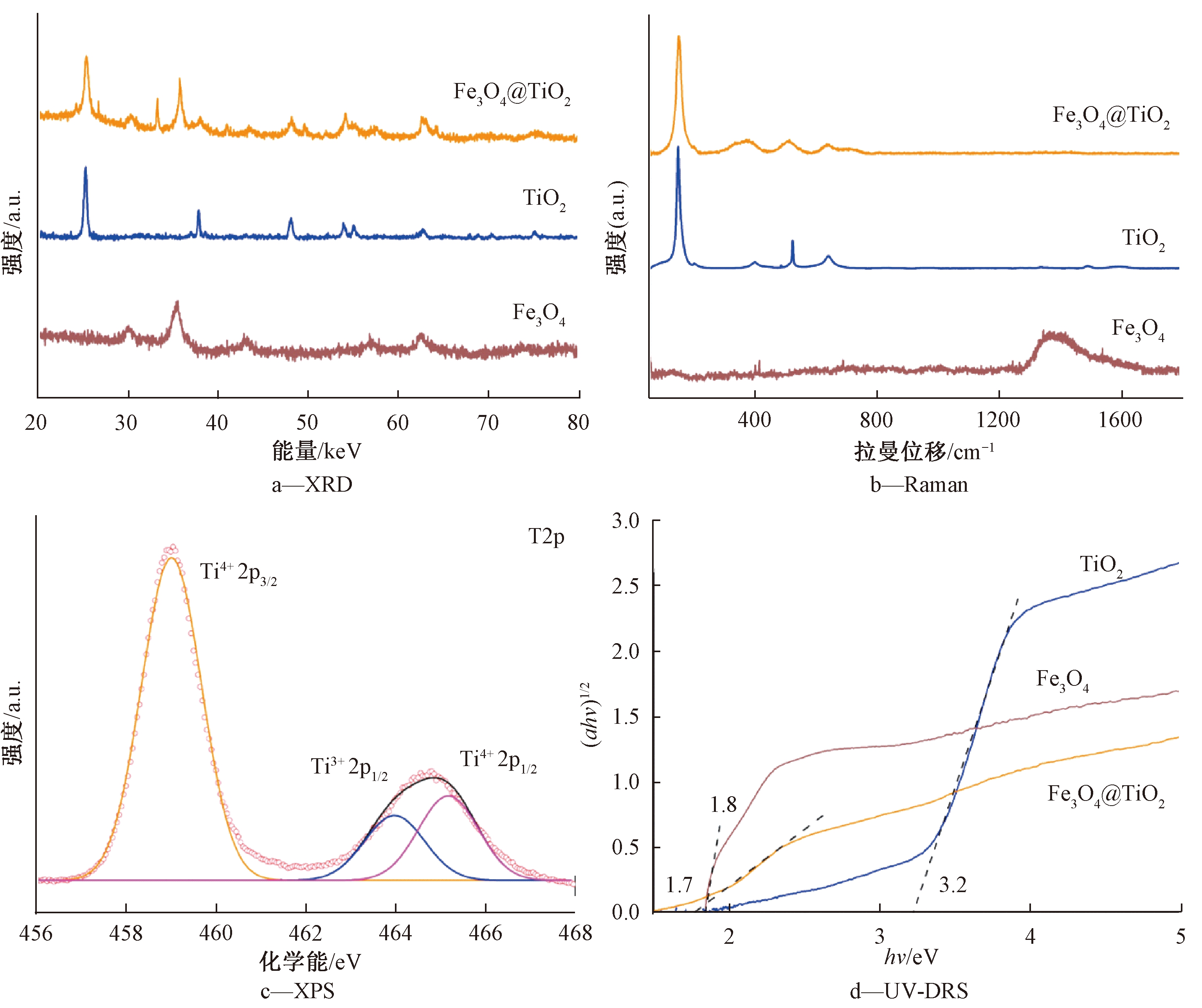
图3 XRD、Raman、XPS、UV-DRS表征Fe3O4@TiO2材料
Fig.3 XRD, Raman,XPS,and UV-DRS spectra of Fe3O4@TiO2 composite
2.4 Fe3O4@TiO2复合材料对As及甲基橙的去除
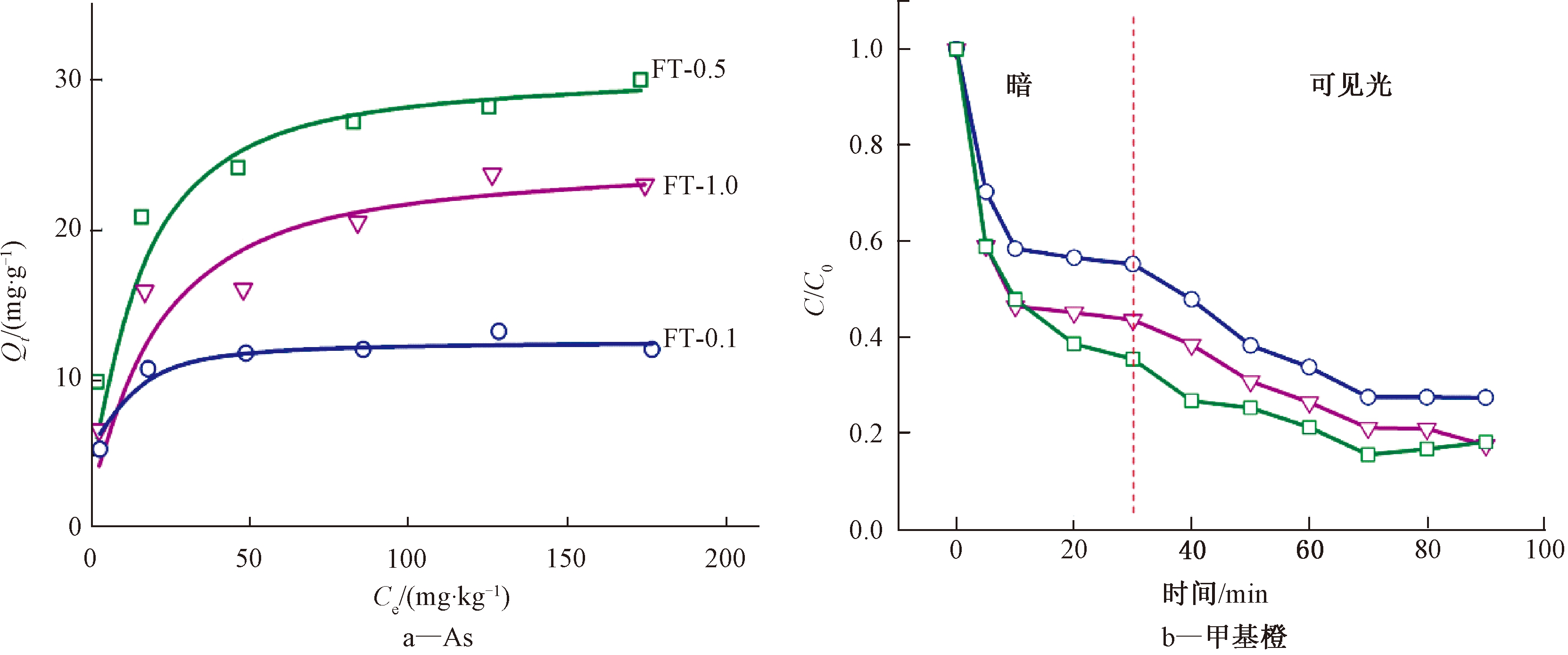
考虑到污染水体中阴离子型重金属的去除较难实现,将Fe3O4@TiO2复合材料用于As3+的吸附,探索该材料吸附去除阴离子型重金属的应用潜力。首先,依据实际水体的基本参数,将吸附条件控制在:温度为25 ℃,pH值为8。Fe3O4@TiO2复合材料对As3+的吸附等温线如图4a所示。在As3+的初始浓度较低时,随着初始As浓度的上升,Fe3O4@TiO2复合材料对As吸附量逐渐提升,且吸附速度不断上升;之后,As浓度继续增加,Fe3O4@TiO2复合材料对As的吸附趋势逐步放缓,最终近似于平衡。随着n(TiO2)∶n(Fe3O4)增加,Fe3O4@TiO2复合材料对As的吸附效率各不相同,且当n(TiO2)∶n(Fe3O4)=0.5时,Fe3O4@TiO2复合材料对As的平衡吸附量最大。
![]() —FT-1.0;
—FT-1.0; ![]() —FT-0.1;
—FT-0.1; ![]() —FT-0.5。
—FT-0.5。
图4 Fe3O4@TiO2复合材料对As的吸附等温线和甲基橙被Fe3O4@TiO2复合材料的光催化降解曲线
Fig.4 Adsorption isotherms of As and photo-catalysis degradation of MO by Fe3O4@TiO2 composite
考虑到污染水体中通常是有机无机复合污染,因此,探究该复合材料在甲基橙催化降解方面的应用潜能(图4b)。首先,在实际环境条件下进行吸附,反应温度为25 ℃,溶液pH=8,避光处理。约30 min后,甲基橙在Fe3O4@TiO2复合材料上的吸附基本平衡,当n(TiO2)∶n(Fe3O4)=0.5时,Fe3O4@TiO2复合材料吸附甲基橙的平衡吸附量最大。吸附饱和后,外加可见光照射,催化降解90 min后,光催化过程基本结束。
3 结 论
1)Fe3O4@TiO2复合材料为典型的核壳结构,内核为Fe3O4,外壳为以(101)晶面为主的锐钛矿TiO2,2种组分进行化学结合,在结合过程中TiO2发生还原形成Ti3+,Ti3+的存在更有利于复合材料捕获光致电子,促进电子和空穴的分离。
2)光谱学手段证明了Fe3O4@TiO2复合材料中2种组分的有机结合,一方面在很大程度上缩小了带隙宽度,进一步提高了对可见光的响应,另一方面,TiO2在受到光激发后产生光致电子与空穴的分离,电子进一步传递给内核的Fe3O4,有利于遏制光致电子与空穴的结合。
3)当n(TiO2)∶n(Fe3O4)=0.5时,Fe3O4@TiO2复合材料对As的吸附效果最佳,同时,甲基橙被光催化降解的效果最佳。
[1] 李鸿炫, 胡金星, 林伟,等. 重金属-有毒有机物复合污染土壤的过硫酸盐氧化修复模拟研究[J]. 环境科学学报, 2017, 37(9):3553-3560.
[2] 周振, 姚吉伦, 庞治邦,等. 跨膜压差和膜面流速对磁絮凝延缓陶瓷微滤膜通量衰减的影响[J]. 环境工程, 2017, 35(6):10-14.
[3] Moon Gunhee, Kim Donghyo, Kim Hyoungil, et al. Platinum-like behavior of reduced graphene oxide as a cocatalyst on TiO2 for the efficient photocatalytic oxidation of arsenite[J]. Environmental Science & Technology Letters, 2014, 1(2):185.
[4] Zhou Zhen, Yu Yaqin, Ding Zhaoxia, et al. Modulating high-index facets on anatase TiO2[J]. European Journal of Inorganic Chemistry, 2018, (6):683-693.
[5] Zhen Zhou, Yao Jilun, Xing Zhang, et al. Enhanced effluent quality of ceramic membrane ultrafiltration combined with UV/TiO2 photocatalysis[J]. Nature Environment & Pollution Technology, 2017, 16(3):695-702.
[6] Jieying Jing, Jing Li, Jie Feng, et al. Photodegradation of quinoline in water over magnetically separable Fe3O4/TiO2, composite photocatalysts[J]. Chemical Engineering Journal, 2013, 219(3):355-360.
[7] Tiejun Xin, Mingliang Ma, Hepeng Zhang, et al. A facile approach for the synthesis of magnetic separable Fe3O4@TiO2, core-shell nanocomposites as highly recyclable photocatalysts[J]. Applied Surface Science, 2014, 288(1):51-59.
[8] Li Wei, Deng Yonghui, Feng Shanshan, et al. A versatile kinetics-controlled coating method to construct uniform porous TiO2 shells for multifunctional core-shell structures[J]. Journal of the American Chemical Society, 2012, 134(29):11864-11847.
[9] Gang Liu, Yang Huagui, Jian Pan, et al. Titanium dioxide crystals with tailored facets[J]. Chemical Reviews, 2014, 114(19):9559.
[10] Chen Fenghua, Yan Fufeng, Chen Qingtao, et al. Fabrication of Fe3O4@SiO2@TiO2 nanoparticles supported by graphene oxide sheets for the repeated adsorption and photocatalytic degradation of rhodamine B under UV irradiation[J]. Dalton Transactions, 2014, 43(36):13537.
[11] Zhang Jun, Qian Lisha, Yang Lingxia, et al. Nano scale anatase TiO2, with dominant {111} facets shows high photocatalytic activity[J]. Applied Surface Science, 2014, 311(9):521-528.