0 引 言
近几年来,我国的工业高速发展,取得了举世瞩目的经济成绩,但同时也带来了日益严重的环境污染问题。挥发性有机物(VOCs)[1]是造成空气污染的主要因素之一,不仅导致了光化烟雾、酸雨以及臭氧枯竭等环境问题[2-4],还引起了诸如儿童白血病、哮喘、癌症等恶性疾病[5-7]。为了治理大气污染,我国相继出台了《环境空气质量标准》、《重点区域大气污染防治“十二五”规划》等相关政策,致力于减少VOCs的排放,改善由此产生的环境污染问题,以期降低VOCs对人类健康的影响。很多传统技术可用于VOCs处理,如吸附法、燃烧法和冷凝法[8]等,但各自都存在缺陷。吸附法和燃烧法会造成二次污染,而冷凝法灵活性差,设备和运行费用较高[9]。为了实现高效环保的降解目标,亟须探索出更优质的VOCs降解技术。许多研究表明,低温等离子体技术是一种非常有效的新型VOCs降解技术,由于其设备简单,处理快捷、普适性强等优点得到广泛的重视和研究[10-11],并且在某些领域已经得到应用。
在低温等离子体中,由于电子的质量很小,易被电场加速变成高能电子,所具有的能量将远大于分子内各种化学键的键能,导致电子与分子间非弹性碰撞的发生。碰撞会产生大量的离子、自由基和UV光子。这些自由基(如N、O·、H·、OH·)具有非常强的氧化性,与VOCs接触后,能迅速地发生氧化反应,使化合物最终降解为CO2和H2O。低温等离子体作为一种高效的VOCs降解技术,通常采用电晕放电[12]、介质阻挡放电[13]以及填充床反应器放电[14-16]进行废气处理。其中,介质阻挡放电作为一种常温常压下获得等离子体的主要方式,相对于电晕放电有更好的放电均匀性和更高的电子密度,因此被广泛应用于各种污染物的降解[17-19]。
尽管低温等离子体技术在VOCs降解中表现出较高效率,但目前也存在VOCs降解机理不清、降解产物不可控、能耗偏高等问题,需要更深入的研究和探索。因此,本文选取2类结构差异明显的VOCs,从电离能、氢含量和沸点3个方面进行对比研究,分析分子结构对降解的影响,探索低温等离子体降解VOCs的机理。VOCs种类繁多,其中芳香烃和烷烃是2类常见的挥发性有机物。芳香烃拥有苯环结构,而烷烃是开链的饱和烃,是2种非常典型的VOCs分子结构。从芳香烃和烷烃中选择6种VOCs进行实验,包括苯、甲苯、二甲苯、戊烷、正己烷和环己烷,以期获得各自的降解规律和降解影响因素。
1 实验部分
1.1 实验装置
如图1所示,实验用空气压缩机来产生压缩空气,经纯净气体发生器(派克,75-52NA,美国)干燥后分成2路:a路空气通向装满液态VOCs的不锈钢鼓泡罐,通过鼓泡法得到VOCs气体,并把气体贮存在100 L的储气罐(浩翔,中国)中;b路空气与储气罐输出的VOCs气体在装满水晶球的玻璃容器中充分混合,混合后的气体进入介质阻挡放电反应器进行降解处理,其中混合气的总流量为2 L/min。通过质量流量控制器(MFC)(七星D07,中国)调节2路气体的流量,可以实现对VOCs初始浓度的控制。本文中,为了对比6种VOCs气体的降解效果,其初始浓度均固定在100 mg/kg。
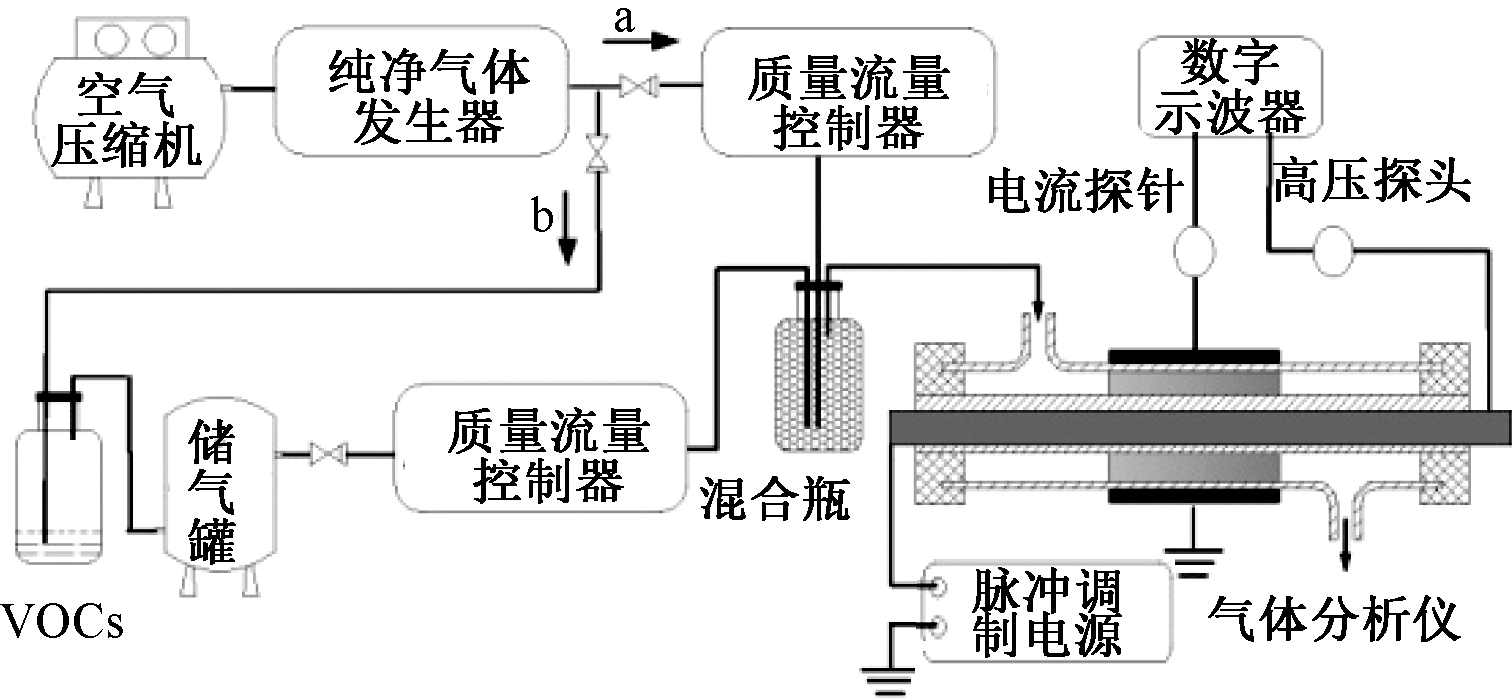
图1 实验装置
Fig.1 Experimental setup
介质阻挡放电反应器由共轴的圆柱形石英管组成。两石英管长度均为360 mm,其中内管的内径为3 mm,壁厚为1 mm,外管的内径为17 mm,壁厚为1.5 mm。将一根直径为3 mm的铜棒置于内管的内部,作为反应器内电极;在外管的外壁上覆盖宽度为120 mm的铜网,作为反应器外电极。反应器的放电间隙为6 mm,放电区间的长度为120 mm。反应器的两端用中心开孔的聚四氟乙烯塞密封,防止有害的VOCs气体泄漏。实验中,内电极连接脉冲调制电源(苏曼,CTP-2000 K,中国)的高压端,外电极接地。数字脉冲发生器(苏曼,PC-07,中国)把电源的占空比和频率分别固定在20%和150 Hz。课题组之前的研究表明,脉冲等离子体可以极大地提升能量效率[20-21]。
脉冲调制电源在DBD反应腔上的激励电压和放电电流分别用高压探头(Tektronix,P6015 A,1000X)和电流探针(ETA,5315,1X)测量,并由示波器(Tektronix,MDO3032,中国)进行记录和存储。VOCs的浓度由气相色谱仪(锐敏,GC2060,中国)(色谱柱:SE-54,进样器温度:120 ℃,FID温度:140 ℃,柱炉温度:120 ℃)利用火焰电离检测器(FID)进行测量。反应过程中产生的臭氧浓度由多功能复合气体分析仪(科尔诺,GT-2000-K3,中国)测得。
1.2 测量方法
能量密度(specific input energy,SIE)常被用来评价VOCs的降解,是一个关键参数。能量密度定义为[22]:
(1)
式中:SIE为能量密度,J/L;Q为总气体流量,L/min;P为反应器的放电功率,W。放电功率可由式(2)计算得到[20]:
P=f![]() V(t)I(t)dt
V(t)I(t)dt
(2)
式中:T为脉冲电源的脉冲宽度,s;f为调制脉冲频率,Hz;V(t)为高压探头在DBD反应器上测得的激励电压,V;I(t)为电流探针在DBD反应器上测得的放电电流,A。
VOCs的降解效率计算方法如式(3)所示[21]:
(3)
式中:DE为VOCs的降解效率;Cin和Cout分别为在反应器入口和出口测量到的VOCs浓度,mg/kg。
2 结果与分析
2.1 电离能对芳香烃和烷烃降解的影响
图2给出了6种VOCs的降解效率DE随SIE的变化曲线。可知:VOCs的降解效率随着SIE的增大而升高。当SIE达到一定程度时,降解效率逐渐趋于饱和。6种VOCs中,二甲苯最易降解,而戊烷最难降解。为了更清晰地比较降解的难易程度,进一步分析给出各种VOCs的降解反应速率常数。

![]() —戊烷;
—戊烷; ![]() —正己烷;
—正己烷; ![]() —环己烷;
—环己烷; ![]() —苯;
—苯; ![]() —甲苯;
—甲苯; ![]() —二甲苯。
—二甲苯。
图2 降解效率和能量密度的关系
Fig.2 Decomposition efficiency (DE) as a function of SIE
在多数情况下,低温等离子体降解VOCs满足一阶动力学方程[23-24]:
(4)
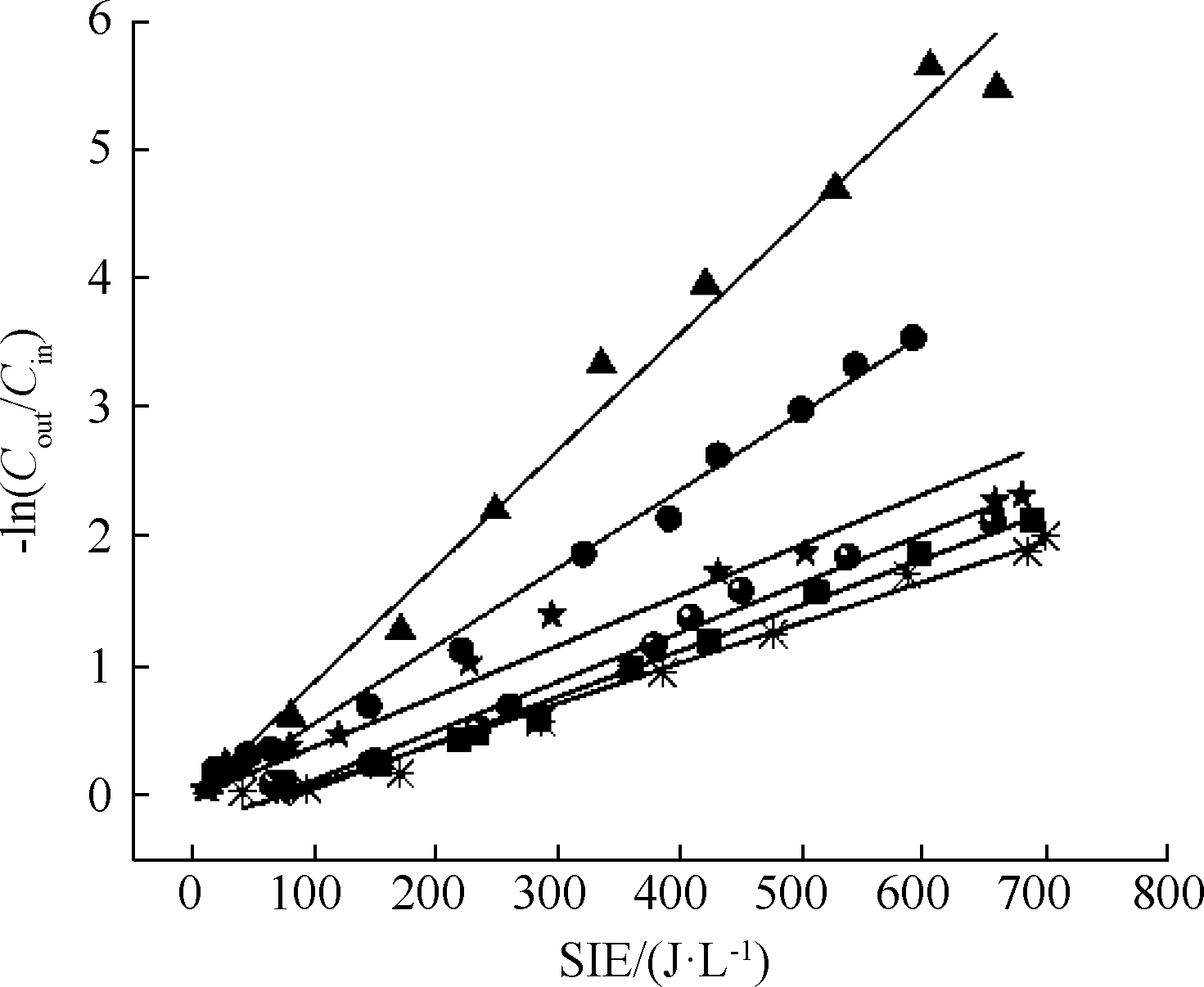
式中:k为反应速率常数,L/J。式(4)是在实验中建立的半经验模型,并不涉及等离子体内部发生的具体化学反应,而是给出一个整体的动力学关系。为不同的VOCs设置相同的实验条件,可以根据反应速率常数的大小比较不同VOCs的降解难易程度,反应速率常数越大,VOCs就越容易被降解。图3给出了6种VOCs的-ln(Cout/Cin)值与SIE的关系。可知:两类VOCs的降解过程基本上满足一次线性关系,通过线性拟合可以得到各VOCs的反应速率常数,如表1所示。由此可见,二甲苯具有最大的k值,而戊烷最小,同时实验选取的芳香烃类VOCs的降解效率均高于烷烃类VOCs。
![]() —戊烷;
—戊烷; ![]() —正己烷;
—正己烷; ![]() —环己烷;
—环己烷; ![]() —苯;
—苯; ![]() —甲苯;
—甲苯; ![]() —二甲苯。
—二甲苯。
图3 -ln(Cout/Cin)和能量密度的关系
Fig.3 -ln(Cout/Cin) as a function of SIE
表1 6种VOCs的反应速率常数
Table 1 The reaction rate constants of 6 kinds of VOCs
VOCs戊烷正己烷环己烷苯甲苯二甲苯k/(L·J-1)0.003130.003540.003790.003890.005990.00893
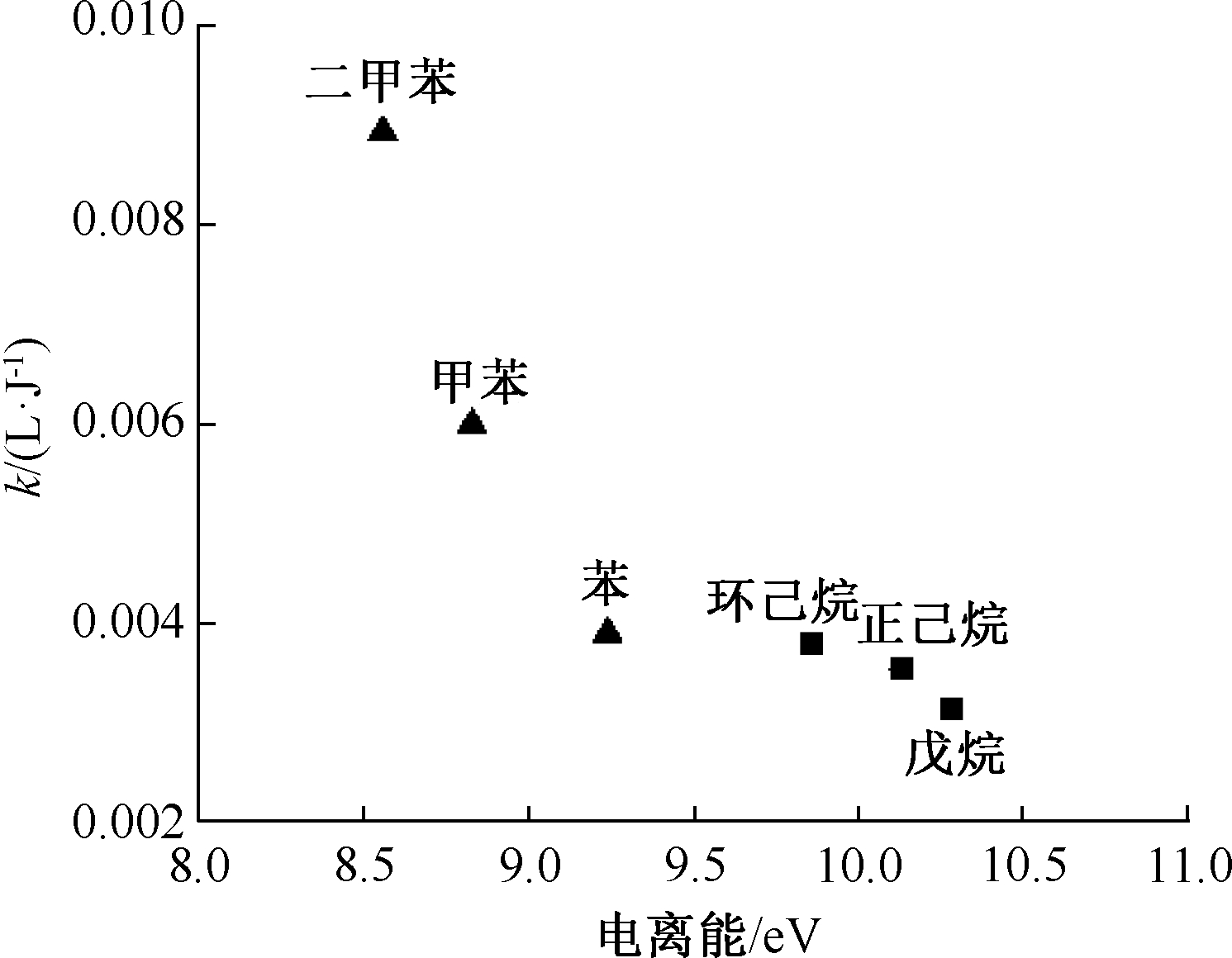
电离能是处于基态的气体原子或者分子失去1个电子所需要的能量。通常来说,第1电离能越大,就越难失去电子。表2列出了6种VOCs的电离能[25],图4所示为介质阻挡放电下6种VOCs反应速率常数与电离能之间的关系。反应速率常数与电离能存在明显的规律:随着电离能的增大,反应速率常数减小,VOCs降解难度增大,即降解效率变低。因此,电离能是影响VOCs降解的一个重要的参数,利用电离能和反应速率常数之间的规律,可以了解不同芳香烃类和烷烃类VOCs降解的难易程度,为工程应用提供指导。
表2 6种VOCs的电离能
Table 2 The ionization energy of 6 kinds of VOCs
VOCs戊烷正己烷环己烷苯甲苯二甲苯电离能/eV10.2810.139.869.248.838.56
![]() 烷烃;
烷烃;![]() 芳香烃。
芳香烃。
图4 6种VOCs反应速率常数与电离能的关系
Fig.4 Reaction rate constants of 6 kinds of VOCs as a function of ionization energy
2.2 氢含量对芳香烃和烷烃降解的影响
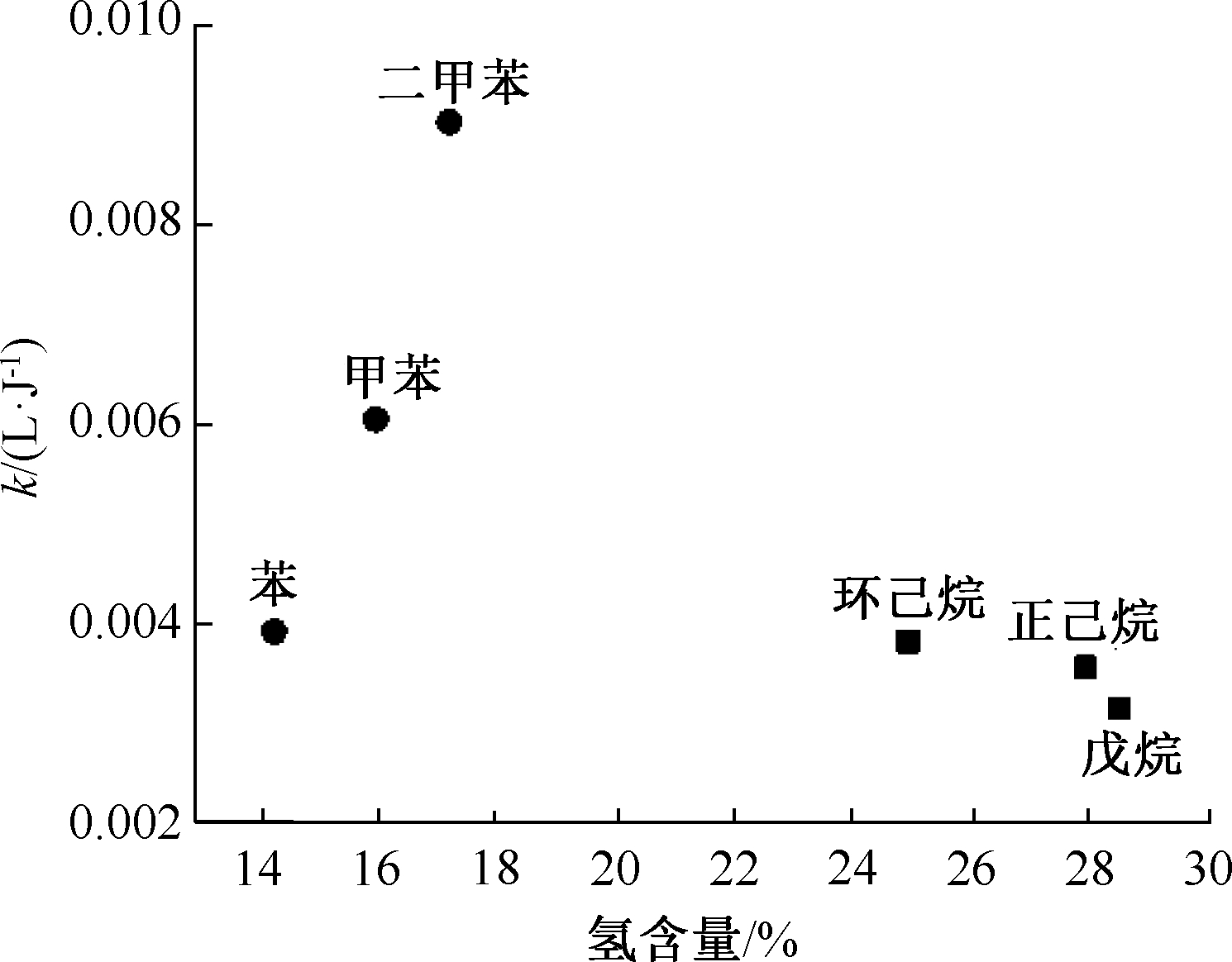
氢含量定义为氢原子在1个VOCs分子中所占的质量百分比。在芳香烃或者烷烃中,氢含量的大小与C—H单键的数量息息相关,随着碳原子数的增加,C—H单键的数量也在增加,相应的氢含量也会发生变化。所以在进行氢含量的研究时,要考虑到C—H单键数量的影响。如图5所示为6种VOCs反应速率常数和氢含量的关系。
![]() 烷烃;
烷烃;![]() 芳香烃。
芳香烃。
图5 6种VOCs反应速率常数与氢含量的关系
Fig.5 Reaction rate constants of 6 kinds of VOCs as a function of hydrogen weight fraction
由图5可知:氢含量和反应速率常数对芳香烃和烷烃有着不同的变化规律:对芳香烃来说,随着氢含量的增加,反应速率常数增大;而对烷烃来说,随着氢含量的增加,反应速率常数减小。这主要是因为烷烃和芳香烃有着不同的分子结构,造成了相反的变化趋势:烷烃是饱和烃,分子都是由单键构成,1个碳最多形成4个C—H键,随着碳原子数增加,势必要形成C—C单键,从而导致每个碳原子周围都会减少1个甚至全部的氢原子,所以当总的单键数量增加时(即碳原子数增加、C—H键数量增加),氢含量减小;而芳香烃是不饱和烃,除了单键以外,主要由大π键组成,当苯环上添加1个甲基时,这样1个新的碳原子就带来了3个氢原子,所以当总的单键数量增加时,氢含量增大。由上述讨论可以发现,芳香烃和烷烃的2种变化趋势内在原因相同:随着总的单键数量增加,反应速率常数变大。表3列出了每个VOC内部化学键的能量,其中,单键具有的能量远远低于大π键,这说明单键很容易与高能电子发生非弹性碰撞从而断裂,当单键数量越来越多时,脆弱的撞击节点也就越多,有机物就越容易被降解。这也造成了单键数量较少的芳香烃增加1个甲基时,反应速率常数大大增加,而由单键构成的烷烃增加1个甲基时,反应速率常数增幅较小,且3种烷烃的反应速率常数紧跟芳香烃。因此,氢含量可以用来单独预测芳香烃或者烷烃的降解效率,但是对于2种以上的VOCs,则需要考虑电离能才能给出正确结果。相比于氢含量,电离能对VOCs的降解具有更重要的影响。
2.3 沸点对芳香烃和烷烃降解的影响
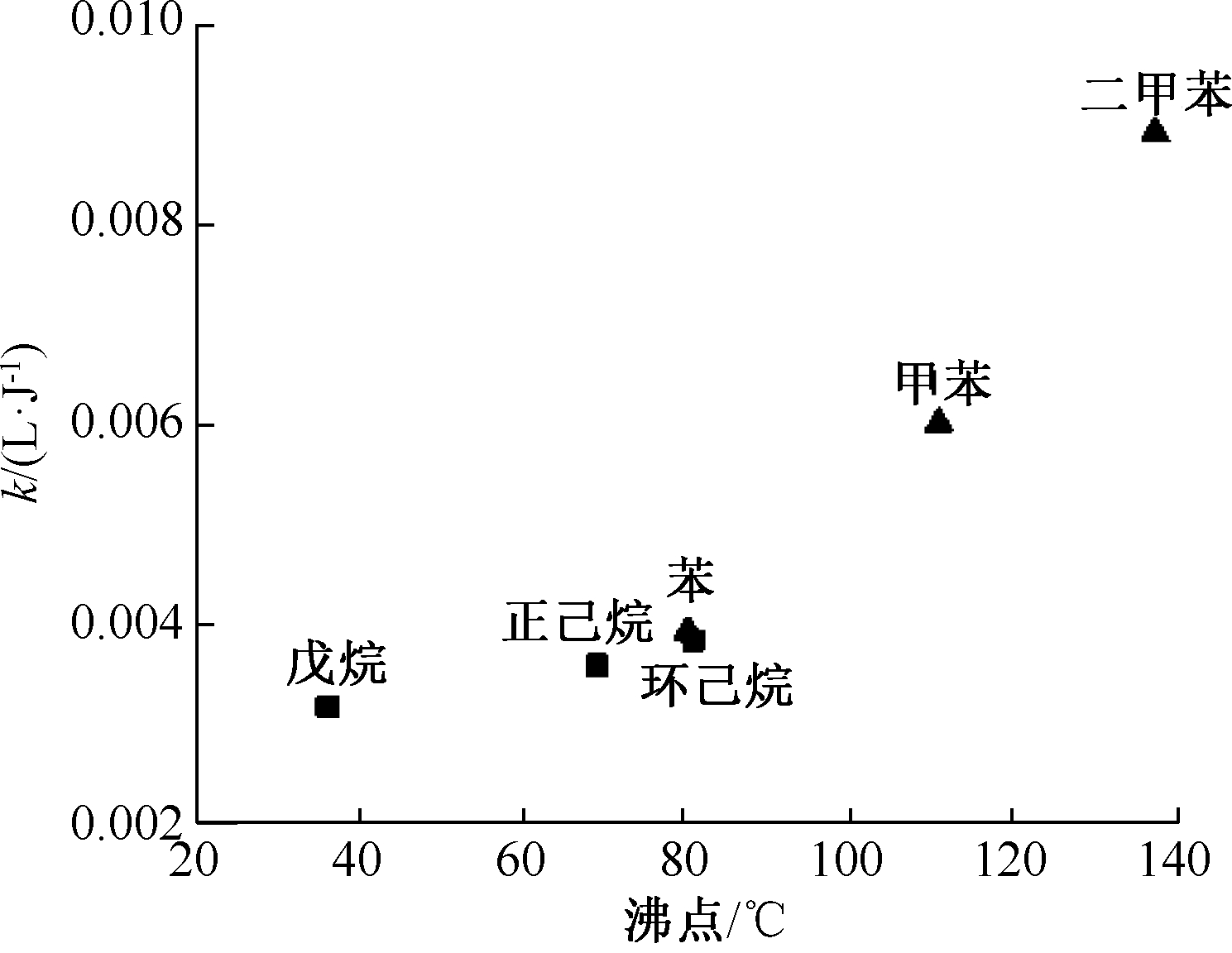
沸点是液体发生沸腾时的温度,在此温度下液体的饱和蒸气压和外界的分压相等。图6给出了6种VOCs反应速率常数和沸点之间的函数曲线。可知:反应速率常数与沸点之间也存在一定的规律,对于芳香烃或者烷烃来说,反应速率常数随着沸点的增加而增加。
![]() 烷烃;
烷烃;![]() 芳香烃。
芳香烃。
图6 6种VOCs反应速率常数与沸点的关系
Fig.6 Reaction rate constants of 6 kinds of VOCs as a function of boiling point
有机物沸点的高低取决于分子间引力的大小,对于结构相似的有机物来说,沸点由分子量决定。因为分子量越大,分子间引力就越大,沸点就越高,所以对芳香烃及烷烃来说,沸点随分子量增加而增加,反应速率常数也随之增大。而在这2类VOCs中,分子量的变化也就是单键数量的变化,因此沸点和氢含量的影响类似,都反映了化学结构对VOCs降解的影响。
表3 6种VOCs的不同键能
Table 3 The bond energy of 6 kinds of VOCs
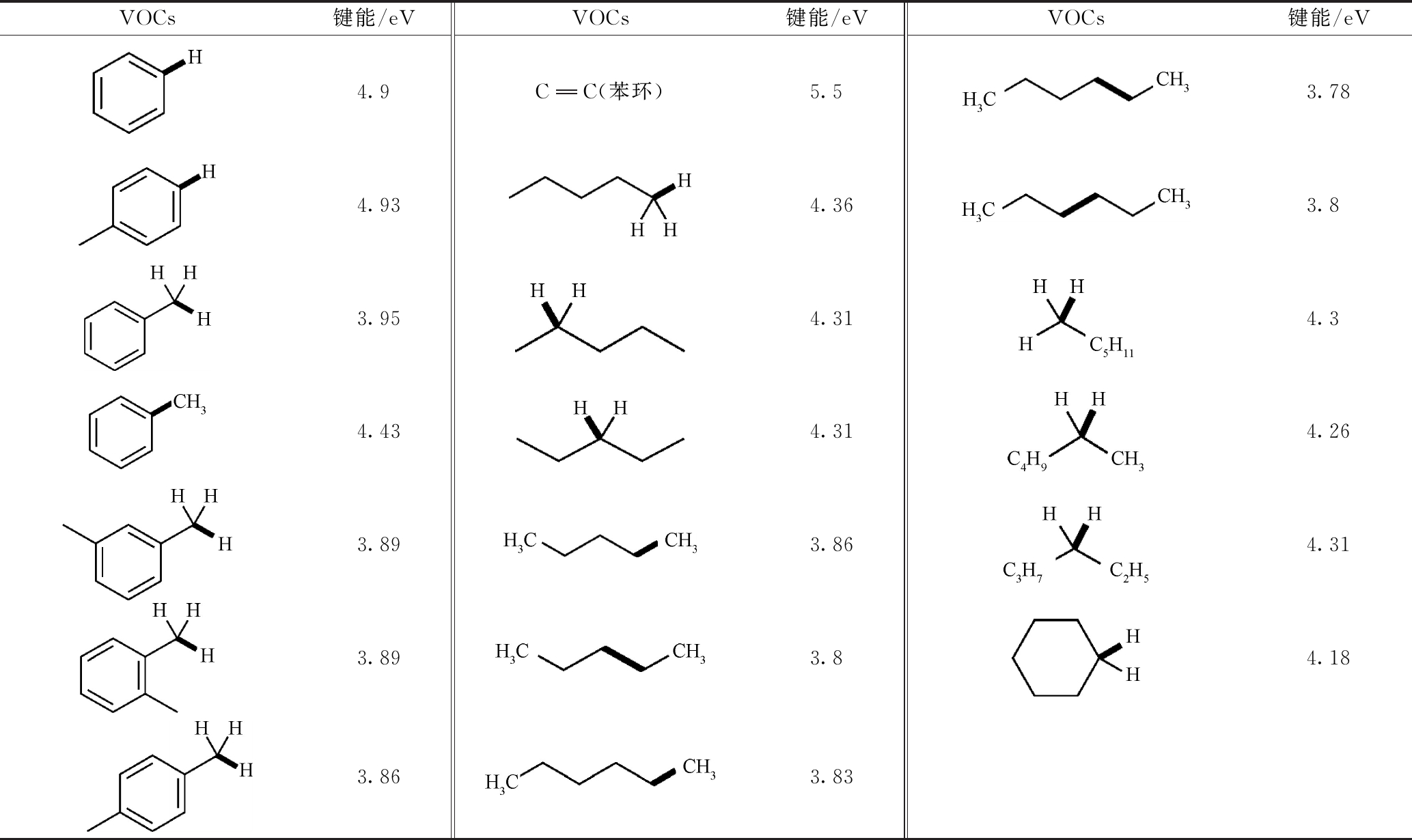
VOCs键能/eVVOCs键能/eVVOCs键能/eV4.9CC(苯环)5.53.784.934.363.83.954.314.34.434.314.263.893.864.313.893.84.18 3.863.83
3 总 结
在低温等离子体中,不同的化学结构对VOCs降解的影响不同。芳香烃中的苯环以及烷烃中的长链是2种典型的VOCs分子结构,本文在芳香烃和烷烃中选择6种常见的VOCs,从电离能、氢含量和沸点3个方面研究了不同化学结构VOCs的降解规律,主要结果如下:
1)电离能是影响VOCs降解的重要因素。对于2类VOCs来说,随着电离能增大,反应速率常数也在增大,即电离能越大,VOCs越难被降解。
2)氢含量对6种VOCs降解有着明显的影响,由于单键数量存在差异,芳香烃和烷烃存在不同的降解规律:对芳香烃而言,随着氢含量增大,反应速率常数增大;而烷烃的反应速率常数随着氢含量的增大而减小。
3)VOCs的沸点对降解效率也存在影响。对于芳香烃或者烷烃来说,随着沸点增大,反应速率常数也增大, 即VOCs更容易被降解。
本文只针对芳香烃和烷烃这2类典型的VOCs进行了对比研究。但在实际工业生产中,VOCs的种类繁多、成分复杂,其他种类的VOCs在低温等离子体作用下的降解规律仍需要更深入的研究,从而更全面地理解低温等离子体降解VOCs的机理。
[1] 梁钊堂. VOC类有毒空气污染物有效控制[J]. 中国资源综合利用, 2018, 36(3): 151-170.
[2] Chaichan M T, Abass Q A. Study of NOx emissions of S.I. engine fueled with different kinds of hydrocarbon fuels and hydrogen[J]. Al-Khwarizmi Engineering Journal, 2018, 6(2): 11-20.
[3] Vo T D H, Lin C, Weng C E, et al. Vertical stratification of volatile organic compounds and their photochemical product formation potential in an industrial urban area[J]. Journal of Environmental Management, 2018, 217: 327-336.
[4] Liu Y, Wang C H, Xiang F, et al. Pollution characteristics and source apportionment of VOCs at city centre of Kunming in summer and autumn[J]. DEStech Transactions on Engineering and Technology Research(icaenm), 2017.
[5] Hanna S R, Paine R, Heinold D, et al. Uncertainties in air toxics calculated by the dispersion models AERMOD and ISCST3 in the Houston ship channel area[J]. Journal of Applied Meteorology & Climatology, 2007, 46: 1372-1382.
[6] Boeglin M L, Wessels D, Henshel D. An investigation of the relationship between air emissions of volatile organic compounds and the incidence of cancer in Indiana counties[J]. Environmental Research, 2006, 100: 242-254.
[7] Sousa S I V, Alvim-Ferraz M C M, Martins F G. Health effects of ozone focusing on childhood asthma: what is now known-a review from an epidemiological point of view[J]. Chemosphere, 2013, 90: 2051-2058.
[8] 陈锐章. VOC处理技术综述[J]. 环境与发展, 2018(7): 98-100.
[9] An G, Sun Y, Zhu T, et al. Degradation of phenol in mists by a non-thermal plasma reactor[J]. Chemosphere, 2011, 84: 1296-1300.
[10] Raju B R, Reddy E L, Karuppiah J, et al. Catalytic non-thermal plasma reactor for the decomposition of a mixture of volatile organic compounds[J]. Journal of Chemical Sciences, 2013, 125(3): 673-678.
[11] Schiavon M, Torretta V, Casazza A, et al. Non-thermal plasma as an innovative option for the abatement of volatile organic compounds: a review[J]. Water, Air, & Soil Pollution, 2017, 228(10): 388-408.
[12] Marotta E, Schiorlin M, Rea M, et al. Products and mechanisms of the oxidation of organic compounds in atmospheric air plasmas[J]. Journal of Physics D—Applied Physics, 2010, 43 (12): 124011.
[13] Ye Z L, Zhang Y L, Li P, et al. Feasibility of destruction of gaseous benzene with dielectric barrier discharge[J]. Journal of Hazardous Materials, 2008, 156 (1/2/3): 356-364.
[14] Sugasawa M, Terasawa T, Futamura S. Additive effect of water on the decomposition of VOCs in nonthermal plasma[J]. IEEE Transactions on Industry Applications, 2010, 46 (5): 1692-1698.
[15] Zhu T, Wan Y D, Li H R, et al. VOCs decomposition via modified ferroelectric packed bed dielectric barrier discharge plasma[J]. IEEE Transactions on Plasma Science, 2011, 39 (8): 1695-1700.
[16] Veerapandian S K P, Leys C, Geyter N D, et al. Abatement of VOCs using packed bed non-thermal plasma reactors: a review[J]. Catalysts, 2017, 7(4): 113-145.
[17] Nguyen H P, Park M J, Kim S B, et al. Effective dielectric barrier discharge reactor operation for decomposition of volatile organic compounds[J]. Journal of Cleaner Production, 2018,198: 1232-1238.
[18] Mustafa M F, Fu X D, Liu Y J, et al. Volatile organic compounds(VOCs) removal in non-thermal plasma double dielectric barrier discharge reactor[J]. Journal of Hazardous Materials, 2018, 347: 317-324.
[19] 吴萧,刘盛余,何廷宇,等. 介质阻挡放电低温等离子体技术处理3种代表性VOC[J]. 环境工程学报, 2017, 11(10): 5502-5508.
[20] Ma T P, Jiang H D, Liu J Q, et al. Decomposition of benzene using a pulse-modulated DBD plasma[J]. Plasma Chemistry and Plasma Processing, 2016, 36(6): 1-11.
[21] Ma T P, Zhao Q, Liu J Q, et al. Study of humidity effect on benzene decomposition by the dielectric barrier discharge nonthermal plasma reactor[J]. Plasma Science and Technology, 2016, 18 (6): 686-692.
[22] Manley T C. The electric characteristics of the ozonator discharge[J]. Transactions on Electrochemical Society, 1943, 84(1): 83-96.
[23] Kim H H, Prieto G, Takashima K, et al. Performance evaluation of discharge plasma process for gaseous pollutant removal[J]. Journal of Electrostatics, 2002, 55: 25-41.
[24] Anderson G K, Snyder H, Coogan J. Oxidation of styrene in a silent discharge plasma[J]. Plasma Chemistry and Plasma Processing, 1999, 19: 131-151.
[25] Lias S G, Bartmess J E, Liebman J F, et al. Gas-phase ion and neutral thermochemistry[J]. Journal of Physical & Chemical Reference Data, 1988, 17(S1).