0 引 言
我国汽车零部件产业的迅速发展,产品的喷漆环节也随之产生了大量废水[1]。废水中含有浓度较高的酯类、苯类和助剂等有机污染物和漆渣,部分污染物具有高毒性,甚至被列入我国水中优先控制污染物名单。废水经过生化或者化学氧化工艺处理后,出水COD和色度很难达到GB 8978—2002《污水综合排放标准》或处理成本较高[2-3]。目前吸附技术为深度处理有机废水的主流技术[4-5],但吸附处理喷漆废水的研究鲜有报道。
制备吸附性能高、易于解吸或易于资源化的吸附材料一直是吸附领域研究的热点。一些比表面积大、活性位点多的吸附材料被广泛应用于吸附领域,如活性炭、生物质、分子筛和天然物质等[6-9]。褐煤是一种具有较高机械强度的天然有机岩,储量丰富且价格低。褐煤因含有碳氢化物的凝胶组分和衍生的—OH、—COOH、—COO等官能团而具有较强的吸附能力,可为有机废水的深度处理提供一种良好的吸附材料。但天然褐煤比表面积小,吸附能力弱,所以通常将其活化改性来提升其吸附性能[10]。研究表明,褐煤采用物理-化学方法改性后,孔道得到疏通,比表面积增大,吸附位点增加,同时也能协同活化其他活性位点,吸附能力得到强化[11]。目前褐煤或改性褐煤吸附处理含有单一组分有机物的废水研究较多[12-13],但对含有多种复杂组分综合废水的研究较少,应给予更多关注。
本文利用浓H2SO4活化改性的褐煤,探索其处理含有复杂多组分有机物喷漆废水的可行性,分析其吸附热力学及动力学行为,以期为汽车零部件产业喷漆废水的深度处理提供有效方法。
1 实验部分
1.1 材料与仪器
废水取自锦州某汽车零部件企业全自动喷漆线Fenton法处理废水工艺中水,ρ(COD)为324 mg/L,pH为8.4,色度为26倍。将水样进行减压蒸发浓缩,使ρ(COD)为1000 mg/L,作为实验储备液,使用液由储备液配制。
褐煤取自内蒙古平庄煤业集团,主要成分(以质量分数计)为:水分2.36%,灰分8.80%,挥发分33.14%,固定碳55.70%。密度为1.13×103 kg/m3。
实验中所用硫酸、氢氧化钠、重铬酸钾、硫酸亚铁铵等试剂均采用分析纯或化学纯。
吸附剂表征采用JEOL电子JSM-6510型扫描电镜(SEM)、岛津IRPrestige-2傅里叶红外光谱仪、贝士德3H-2000BET-A型比表面积测试仪。
1.2 实验方法
1.2.1 褐煤改性
取破碎后(-80~+100)目的褐煤粉,用蒸馏水冲洗去掉杂质和部分灰分,烘干。按液固比4∶1将H2SO4(质量分数为98%)缓慢加入煤粉中并搅拌,置于回流烧瓶中,135 ℃加热3 h。加热完毕后自然放置12 h,分离液体,改性产物用蒸馏水洗至中性,制得改性褐煤。
1.2.2 吸附实验
影响吸附的主要因素包括初始pH值、吸附时间(t)、体系温度(T)和吸附剂投加量,采用静态实验方法依次确定。每个因素所确定的最佳条件值作为下一因素最佳水平的实验条件。
pH值确定初始条件:改性褐煤投加量为10 g/L,T为20 ℃,t为60 min。
实验方法:取250 mL三角烧瓶若干,分别加入100 mL水样(ρ(COD)为324 mg/L),调节pH值,再加入一定量的改性褐煤,设置温度并振荡,吸附结束后静置过滤,取上清液测定COD。
静态实验条件见表1。
表1 静态实验条件
Table 1 Conditions of the static experiment
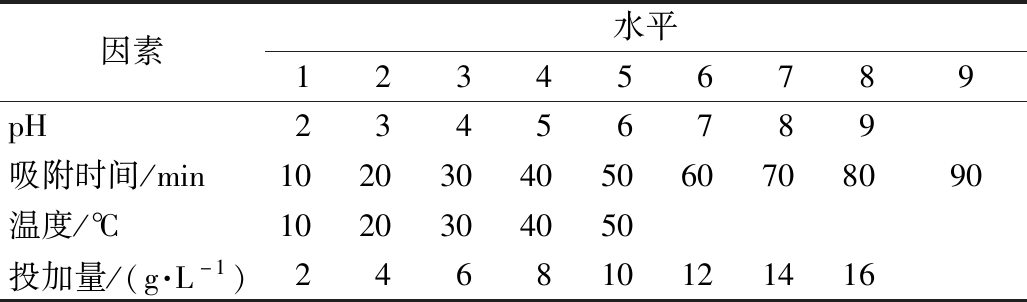
因素水平123456789pH23456789吸附时间/min102030405060708090温度/℃1020304050投加量/(g·L-1)246810121416
吸附等温实验:取7个250 mL锥形瓶,分别加入100 mL水样,使用液ρ(COD)分别为100,200,300,400,500,600,700 mg/L,调节pH值和吸附时间为最佳水平,改性褐煤投加量为10 g/L,并分别将其置于恒温水浴振荡器中,温度分别设置为10,20,30 ℃。实验结束后,过滤取上清液测定COD。
动力学实验:取9个250 mL锥形瓶,分别加入100 mL水样,ρ(COD)为324 mg/L,pH、温度和投加量分别设置为最佳水平,每10 min取样1次,过滤取上清液测定COD。
1.3 检测与指标计算
褐煤改性前后形貌特征采用SEM表征,化学结构特征采用傅里叶红外光谱仪表征,比表面积采用比表面积测试仪测定。
COD采用HJ 828—2017《水质 化学需氧量的测定 重铬酸盐法》测定。
实验结束后,计算参数指标包括COD去除率(%)、t时刻吸附量(qt,mg/L)或平衡吸附量(qe,mg/g)。
2 结果与讨论
2.1 改性褐煤空隙结构及官能团特征
褐煤改性前后SEM形貌表征(图1)和比表面积测试表明:改性褐煤呈现了发达的蜂窝状孔隙结构,比表面积由原来的274.62 m2/g上升至856.27 m2/g,说明浓H2SO4是良好的改性剂。浓H2SO4改性为有机物与改性褐煤的相互作用提供了良好的接触条件。

图1 改性褐煤的微观结构
Fig.1 Microstructure of the modified lignite
红外光谱特征表明(图2):褐煤改性后化学结构发生了重要变化,在波数1190 cm-1处出现了—SO3H的伸缩振动峰,—SO3H键合至褐煤的多环芳香结构和侧链中,丰富了其官能团结构。在各波数处的—C![]() O—、—COOH、—OH、—C—H等官能团伸缩振动峰被强化,说明浓H2SO4明显活化了吸附位点,强化了吸附位点条件。
O—、—COOH、—OH、—C—H等官能团伸缩振动峰被强化,说明浓H2SO4明显活化了吸附位点,强化了吸附位点条件。
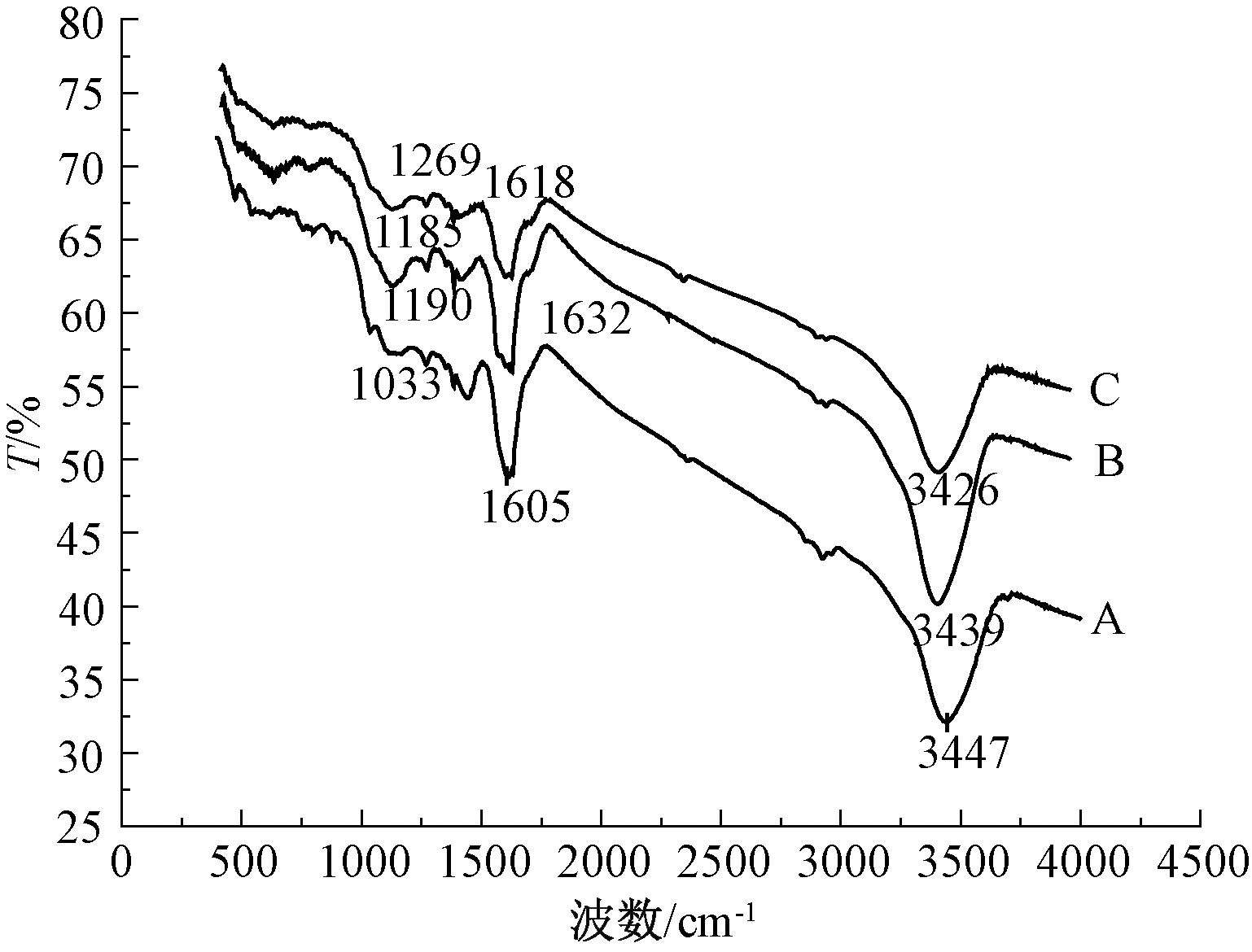
A—褐煤; B—改性褐煤; C—吸附后的改性褐煤。
图2 褐煤改性前后红外光谱(FTIR)特征
Fig.2 FTIR of lignite, modified lignite and modified lignite after adsorption
2.2 改性褐煤对喷漆废水有机物的吸附特性
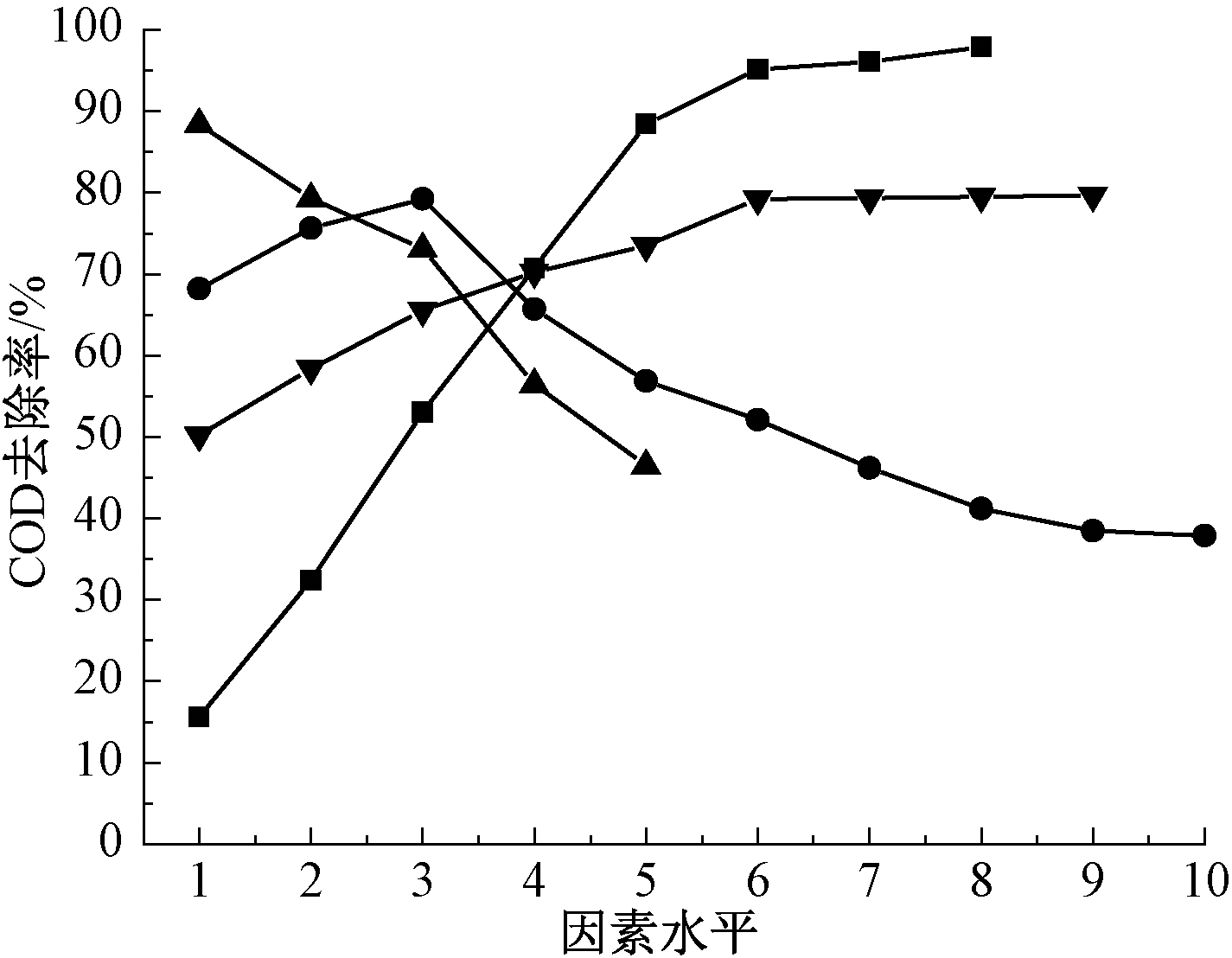
pH值、吸附时间、温度和投加量等因素对改性褐煤吸附喷漆废水有机物具有重要影响(详见图3),并显示了改性褐煤对喷漆废水有机物具有良好的吸附能力。
![]() —pH;
—pH; ![]() —t;
—t; ![]() —T;
—T; ![]() —投加量。
—投加量。
图3 改性褐煤吸附去除COD的工艺条件
Fig.3 Removal rate of COD treated by modified lignite
pH为2~9的体系中,COD去除率先增大后减小,当pH=4时COD去除率达到79.2%。当体系呈碱性后,喷漆废水中酯类有机物发生水解,虽然利于酯类有机物水解产物的吸附,但改性褐煤的酸性活性基团被中和,活性位点数量不足限制了对酯类物质的吸附[14],致使COD去除率下降。pH<4时,改性褐煤的活性位点被大量的H+占据,有机物失去了部分吸附位点,导致废水中酯类有机物去除率不高,但却非常有利于烃类、酚类有机物的吸附[15],因此COD去除率仍然较高。从总体的COD去除率判断,pH=4时,改性褐煤表面的电荷特性更加适合喷漆废水中复杂多组分有机物的吸附。因此,吸附过程宜在酸性体系中进行,pH=4为体系酸碱度环境的最佳水平。
由图3可知:吸附时间对改性褐煤吸附废水中的有机物呈现逐渐增加趋势,当在10 min时,COD去除率达到50.0%以上,这是因为有机物与改性褐煤丰富的活性位点快速结合所致,范德华力起到至关重要的作用。当吸附时间达到60 min时,吸附基本达到饱和,COD去除率在70.0%以上,活性位点基本被完全占据,吸附速率和解吸速率达到平衡。从总体吸附平衡过程而言,改性褐煤吸附有机物是一个较为快速的过程,但比活性炭吸附有机物的平衡时间略长[8],这可能是活性炭吸附有机物为物理吸附,而改性褐煤吸附有机物除物理吸附外,还存在官能团与有机物的成键作用,因此需要更长时间才能达到吸附平衡。图2中改性褐煤吸附后红外光谱(C)中官能团的伸缩振动峰减弱也说明了喷漆废水中有机物与官能团发生了化学键合作用。因此,本研究确定吸附工艺的接触时间应≥60 min。
由图3可知:吸附体系温度与COD去除率呈负相关。在T<20 ℃时,改性褐煤对废水COD去除率可达80.0%以上,表明低温有利于吸附,吸附过程应是一个放热过程,这与煤活性焦、活性炭低温下易于吸附有机物有相似之处[8, 10, 16-17]。这是因为温度高时,虽然活性位点也略微增多,但也会引起由水分子通过氢键形成的水分子簇的显著增加[18],水分子簇阻塞了改性褐煤的通道,吸附位点不能被充分利用,导致COD去除率降低。高温虽有利于有机物与改性褐煤官能团的化学成键反应,但是实验结果表明,较高的温度并不是COD去除率的有利因素,因此吸附过程宜在较低温度下进行。由于喷漆车间废水温度一般为10~15 ℃,因此采用改性褐煤吸附深度处理有机废水工艺时不必采用温度调节措施。
由图3还可以看出:COD去除率随改性褐煤的投加量增加而升高,当投加量达到10 g/L时,COD去除率达到85%以上,废水ρ(COD)<50 mg/L时,可达GB 8978—2002一级标准(50 mg/L),改性褐煤的平衡吸附量为27.8 mg/g。考虑到实际使用中的材料成本,吸附体系中改性褐煤投加量为10 g/L即可。
对吸附饱和的改性褐煤进行解吸,因其浓水中含有大量有机物,再次进行废水处理将更加困难,因此在实际工业应用中,建议将吸附饱和的改性褐煤以及被吸附的有机物一起资源化焚烧处理[19]。
2.3 吸附等温模型
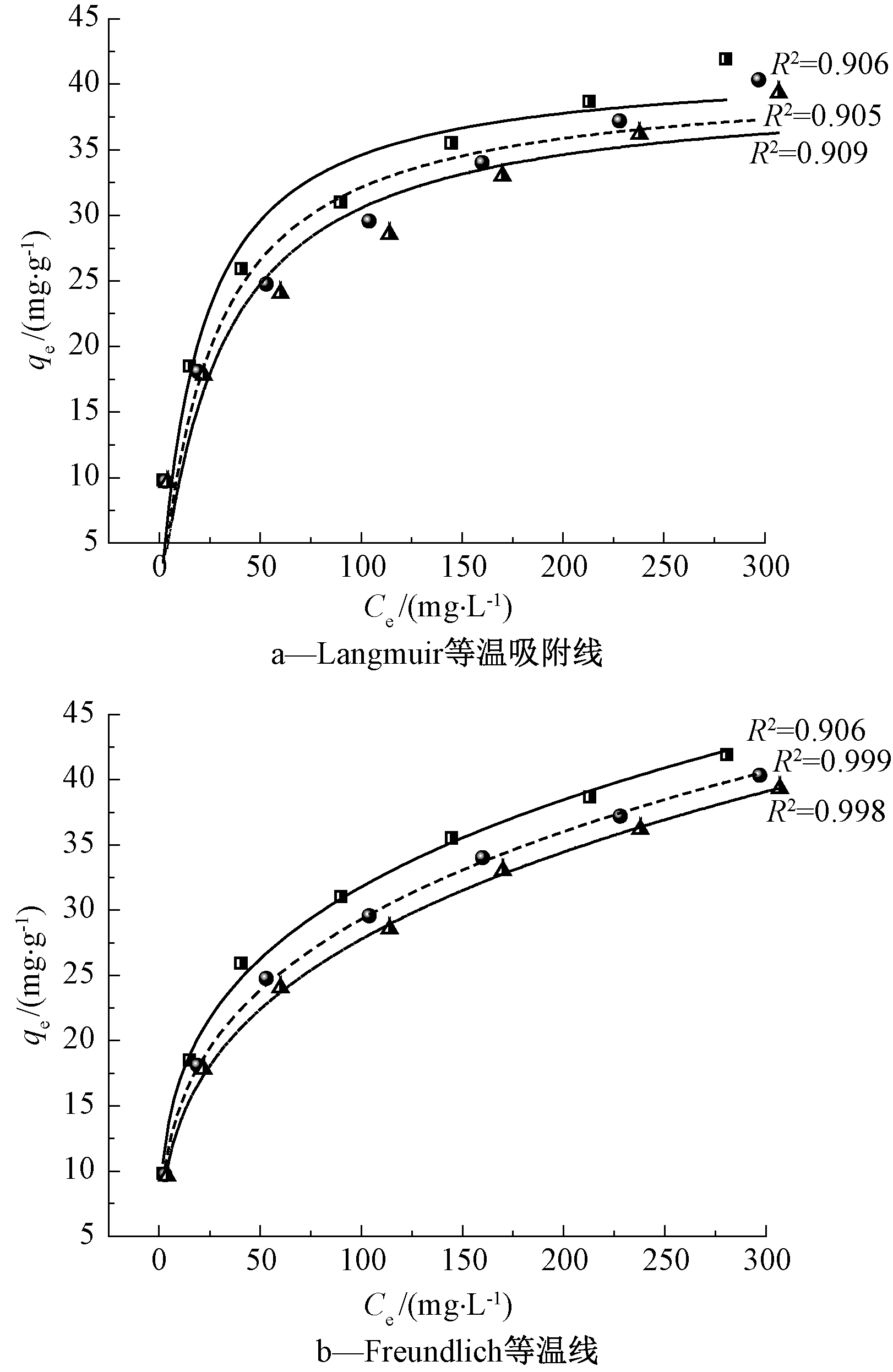
应用Langmuir和Freundlich等温吸附模型对等温吸附数据进行非线性拟合,拟合结果如图4所示。
![]() —10 ℃; --
—10 ℃; --![]() ---20 ℃;
---20 ℃; ![]() …30 ℃。
…30 ℃。
图4 Langmuir和Freundlich等温吸附线
Fig.4 Adsorption isotherm by model of Langmuir and Freundlich
由图4可知:Langmuir和Freundlich等温吸附模型相关系数均R2>0.9,但Freundlich等温吸附模型的R2值均大于Langmuir的R2值,这表明改性褐煤吸附漆废水有机物的等温吸附数据更符合Freundlich模型,并且改性褐煤对有机物的吸附为多层吸附,并兼有单层吸附[20]。图4还表明:改性褐煤的平衡吸附量与喷漆废水COD的初始浓度呈正相关,当废水ρ(COD)初始为700 mg/L时,平衡吸附量可达40 mg/g以上,这也证明有机物在改性褐煤上的吸附符合多层吸附的特征。
Freundlich模型拟合出的1/n<0.5,表明喷漆废水中的有机物利于被改性褐煤吸附。通过Langmuir模型拟合出的KL,计算出的分离因子RL介于0.029~0.20[21],也表明喷漆废水中的有机物利于被改性褐煤吸附。
2.4 吸附热力学
热力学参数ΔG0、ΔH0、ΔS0的计算如式(1)—(3)所示。
ΔG0=-RTlnKad
(1)
ΔG0=ΔH0-TΔS0
(2)
(3)
式中:ΔG0为吉布斯自由能,kJ/mol;ΔH0为焓变,kJ/mol;ΔS0为熵变,J/(mol·K);R为8.314 J/(mol·K);Kad为吸附分配比。
通过吸附分配比Kad计算得到吸附过程中ΔG0、ΔH0、ΔS0的量值。根据Khan的研究[22],lnKad可以由ln(qe/Ce)-qe一次拟合曲线的截距得到。ln(qe/Ce)-qe拟合曲线如图5所示。
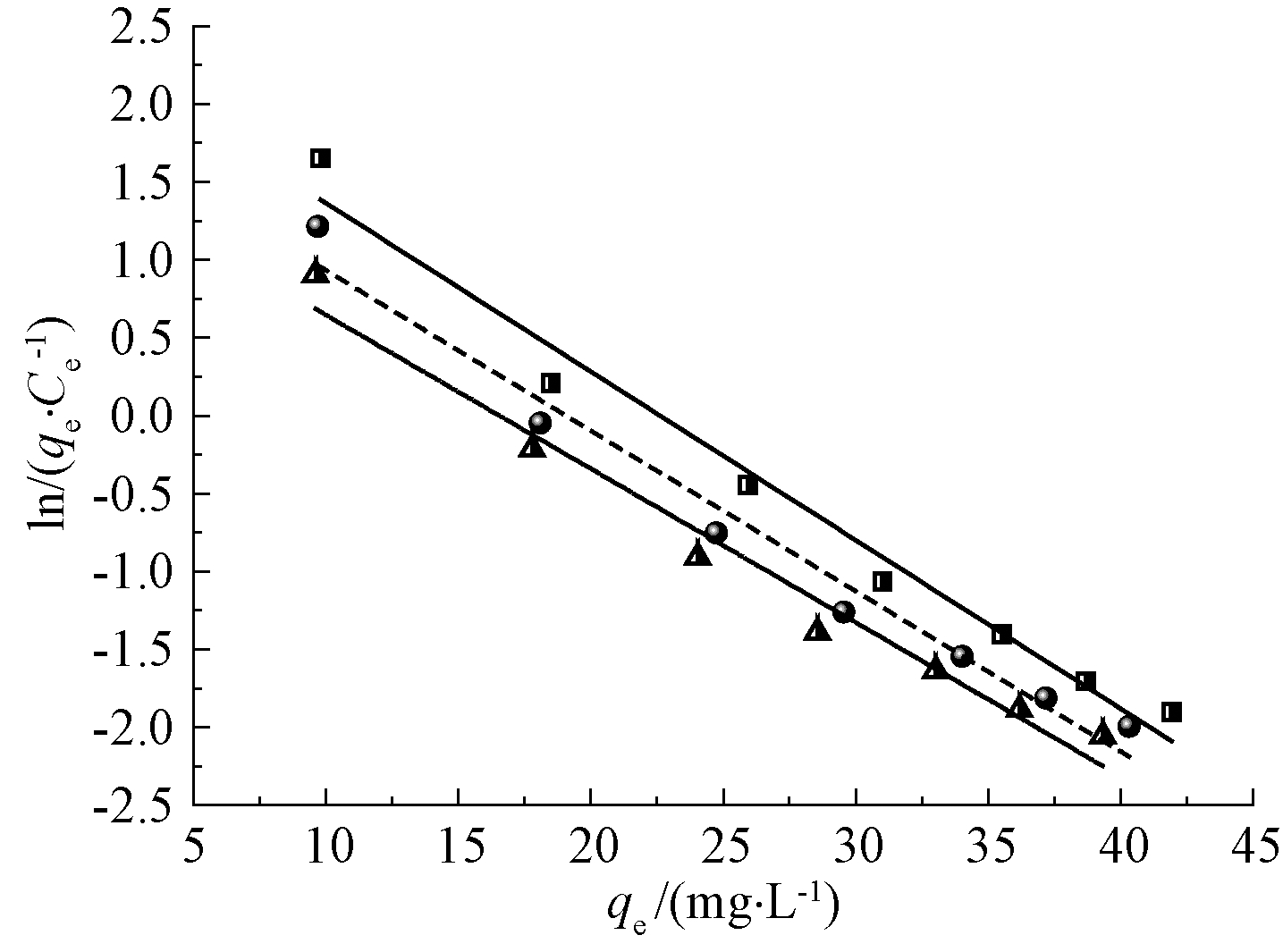
![]() —10 ℃(y=-0.10818x+2.445,R2=0.975); --
—10 ℃(y=-0.10818x+2.445,R2=0.975); --![]() ---20 ℃(y=-0.10303x+1.964,R2=0.971);
---20 ℃(y=-0.10303x+1.964,R2=0.971); ![]() …30 ℃(y=-0.09875x+1.636,R2=0.970)。
…30 ℃(y=-0.09875x+1.636,R2=0.970)。
图5 ln(qe/Ce)-qe拟合曲线
Fig.5 Fitting curves of ln(qe/Ce)-qe under different temperature
由图5得到10,20,30 ℃的3个lnKad,依据式(3)得到lnKad与1/T的一次曲线拟合方程,如图6所示。根据式(1)和lnKad与1/T的一次曲线拟合方程,ΔG0、ΔH0、ΔS0的计算结果如表2所示。
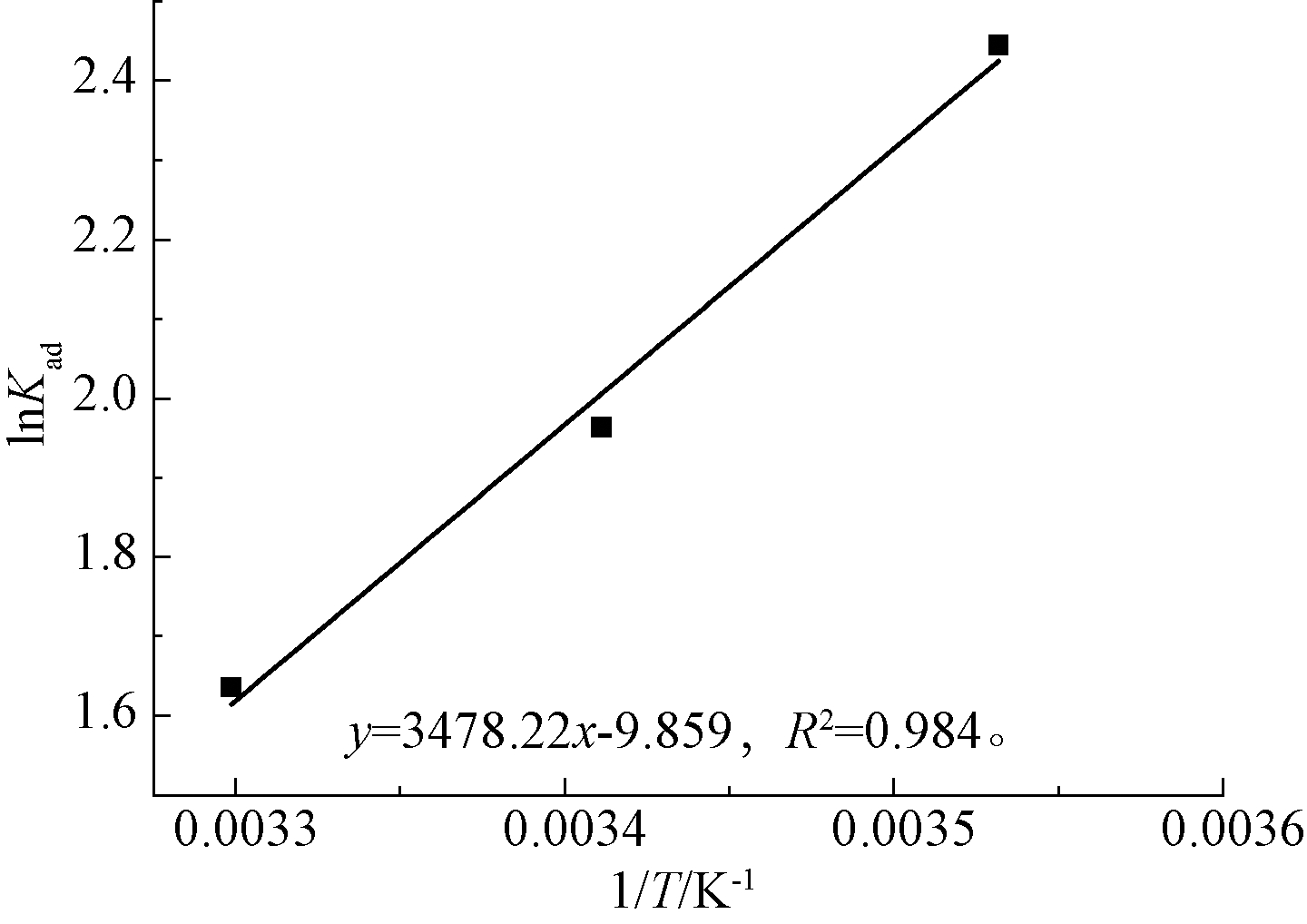
图6 lnKad与1/T的拟合曲线
Fig.6 Fitting curves of lnKad-1/T
表2 改性褐煤吸附喷漆废水有机物热力学参数
Table 2 Thermodynamic parameters for the adsorption of organic compounds onto modified lignite

T/KKadΔG0/(kJ·mol-1)ΔH0/(kJ·mol-1)ΔS0/(J·mol-1·K-1)298.152.445-5.76303.151.964-4.79-28.92-81.97308.151.636-4.12
由表2可知:3个温度时的ΔG0均为负值,表明废水中有机物倾向于从溶液中到达改性褐煤的内表面,在常温下既可自发进行;ΔH0为负值,表明吸附过程为放热过程,低温有力于吸附,进一步说明改性褐煤吸附喷漆废水中的有机物属于物理吸附;ΔS0为负值,表明有机物分子被吸附到改性褐煤表面上后,运动受到限制,致使吸附熵减小,有机物的自由度是减小的,但是吸附过程不是一个单一过程,从吸附体系的整体而言,系统的混乱度仍是增加的。ΔG0介于-5.76~-4.12 kJ/mol,表明吸附过程强化学键作用较少。
2.5 吸附动力学
在温度为298.15 K时,改性褐煤对喷漆废水中COD去除率、平衡吸附量与时间关系如图7所示。
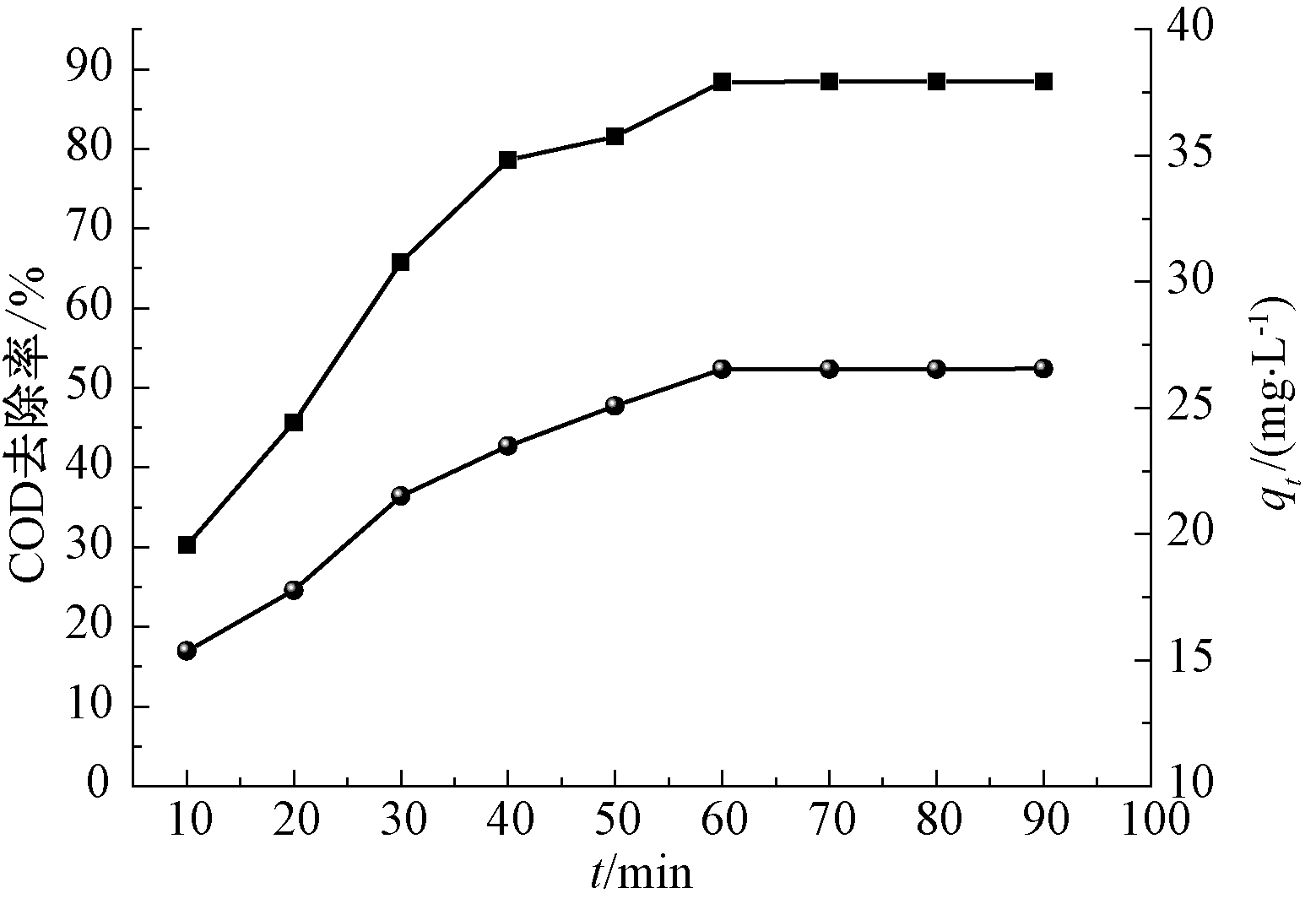
![]() —COD去除率;
—COD去除率; ![]() —qt。
—qt。
图7 最佳因素水平下COD去除率、qe与t的关系
Fig.7 Curves of COD remove rates and qe-t under the optimal condition
准一级反应动力学模型:
lg(qe-qt)=-k1t/2.303+lgqe
(4)
准二级反应动力学模型:
(5)
式中:qe为吸附平衡时的吸附量,mg/g;qt为t时吸附量,mg/g;k1为准一级吸附速率常数,min-1;k2为准二级吸附速率常数,g/(mg·min)。
根据图7吸附动力学数据,以t为横坐标,分别以lg(qe-qt)和t/qt为纵坐标,采用一次曲线分别拟合lg(qe-qt)-t和t/qt-t,拟合相关参数见表3。
表3 改性褐煤吸附喷漆废水有机物的吸附动力学模型参数(298.15 K)
Table 3 Kinetic parameters obtained from kinetic models for organic compounds onto modified lignite at 298.15 K

准一级动力学方程准二级动力学方程方程k1/min-1qe1,theory/(mg·g-1)R2方程k2/(g·mg-1·min-1)qe2/(mg·g-1)R2y=-0.0617x+3.1980.14224.490.941y=0.0339x+0.3520.00329.500.995
由表3可知:2种动力学模型的相关系数均在0.9以上,这表明吸附过程不是单一过程,而受物理过程和化学过程综合控制。而准二级动力学模型R2为0.995,大于准一级动力学方程的R2=0.941,这表明改性褐煤吸附喷漆废水有机物更符合准二级动力学模型,并且在整个吸附过程中,吸附速率受化学过程控制,即化学键合作用是制约整个吸附过程快慢的因素[21]。分析认为改性褐煤吸附喷漆废水有机物过程的机制为:1)改性褐煤基面与有机物之间的π-π色散作用力;2)改性褐煤表面的—COOH、—OH等官能团与废水有机物的氢键作用;3)官能团与有机物的成键作用。在这3个作用机制中,π-π色散作用、氢键作用机制优于化学成键机制,致使总体的吸附速率受化学反应控制。因此,改性褐煤吸附喷漆废水有机物是物理吸附和化学吸附共存的综合过程,吸附速率受化学反应速率控制。
3 结 论
1)改性褐煤吸附喷漆废水中的有机物可以在常温下自发进行,最优条件为ρ(COD)<350 mg/L,吸附体系处于酸性环境,吸附时间≥60 min,吸附剂投加量>10 g/L。
2)改性褐煤吸附喷漆废水中有机物的极限平衡吸附量与废水初始COD浓度有关,浓度越大,极限平衡吸附量越大,但增幅逐渐缩小,废水ρ(COD)为700 mg/L 时,平衡吸附量在40 mg/g以上。
3)改性褐煤吸附喷漆废水中有机物是一个物理吸附为主,化学吸附为辅的综合过程,吸附速率受化学反应速率控制。
[1] 谭雨清, 关晓辉, 刘海宁, 等. 混凝—氧化法处理喷漆废水的应用研究[J]. 工业水处理, 2006,26(10):75-77.
[2] 陈烨, 董菲菲, 陆骏, 等. 混凝芬顿法处理汽车涂装有机废水[J]. 材料保护, 2018,51(9):126-129.
[3] 张慧春, 闫爱军, 李俊文, 等. 混凝沉淀—化学氧化法处理喷漆废水[J]. 工业水处理, 2000,20(2):11-13.
[4] 雷艳, 钟声. 树脂吸附法处理癸二酸生产中含酚废水的研究[J]. 环境科学与技术, 2015,38(7):129-132.
[5] 许敏, 张林生. H103大孔树脂吸附苯酚性能研究[J]. 环境工程学报, 2011,5(8):1811-1814.
[6] Ge J C, Kim J Y, Yoon S K, et al. Fabrication of low-cost and high-performance coal fly ash nanofibrous membranes via electrospinning for the control of harmful substances[J]. Fuel, 2019,237:236-244.
[7] 周夏芝, 居殿春, 冯宁, 等. 改性小麦秸秆对苯酚的吸附性能研究[J]. 环境保护科学, 2018,44(4):57-60.
[8] 杨晓霞, 陈浩敏, 高晓明, 等. 活性炭吸附对硝基苯酚的动力学和热力学研究[J]. 离子交换与吸附, 2018,34(3):247-258.
[9] 毕晨阳, 郭会琴, 曾春城, 等. 油茶果壳活性炭对模拟燃油中二苯并噻吩的吸附[J]. 环境工程, 2018,36(4):103-107.
[10] 仝坤, 宋启辉, 刘国廷, 等. 褐煤活性焦吸附难降解有机废水研究进展[J]. 油气田环境保护, 2016,26(5):44-47.
[11] 赵东洋, 柴锦鹏. 褐煤腐殖酸对废水中活性翠兰KN-G的吸附实验[J]. 辽宁工程技术大学学报(自然科学版), 2013,32(12):1609-1612.
[12] 詹海鹃, 吴之强, 张腾飞, 等. 磺化太西煤吸附剂的制备及吸附性能研究[J]. 应用化工, 2017,46(6):1097-1102.
[13] 杨戊戌, 张洁, 姚雅雪, 等. 褐煤对苯酚的吸附性能及机制研究[J]. 安全与环境学报, 2017,17(1):215-219.
[14] 张志辉, 郑天龙, 王孝强, 等. 活性炭吸附处理锂电池厂含酯废水及微波再生实验[J]. 中国环境科学, 2014,34(3):644-649.
[15] 徐宏祥. 有机废水的煤吸附净化机理研究[D]. 北京:中国矿业大学(北京), 2015.
[16] Dastgheib S A, Karanfil T, Cheng W. Tailoring activated carbons for enhanced removal of natural organic matter from natural waters[J]. Carbon, 2004,42(3):547-557.
[17] 滕济林, 张萌, 李若征, 等. 褐煤活性炭吸附处理焦化废水[J]. 环境工程学报, 2011,5(1):117-120.
[18] Zhang B, Li F, Wu T, et al. Adsorption of p-nitrophenol from aqueous solutions using nanographite oxide[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2015,464(1):77-88.
[19] 刘明, 李金丽, 陈紫珊, 等. 不同条件下褐煤吸附印染废水的研究[J]. 煤炭技术, 2018,37(11):348-351.
[20] Goldberg S, Criscentib L J, Turnerc D R, et al. Adsorption-desorption processes in subsurface reactive transport modeling[J]. Vadose Zone Journal, 2007,6(3):407-435.
[21] 康亚璞, 刘国光, 李富华, 等. 花生壳、核桃壳吸附活性艳蓝动力学、热力学研究[J]. 环境工程, 2014,32(S1):31-33.
[22] Khan A A, Singh R P. Adsorption thermodynamics of carbofuran on Sn (Ⅳ) arsenosilicate in H+, Na+ and Ca2+ forms[J]. Colloids and Surfaces, 1987,24(1):33-42.