0 引 言
随着海产养殖业的兴起,抗生素在海产养殖过程中的使用量与日俱增。但是,部分养殖户盲目追求经济效益,在养殖过程中不科学地投加抗生素,导致了抗生素在养殖水体中大量残留,给养殖区域及附近水体造成严重污染。因此,如何有效去除养殖废水中的抗生素,已成为国内外研究的热点。现有的抗生素去除技术中,高级氧化技术最为有效,其中臭氧氧化技术以其工艺简单,对抗生素的去除率高而受到众多学者的关注。但是,由于臭氧氧化技术运行成本高、气液传质效率低、臭氧在水中稳定性差等客观问题[1],在海产养殖业推广的过程中受到一定限制。针对以上情况,催化臭氧氧化技术应运而生,其主要原理是利用具有强氧化性、低选择性、反应速度快[2]的羟基自由基(·OH)去除抗生素。由于催化剂的引入,单位时间内·OH产量更高,污染物的去除效率可得到大幅提高。基于以上原因,本文采用催化臭氧氧化技术去除海产养殖废水中的抗生素氟苯尼考(Florfenicol,FF)。文中对催化剂类型进行筛选,考察了臭氧浓度、催化剂用量等工艺条件对FF去除率的影响,同时探究了海水中CODMn和氨氮浓度对FF去除效果的影响。利用液相质谱-色谱(LC-MS)技术推断FF的降解途径,并通过生物毒性实验对经过Mn-CeOx/γ-Al2O3催化臭氧氧化处理后的废水生物毒性进行分析测定。
1 实验部分
1.1 实验药品
氟苯尼考分析标准品(色谱纯,阿拉丁生化科技有限公司),氟苯尼考(纯度为98%,阿拉丁生化科技有限公司),乙腈(色谱纯,阿拉丁生化科技有限公司),氢氧化钠(分析纯,天津市天力化学试剂有限公司),溴化钾(纯度为99%,天津市光复科技有限公司),盐酸萘乙二胺(分析纯,天津市大茂化学试剂厂),磺胺(纯度为99.5%,天津市大茂化学试剂厂),硝酸锰(纯度为50%,产自西陇化工有限公司),盐酸(分析纯,天津博迪化工有限公司),明亮发光杆菌T3小种冻干粉(购自中科院南京土壤研究所)。
1.2 实验装置及工艺流程
实验装置和工艺流程如图1所示,催化臭氧氧化塔总体积为1.2 L,有效体积为1.0 L,催化剂填充于承托层之上。实验所用催化剂为实验室以γ-Al2O3为载体采用浸渍法自行制备,活性组分分别为Mn-Ce、Co和Mn-Cu的金属氧化物。臭氧发生器为COM-AD系列臭氧发生器(氧气源),可以通过调节氧气流量和臭氧发生器的功率来调整臭氧浓度。纯氧通过二级减压阀进入臭氧发生器,通过使用一定频率的高压电流制造的高压电晕电场,激发产生臭氧和氧气的混合气体。通过二级减压阀以及气体流量进行流量调节,经反应塔底部钛合金曝气头微气泡化后进入反应塔内,与催化剂和水充分接触,发生催化臭氧氧化反应。反应后的尾气通入含有碘化钾的洗气瓶中,防止未利用的臭氧造成二次污染。

1—氧气源; 2—臭氧发生器; 3—反应器; 4—进水泵; 5—尾气吸收; 6—出水箱; 7—进水箱。
图1 催化臭氧氧化去除FF和工艺流程
Fig.1 Flowchart of the FF removal process by catalytic ozonation
1.3 实验用水
本实验用海水取自大连某海产养殖场,经过0.22 μm的水系滤膜(PES,津腾)过滤后待用,水质情况如表1所示。在反应前向水中添加25 mg/L的FF作为模拟养殖废水。
表1 模拟养殖废水主要水质指标
Table 1 Major indexes of the simulated marine aquaculture wastewater

水温/℃ρ(NH+4-N)/(mg·L-1)pHρ(CODMn)/(mg·L-1)20~210.2~0.87~7.240~42
1.4 分析方法
采用高效液相色谱法测定FF浓度,色谱条件如下[3]:色谱柱(Ultimate,LP-C18)的尺寸和填料粒度为4.62 mm×50 mm,5 μm,检测波长λ=224 nm,流动相:V(C2H3N)∶V(H2O)的配比为40%∶60%,流速为0.75 mL/min,柱温为35 ℃,进样量为20 μL,保留时间为5.5 min。氨氮浓度采用次溴酸盐氧化法测定(GB 1738.4—1998)。CODMn的测定参考水和废水监测分析方法(第四版)。臭氧的浓度采用碘量法(CJ/T 3028.2—94)测定。降解中间产物分析采用液相色谱-三重串联四极杆质谱联用仪,电喷雾电离源,负离子扫描模式进行分析。生物毒性分析采用明亮发光杆菌T3急性毒性实验(GB/T 15441—1995),用原子摩尔冷光检测仪测试明亮发光杆菌T3的发光强度。
1.5 实验步骤
将配好的海水养殖模拟废水加入进水箱中,开启进水阀,打开进水泵,使废水通入填充一定质量催化剂的反应器,待进水箱里的水全部进入反应器后,关闭进水阀和进水泵。打开氧气源,开启臭氧发生器,调节氧气流量和臭氧发生器的功率控制臭氧浓度。根据实验需求每间隔一定时间取样,所取样品经0.22 μm的水系滤膜过滤后分析测定FF浓度、氨氮、CODMn等指标。
2 实验结果与讨论
2.1 不同活性组分催化剂对FF去除的影响
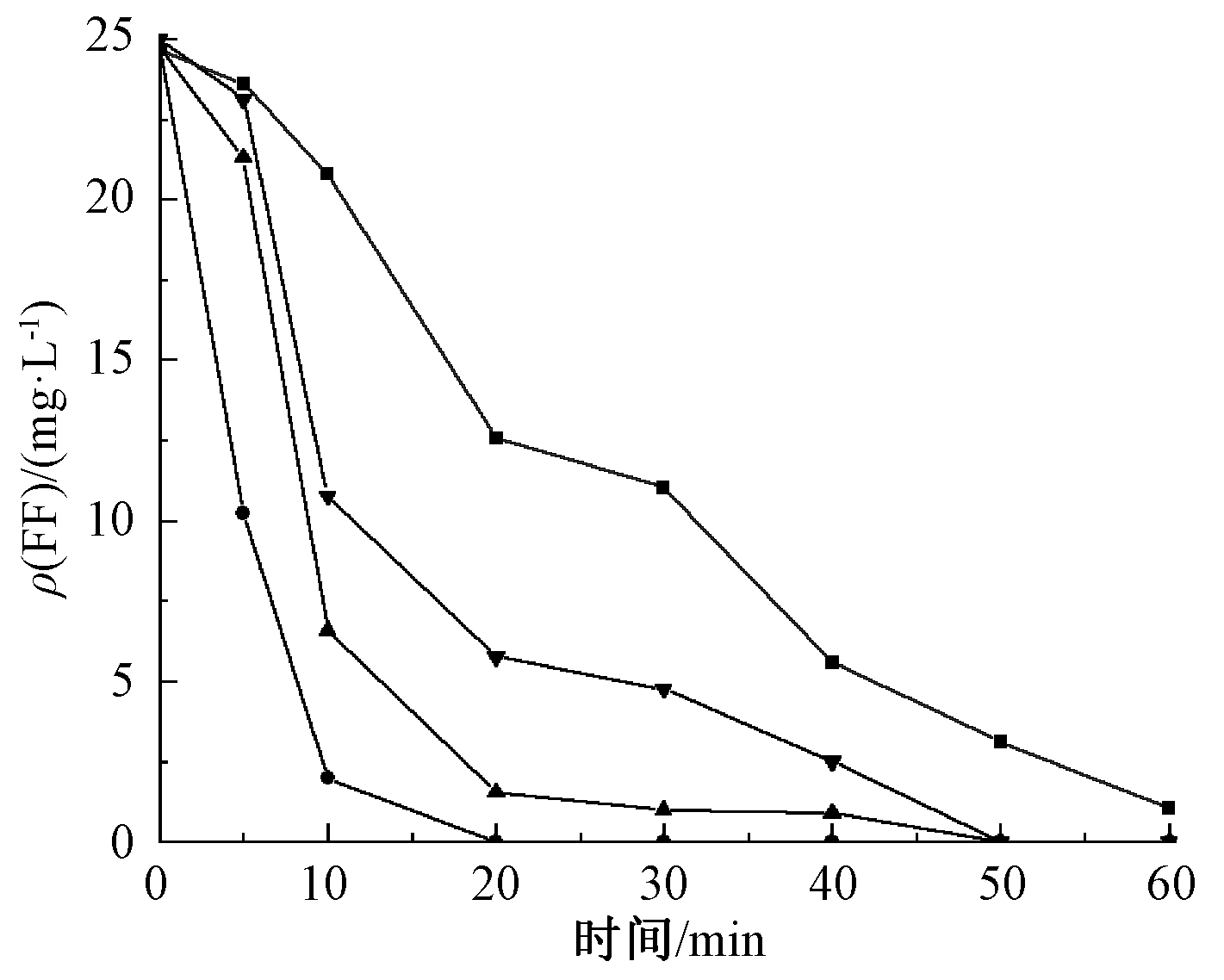
以Mn-CeOx/γ-Al2O3、Co3O4/γ-Al2O3和Mn-Cu/γ-Al2O3为催化剂进行FF的催化臭氧氧化实验,此外,以单独臭氧氧化试验作为对照组进行对比。实验条件如下:初始ρ(FF)为25 mg/L,臭氧浓度为12.86 mg/L,臭氧进气量为1.25 L/min,催化剂投加量为200 g。实验结果如图2所示。
![]() —O3;
—O3; ![]() —Mn-CeOx/γ-Al2O3+O3;
—Mn-CeOx/γ-Al2O3+O3; ![]() —Mn-Cu/γ-Al2O3+O3;
—Mn-Cu/γ-Al2O3+O3; ![]() —Co3O4/γ-Al2O3+O3。
—Co3O4/γ-Al2O3+O3。
图2 不同催化剂对FF的去除
Fig.2 Removal of FF by different catalysts
由图2可知:单独臭氧氧化和催化臭氧氧化(选用3种不同活性组分附载的催化剂)过程对FF均有去除作用。其中,Mn-CeOx/γ-Al2O3对FF的去除效果最好,20 min内几乎可将FF完全去除。这可能是因为锰、铈金属氧化物存在一定的协同作用[4],能产生更多四价态的锰和氧空穴,从而使得该催化剂具有更好的氧化活性。
催化臭氧氧化一般适用于一阶反应动力学定律,见式(1)[5],但对于降解有机物适用于混合型一阶反应动力学,见式(2)[6]:
C=C0exp(-kappt)
(1)
C=C01exp(-kapp1t)+C02exp(-kapp2t)
(2)
式中:C0、C01和C02分别为FF的初始浓度;kapp、kapp1、kapp2分别为一阶反应动力学、混合一阶反应动力学第一阶段、混合一阶反应动力学第二阶段3个反应的相对反应速率常数。
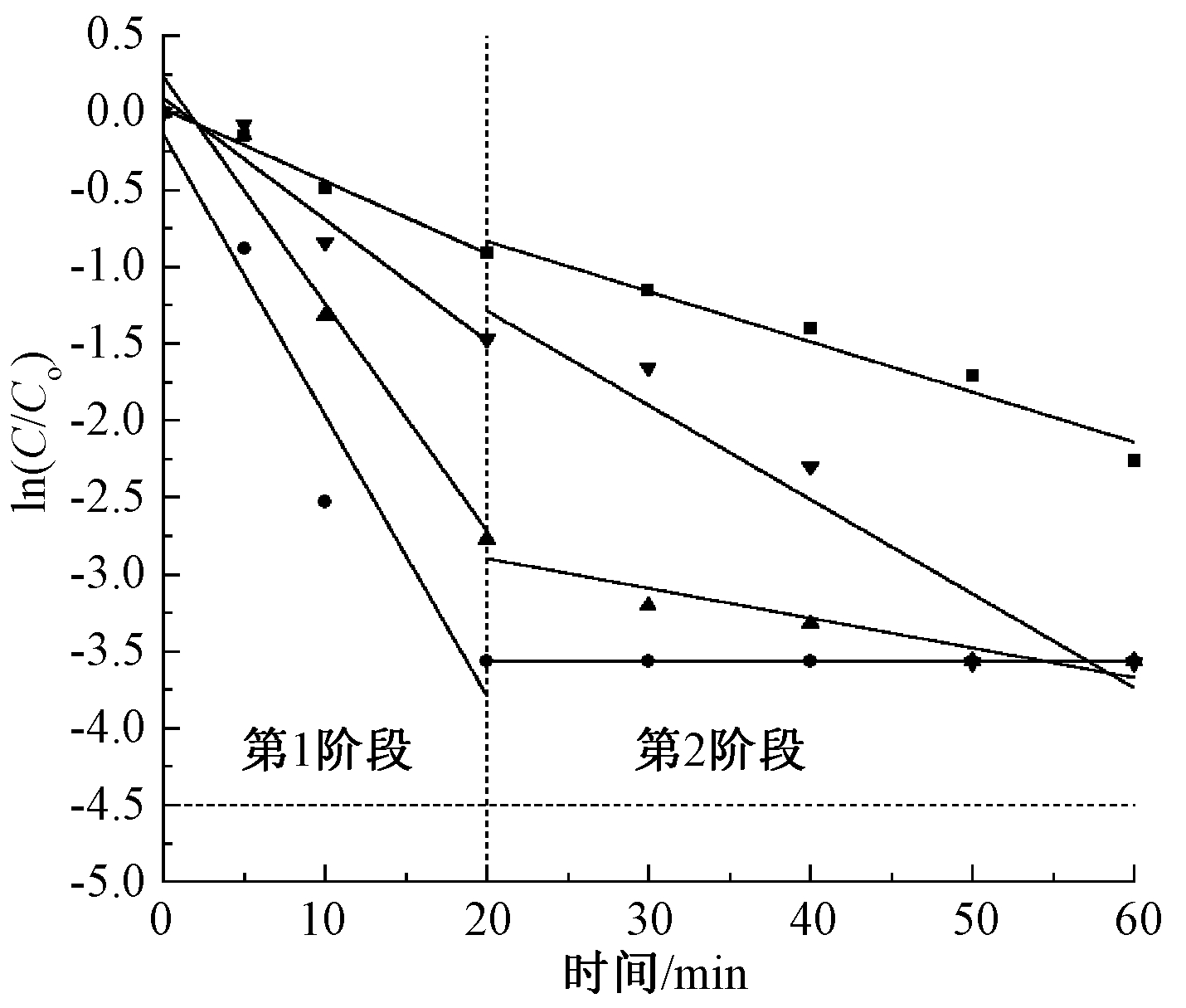
将单独臭氧氧化、Mn-CeOx/γ-Al2O3、Mn-Cu/γ-Al2O3、Co3O4/γ-Al2O3催化氧化降解FF的过程分别用式(1)、式(2)中的2种反应动力学模型进行拟合,结果如图3和表2所示。
![]() —O3;
—O3; ![]() —Mn-CeOx/γ-Al2O3+O3;
—Mn-CeOx/γ-Al2O3+O3; ![]() —Mn-Cu/γ-Al2O3+O3;
—Mn-Cu/γ-Al2O3+O3; ![]() —Co3O4/γ-Al2O3+O3。
—Co3O4/γ-Al2O3+O3。
图3 不同催化剂对FF的动力学拟合
Fig.3 Dynamic fitting of FF degradation with different catalysts
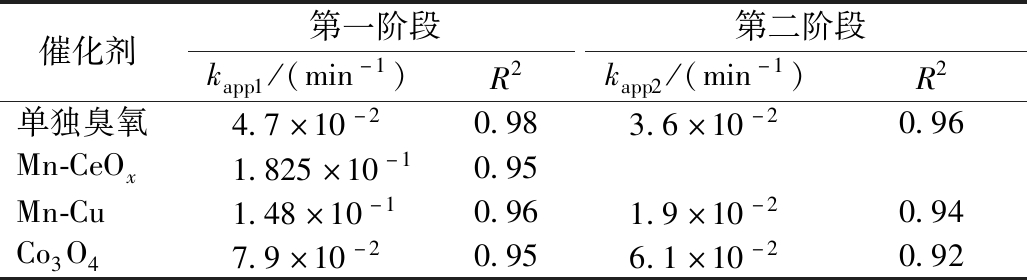
由图3可知:FF的催化臭氧氧化降解过程更符合混合型一阶反应动力学。由表2可看出:相对其他几种催化剂,Mn-CeOx/γ-Al2O3体系具有更高的反应速率,即FF去除得更快。另外,表2中二阶反应速率常数均低于一阶反应速率常数。这是由于在反应初始阶段,FF浓度较大且中间产物较少,超氧自由基和·OH与FF的碰撞概率较大,反应速度较快,随着FF中间产物的增加,20~60 min时反应速率降低。因此,实验确定选择Mn-CeOx/γ-Al2O3为催化剂进行催化臭氧氧化降解FF。
表2 不同活性组分催化剂降解FF的混合
一阶反应动力常数
Table 2 Mixed first order dynamic constants of FF degradation by different catalysts
催化剂第一阶段第二阶段kapp1/(min-1)R2kapp2/(min-1)R2单独臭氧4.7×10-20.983.6×10-20.96Mn-CeOx1.825×10-10.95Mn-Cu1.48×10-10.961.9×10-20.94Co3O47.9×10-20.956.1×10-20.92
2.2 不同臭氧浓度对催化臭氧氧化去除FF的影响
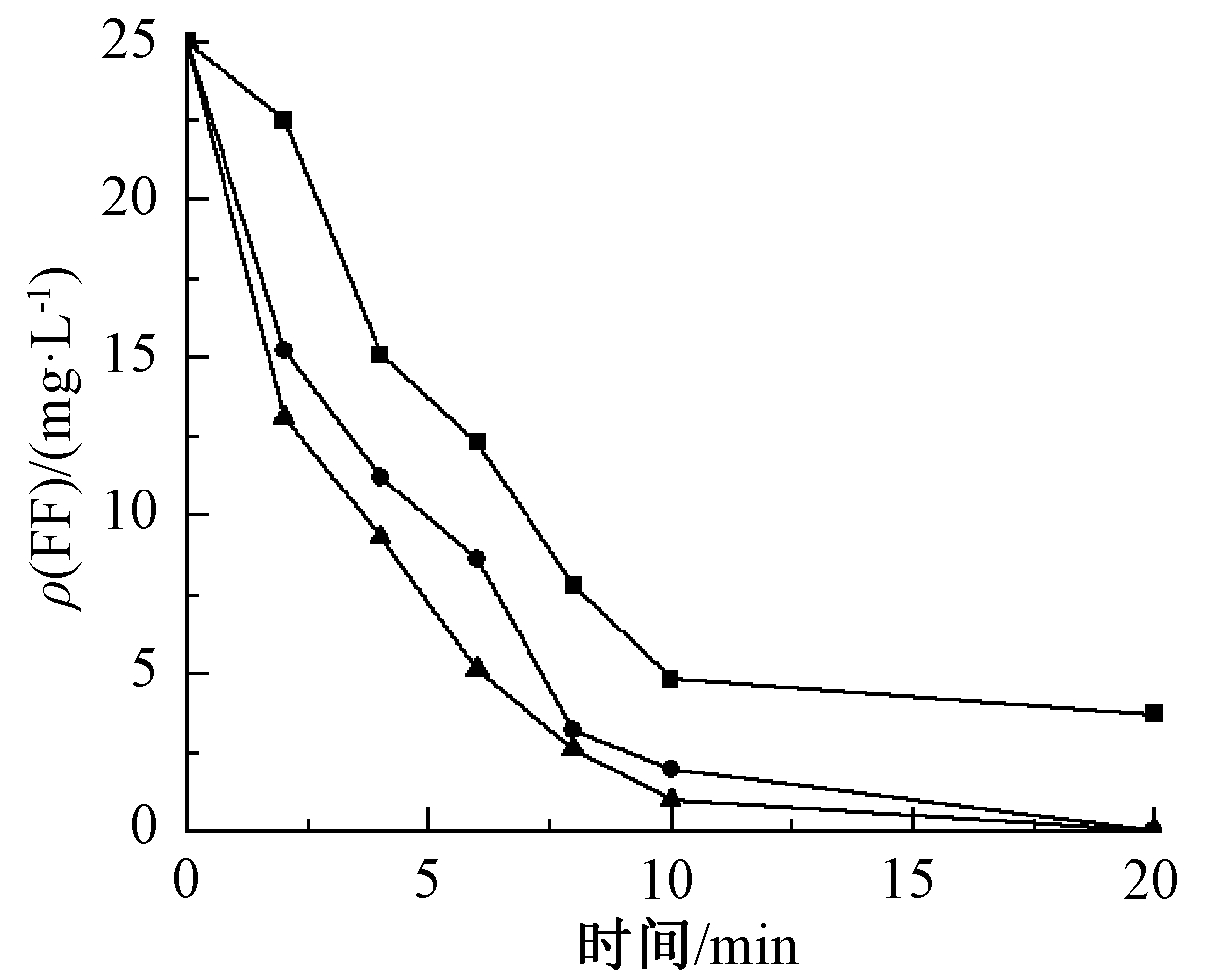
保持进气量1.25 L/min不变,通过调节臭氧发生器功率控制臭氧浓度分别为7.68,12.86,19.2 mg/L,以探究不同臭氧浓度对催化臭氧氧化降解FF效果的影响,结果如图4所示。
![]() —7.68 mg/L;
—7.68 mg/L; ![]() —12.86 mg/L;
—12.86 mg/L; ![]() —19.2 mg/L。
—19.2 mg/L。
图4 不同臭氧浓度对FF去除的影响
Fig.4 Effect of ozone concentration on removal of FF
由图4可知:FF去除率随着臭氧浓度增加而增加,当臭氧浓度为19.2 mg/L,反应10 min,FF去除率可接近100%。这是因为催化臭氧氧化反应为液相反应,臭氧在液相中的气液传质过程是催化臭氧氧化的控制步骤。随着水中臭氧浓度增加,臭氧在气液界面的推动力逐渐增大,传质速度加快,更有利于臭氧与催化剂表面充分接触,因此·OH和超氧自由基产量增大,FF去除率得到提高。
2.3 催化剂投加量对催化臭氧氧化去除FF速率的影响
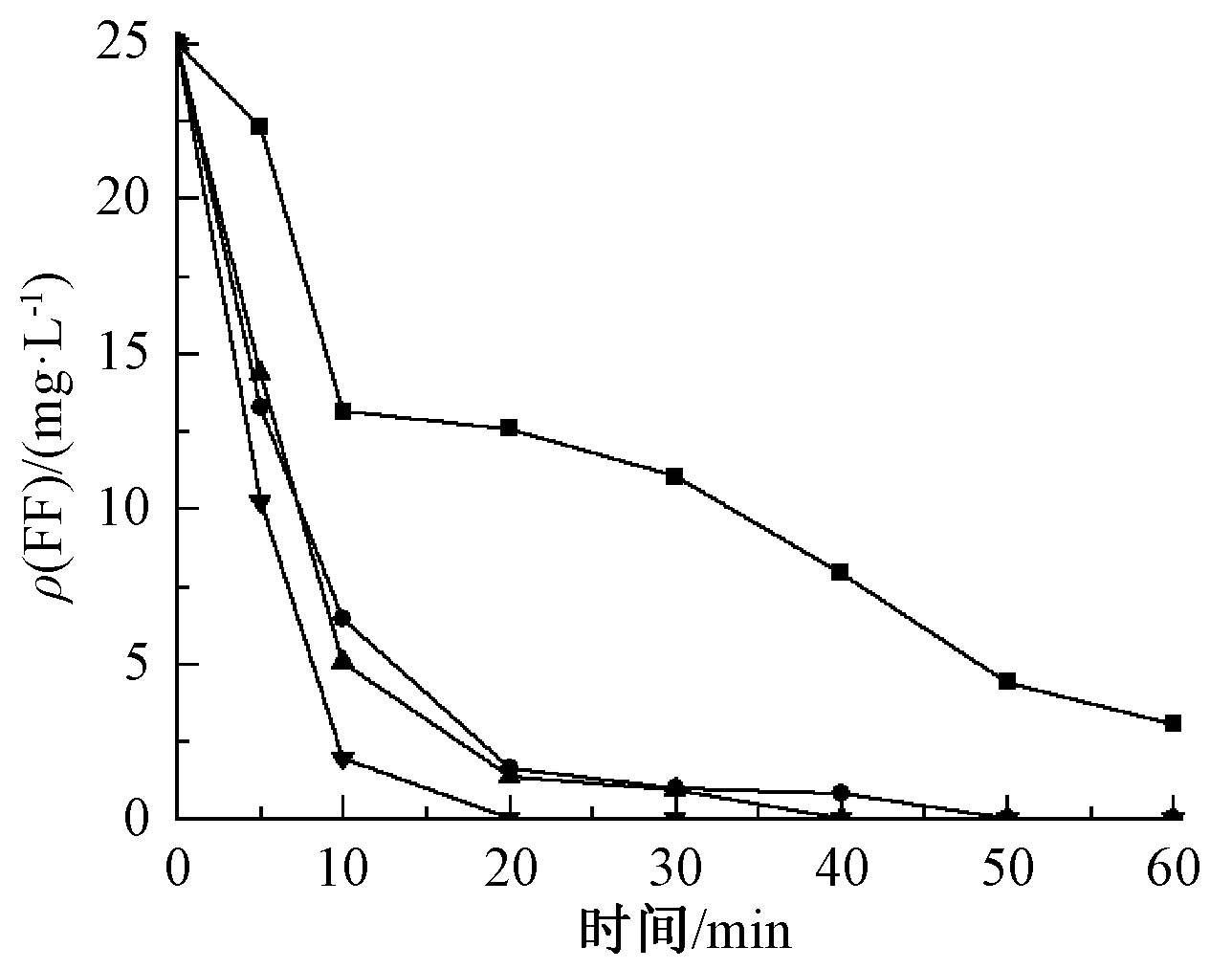
催化剂的加入有利于提高臭氧的利用率,促进臭氧分解产生更多的·OH。分别加入0,50,100,200 g催化剂,以考察不同催化剂投加量对FF降解速率的影响,结果如图5所示。
![]() —0 g;
—0 g;![]() —50 g;
—50 g;![]() —100 g;
—100 g;![]() —200 g。
—200 g。
图5 不同催化剂投加量对FF去除的影响
Fig.5 Effect of catalyst dosage on removal of FF
由图5可知:未添加催化剂时,单独臭氧氧化对FF去除效果不佳,10 min时FF仅能去除48%。当加入催化剂时,FF去除率显著提升。当加入催化剂质量为200 g时,FF在10 min时的去除率便可达到92%。这可能是因为催化剂投加量增加,有更多活性位点催化产生·OH,以提高FF的去除效率。
2.4 氨氮浓度对FF去除率的影响
在海产养殖中,由于饵料无法充分利用和生物生长中产生的排泄物难以及时清除,将导致氨氮浓度升高,对生物产生毒害作用[7]。本实验通过向废水中添加1,3,5 mg/L氨氮(用NH4Cl配置)以探究不同氨氮浓度对反应体系的影响,实验结果如图6和图7所示。

![]() —原废水;
—原废水; ![]() —1 mg/L;
—1 mg/L; ![]() —3 mg/L;
—3 mg/L; ![]() —5 mg/L。
—5 mg/L。
图6 不同氨氮浓度对FF去除的影响
Fig.6 Effect of ammonia concentration on removal of FF
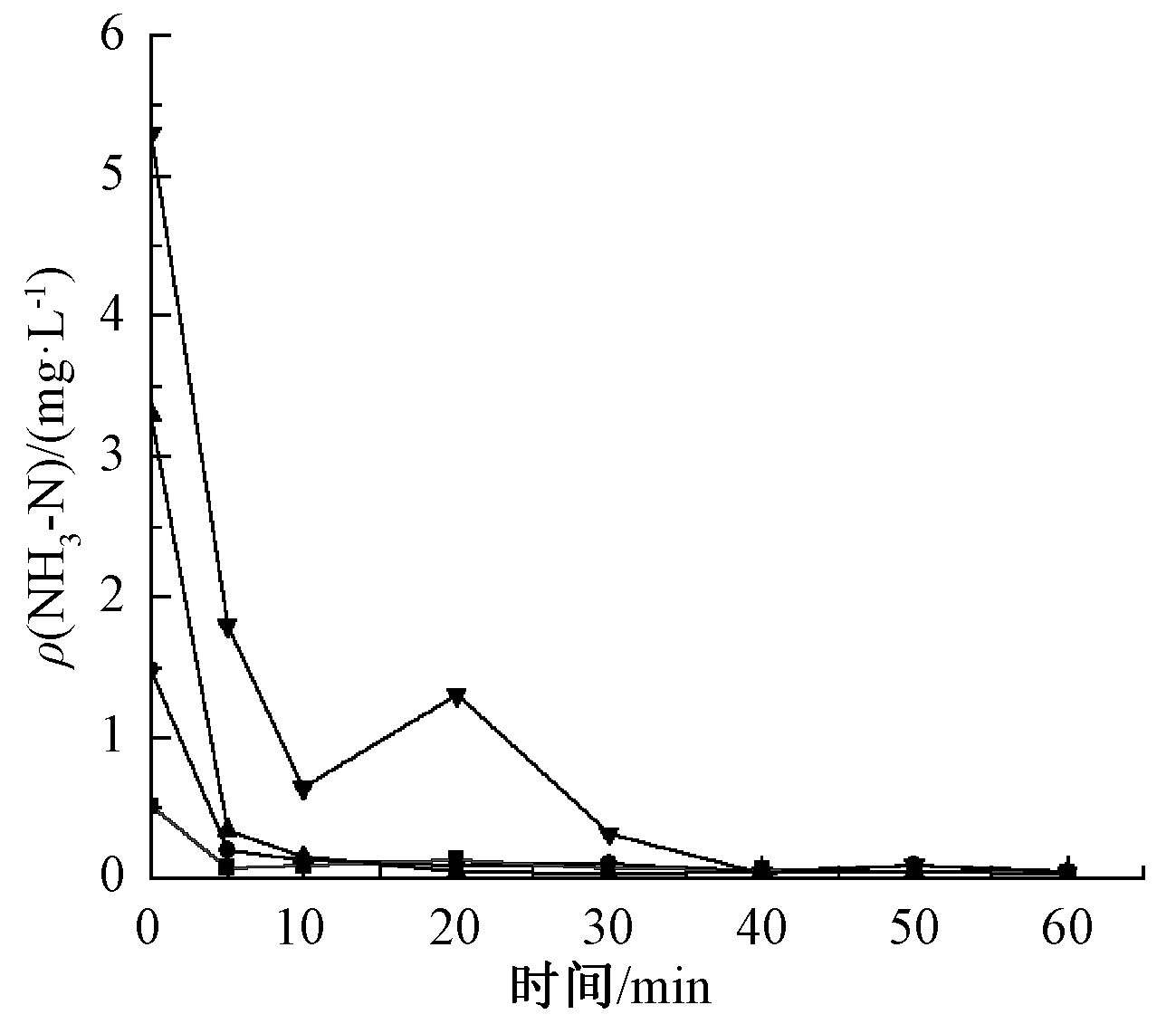
![]() —原废水;
—原废水; ![]() —1 mg/L;
—1 mg/L; ![]() —3 mg/L;
—3 mg/L; ![]() —5 mg/L。
—5 mg/L。
图7 不同初始浓度氨氮的去除效果
Fig.7 Ammonia removal with different initial concentration
由图6可知:未添加氨氮时,FF去除率最高,20 min 内FF去除率接近100%,随着氨氮浓度增加FF的去除率明显下降。这表明在催化臭氧氧化过程中,氨氮和FF的去除存在一定竞争关系。
由图7可知:不同初始浓度氨氮在10 min内均可除去90%以上。这可能是因为海水中平均ρ(Br-)为66 mg/L[8],·OH氧化Br-的速率很高[9],臭氧和·OH会与海水中Br-生成HOBr/BrO-并与NH3产生反应生成NBr3[10]从而去除氨氮,反应式如下[10]:
1)O3+Br-→BrO-+O2
2)2·OH+Br-→BrO-+H2O
3)2O3+BrO-→BrO3-+2O2
4)HOBr+NH3→NH2Br+H2O
5)HOBr+NH2Br→NHBr2+H2O
6)HOBr+NHBr2→NBr3+H2O
7)H2O+NHBr2+NBr→2HOBr+3H++3Br-
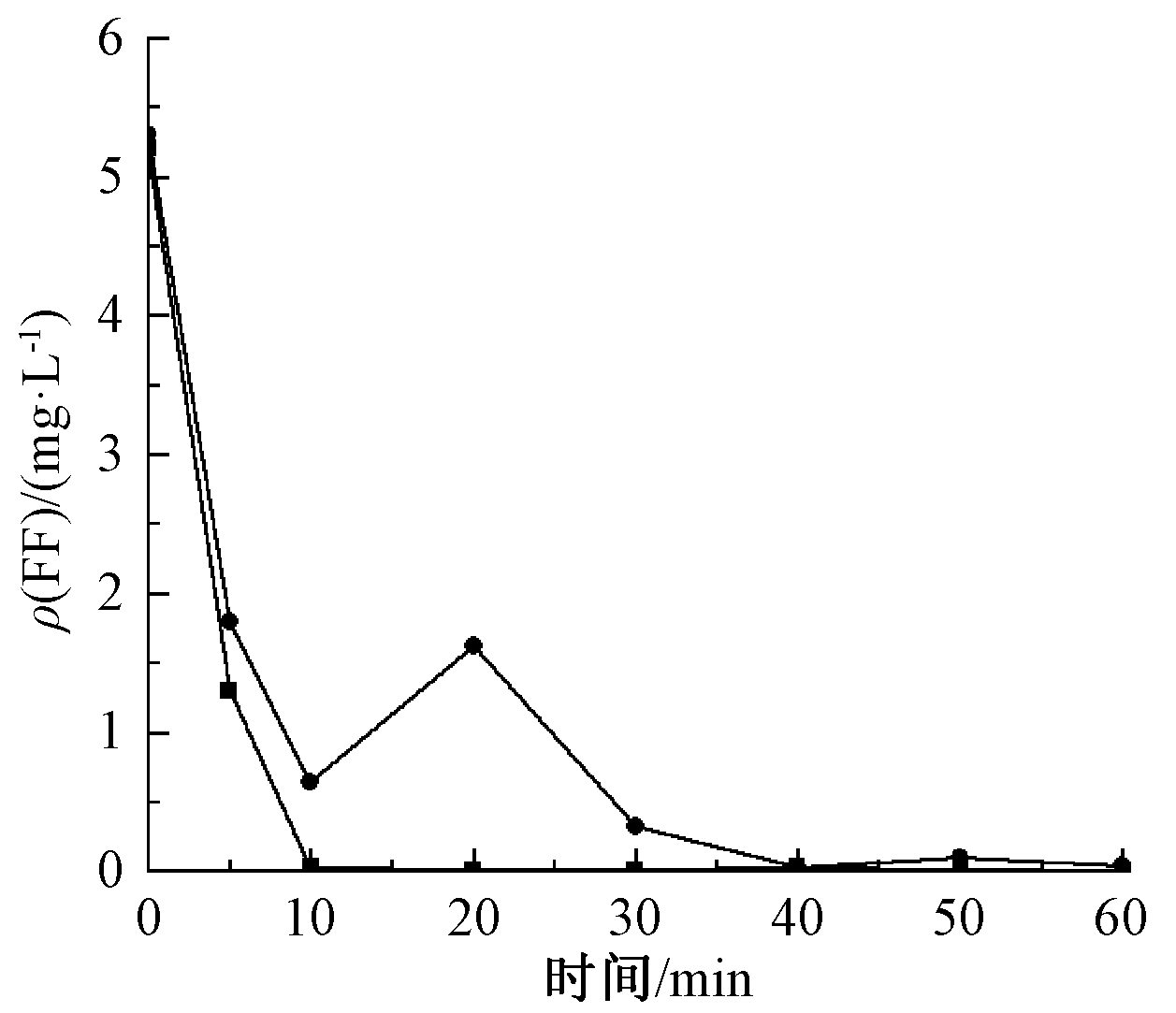
图7表明,添加5 mg/L氨氮时,反应20 min,出现了氨氮升高的现象。为揭示此原因,对未添加FF的氨氮进行催化臭氧降解,结果如图8所示。可以推断出,氨氮的升高是由于FF在降解过程中C—N断开,生成氨氮所致。
![]() —5 mg/L NH3-N;
—5 mg/L NH3-N; ![]() —5 mg/L NH3-N+FF。
—5 mg/L NH3-N+FF。
图8 FF添加对氨氮去除的影响
Fig.8 Effect of FF addition on removal of ammonia nitrogen
2.5 CODMn浓度对Mn-CeOx/γ-Al2O3催化臭氧氧化去除FF速率的影响
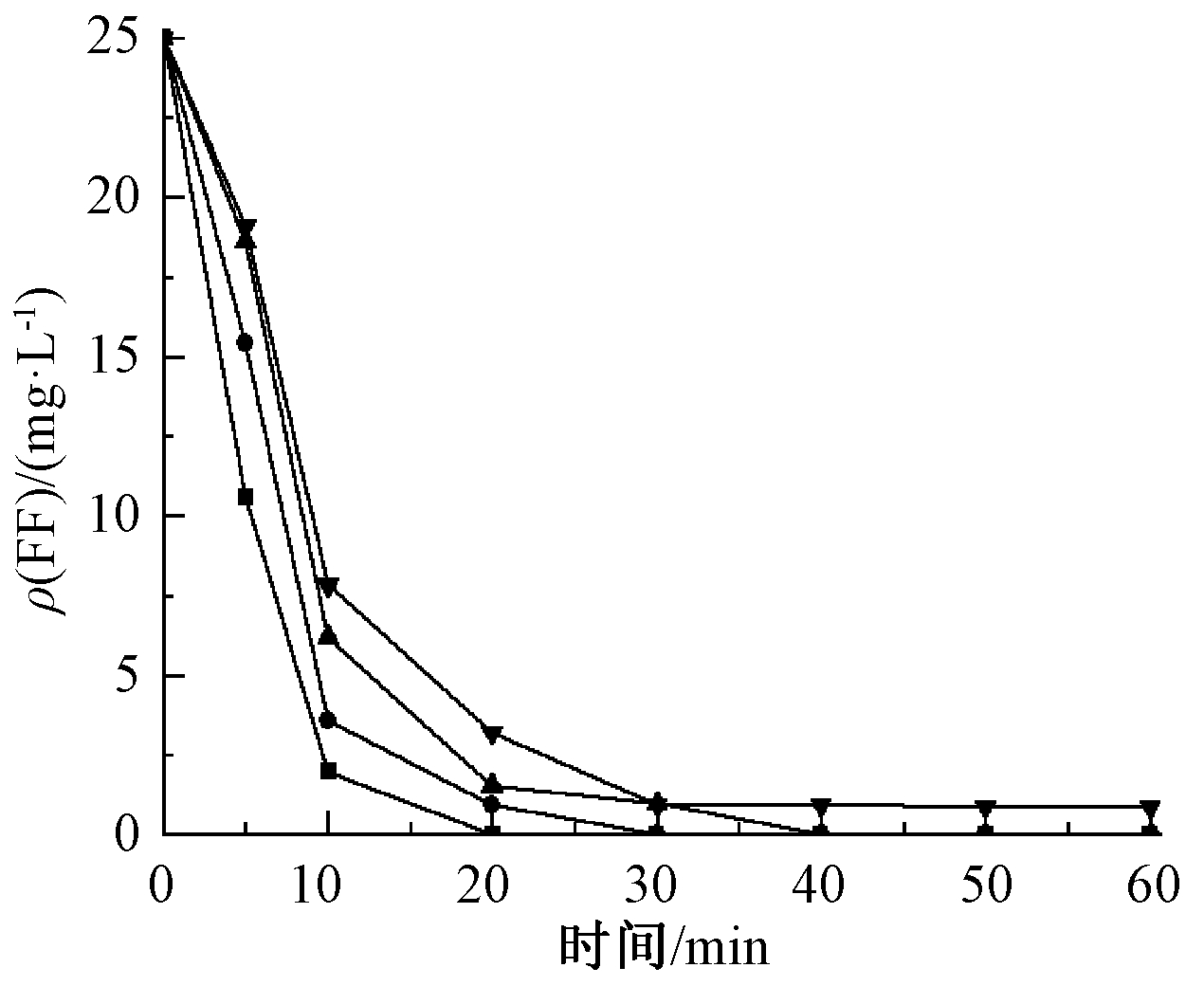
CODMn浓度波动可以体现出养殖水体水质的变化。本实验通过向海水中分别添10,30,50 mg/L的CODMn(采用邻苯二甲酸氢钾配制,25 mg/L FF相当于40 mg/L CODMn),以考察不同浓度CODMn对FF去除率的影响,实验结果如图9和图10所示。
![]() —原废水;
—原废水; ![]() —10 mg/L;
—10 mg/L; ![]() —30 mg/L;
—30 mg/L; ![]() —50 mg/L。
—50 mg/L。
图9 不同浓度CODMn对FF去除的影响
Fig.9 Effect of CODMn concentration on removal of FF
![]() —原废水;
—原废水; ![]() —10 mg/L;
—10 mg/L; ![]() —30 mg/L;
—30 mg/L; ![]() —50 mg/L。
—50 mg/L。
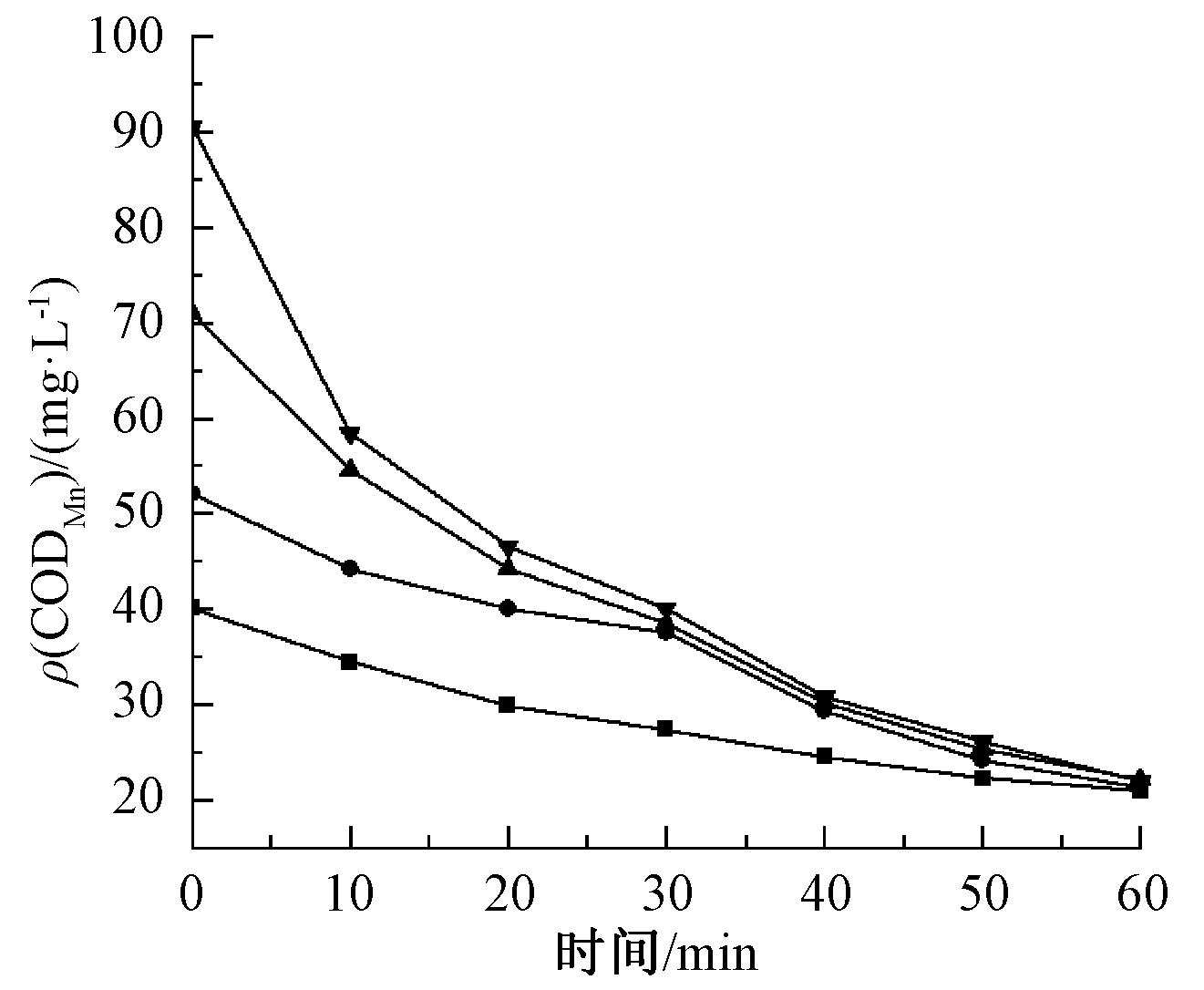
图10 不同初始浓度CODMn的去除效果
Fig.10 Removal CODMn with different initial concentration
由图9可知:CODMn浓度增加会降低Mn-CeOx/γ-Al2O3催化臭氧氧化去除FF速率。未添加CODMn时,FF去除速率最快,反应20 min时,FF去除率可达到100%。当添加ρ(CODMn)为50 mg/L时,反应20 min,FF去除率仅为80%。这可能是因为外加有机物和FF存在竞争使得单位体积内·OH与FF的碰撞概率下降,造成对FF去除率的下降。
由图10可知:未添加CODMn的海水体系ρ(CODMn)约为40 mg/L,在反应20 min时,仅去除了10 mg/L,随着反应时间的进一步延长,CODMn持续下降,反应60 min时,ρ(CODMn)仍为20 mg/L。这可能是由于催化臭氧氧化FF的过程中,FF未实现完全矿化,其首先发生断链反应,生成中间产物,对CODMn仍有贡献。
2.6 降解机理分析
运用LC-MS技术在电喷雾电离源,负离子扫描模式下对FF在体系中的降解中间产物进行分析,结果如表3所示。结合LC-MS产物结果分析,对FF在Mn-CeOx/γ-Al2O3催化臭氧氧化作用下的可能降解途径进行推断,如图11所示。
表3 FF降解过程中主要中间产物
Table 3 Main intermediate products in FF degradation

化合物m/z化学结构115521693171417251836199720283409372
由图11 FF在体系中的降解路径分析可知:臭氧在Mn-CeOx/γ-Al2O3催化作用下产生的大量·OH与FF进行反应,可能的降解路径如下:1)·OH首先与苯环反应,形成新的产物9[11],后由自由基引发裂解,产生新酚类物质3;2)发生加氢反应生成新的氢加成物8,之后在·OH氧化和加成作用下形成酰基类有机物 6;3)一部分FF在自由基作用下在苯环上裂解,脱掉有机氟和有机氯,形成带有醛基的有机物。产物4、7受到·OH攻击,C—N键等破坏,产生无机离子如![]() 等[11-12],前面实验中氨氮含量的升高验证了这一过程的发生,最后,
等[11-12],前面实验中氨氮含量的升高验证了这一过程的发生,最后,![]() 被进一步氧化为
被进一步氧化为![]() 并逐渐被矿化为CO2和H2O。
并逐渐被矿化为CO2和H2O。
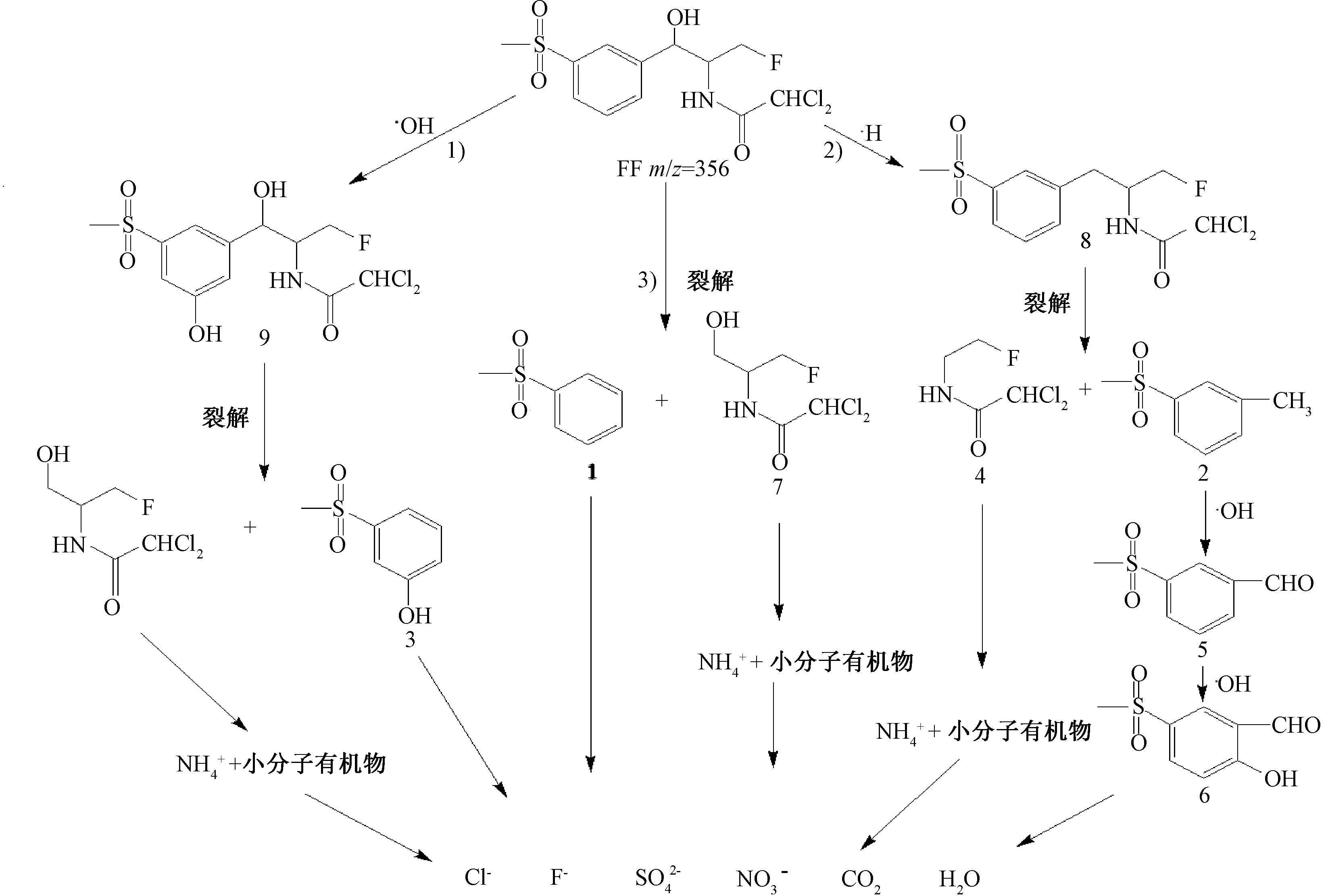
图11 FF的降解途径
Fig.11 Degradation pathway of FF
2.7 明亮发光杆菌急性毒性实验
由于FF在催化臭氧氧化过程中并未实现完全矿化,而是部分转化为某些中间产物,因此,有必要评价FF在催化臭氧氧化降解过程中生成的中间产物的毒性,实验结果如图12所示。
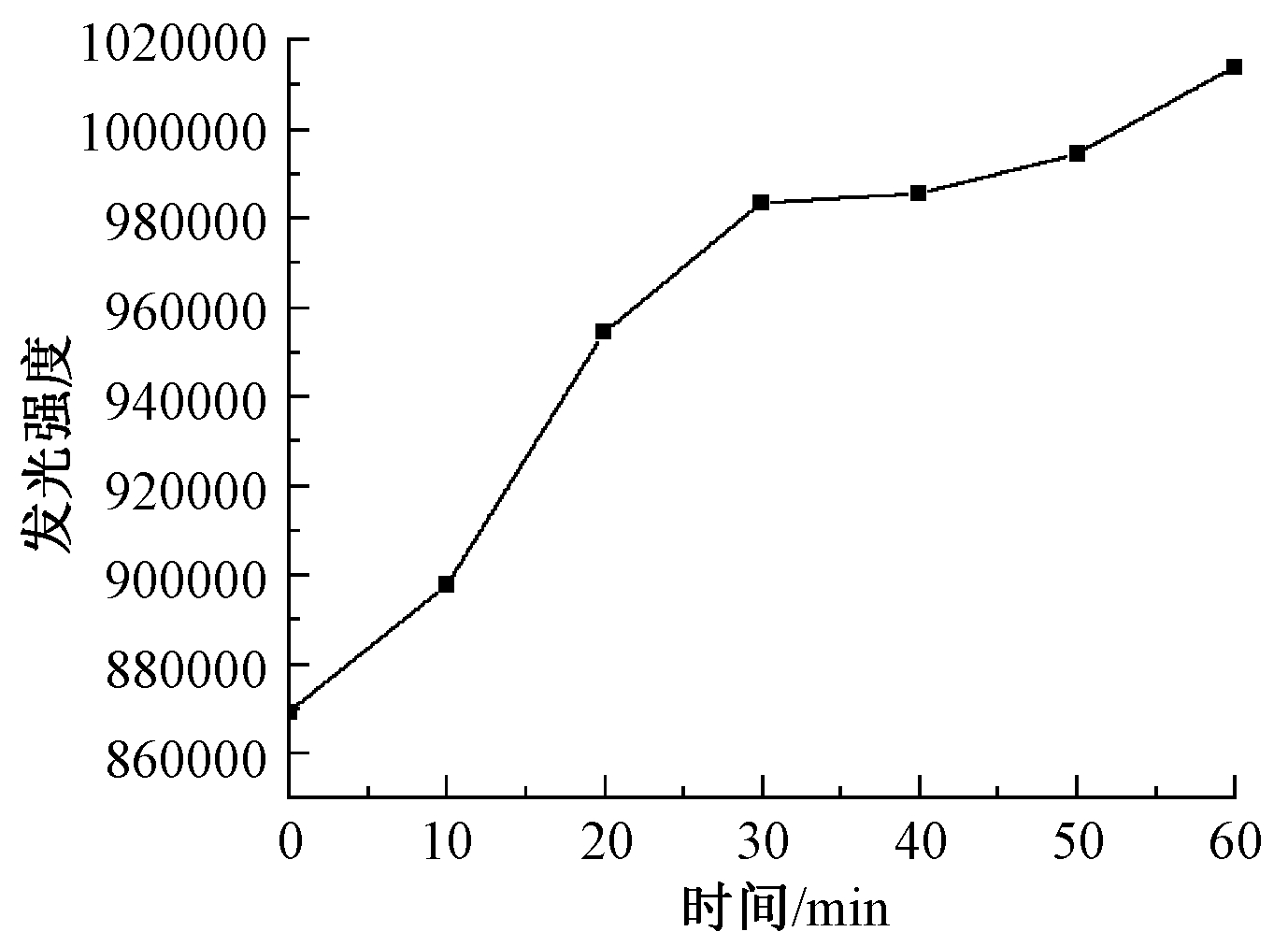
图12 明亮发光杆菌发光强度在体系中的变化
Fig.12 Variation of luminous intensity of luminescent bacilli in the reaction system
由图12可知:经过60 min催化臭氧氧化降解后,明亮发光杆菌的发光强度相比初始上升约16%。这表明经过处理后的废水水质更适宜明亮发光杆菌的生存,降解反应后的废水毒性明显有所降低,即经过催化臭氧氧化处理后的水更适合生物生长。这可能是由于FF结构中的有机氯和有机氟得到脱除,使得生物毒性下降[13]。
3 结 论
1)Mn-CeOx/γ-Al2O3作为催化剂更适合于催化臭氧氧化去除模拟海产养殖废水中的FF。
2)Mn-CeOx/γ-Al2O3催化体系中臭氧浓度为12.86 mg/L,催化剂投加量为200 g,ρ(FF)为25 mg/L,反应20 min时,FF去除率接近100%。
3)Mn-CeOx/γ-Al2O3催化臭氧氧化体系中,增加催化剂投加量或者提高臭氧浓度,均可提高FF去除率。
4)Mn-CeOx/γ-Al2O3催化臭氧氧化体系中,氨氮和CODMn浓度增加均会降低FF的去除率。
5)FF的降解机理为·OH攻击FF使其转化为酰基有机物或是醛类有机物,之后逐步被分解成小分子有机物和氨氮,最后,![]() 被进一步氧化为
被进一步氧化为![]() 小分子有机物逐步矿化为CO2和H2O。
小分子有机物逐步矿化为CO2和H2O。
6)明亮发光杆菌T3毒性实验结果表明,经过Mn-CeOx/γ-Al2O3催化臭氧氧化去除FF后的模拟海产养殖废水,生物毒性降低,更适合生物生存。
[1] 孙子为, 归谈纯, 高乃云, 等. 高级氧化技术降解水体中抗生素的研究进展[J]. 四川环境, 2014, 33(5): 146-153.
[2] 刘祖庆, 魏晓波, 王德喜. 臭氧高级氧化污水处理技术综述[J]. 广州化工, 2018, 46(17): 14-16.
[3] 田丽粉. 氟苯尼考在牙鲆体内的药代动力学及残留消除规律研究[D]. 青岛: 中国海洋大学, 2009.
[4] Liao Y N,He L F,Chen L M,et al. Catalytic oxidation of toluene over nanorod-structured Mn-Ce mixed oxides[J]. Catalysis Today, 2013,216(6):220-228.
[5] Qi F, Xu B B, Chen Z L, et al. Mechanism investigation of catalyzed ozonation of 2-methylisoborneol in drinking water over aluminum (hydroxyl) oxides: role of surface hydroxyl group[J]. Chemical Engineering Journal, 2010, 165(2):490-499.
[6] Faï, Larachi A, Pierre M, et al. Ce 3d XPS study of composite CexMn1-xO2-y wet oxidation catalysts[J]. Applied Surface Science, 2002, 195(1/2/3/4):236-250.
[7] 胡江伟.无公害养殖池塘水质调控关键技术[J]. 科学养鱼, 2018(4): 82-83.
[8] 王雲. 可逆气态膜过程用于浓海水提溴和废水脱氨[D].天津: 天津大学, 2016.
[9] 何茹, 鲁金凤, 马军, 等. 臭氧催化氧化控制溴酸盐生成效能与机理[J].环境科学, 2008,29(1): 99-103.
[10] Tanaka J. Application of ozone treatment for ammonia removal in spent brine[J]. Advances in Environmental Research, 2003, 7(4):835-845.
[11] Zhang Y, Li J H, Zhou L, et al. Aqueous photodegradation of antibiotic florfenicol: kinetics and degradation pathway studies[J]. Environmental Science and Pollution Research, 2016,23(7):6982-6989.
[12] 张佳琪, 李启龙, 何义亮, 等.光催化-膜分离耦合工艺处理水溶液中氟苯尼考的研究[J].环境工程,2017,35(12): 51-56.
[13] Liu N, Sijak S, Zheng M, et al. Aquatic photolysis of florfenicol and thiamphenicol under direct UV irradiation, UV/H2O2 and UV/Fe(Ⅱ) processes[J].Chemical Engineering Journal, 2015, 260:826-834.