0 引 言
化工废气和室内空气中含有大量甲苯,以甲苯为主要成分的VOCs排放到大气中会与NOx发生光化学反应,且在过程中生成O3等二次污染物,严重影响空气质量[1-3]。传统的VOCs治理技术,如生物法、燃烧法、吸附法由于高能耗和技术适用问题不适用于低浓度VOCs的治理[4-5]。低温等离子体是在常温常压下通过施加高压电场使气体电离成高能电子和活性物质,与气体发生非弹性碰撞,形成活性粒子降解甲苯等污染物,具有反应速度快、能耗低、适用范围广等特点[6-7]。由于以空气为背景气体时会产生中间产物,现有研究多以N2或O2为背景气体进行实验研究,限制了低温等离子体技术的实际应用[8-9]。将低温等离子体结合催化技术降解VOCs,是利用放电等离子体阶段产生的高能电子和活性物质触发催化剂在较低温度下起到催化作用,这样不仅提高了VOCs的降解效率,同时促进NOx及二次污染物的降解[10-11]。Guo等[3]研究发现,在空气中以较低能量的等离子体降解甲苯时,有大量的中间产物产生,当能量提高到17.4 W时中间产物完全转化为CO2和H2O。Bo等[12]在采用等离子体降解甲苯时增加Mn3O4催化剂,对甲苯降解率从58.1%增加到87.2%,且很好地抑制了NO2产生。早期研究发现在Al2O3上负载MnOx可将O3分解成活性氧原子,在较低温度氧化VOCs[13]。低温等离子体技术不仅可以用来降解甲苯等VOCs,而且在抑制NOx方面也具有一定应用。 Yu等[14]研究发现,在不同背景气体下,等离子体对NO去除的效果不同,以N2为背景气体时对NO抑制作用最佳。此外,Rezaei等[15]通过实验研究表明,乙酸锰和硝酸锰2种前驱物制备的催化剂对甲苯的氧化能力和对O3的分解能力不同,与硝酸锰制备的催化剂相比乙酸锰制备的催化剂表面的Mn催化点位分散性较高,有利于甲苯的降解及O3分解。
本实验中采用双层介质阻挡放电(double dielectric barrier discharge,DDBD)反应器结合MnOx催化反应器形成二段式催化氧化系统。探究不同特定输入能量(SIE)、不同前驱物对甲苯和NOx降解的影响,并在最佳条件下探究O3和COx产生情况。
1 实验部分
1.1 催化剂制备
实验中分别以硫酸锰和乙酸锰为前驱物,以Al2O3为载体制备MnOx(MS)和MnOx(MA)2种催化剂,负载量为15%,制备方法为浸渍法:即将Al2O3在乙酸锰或硫酸锰溶液中浸渍24 h,后烘干6 h,得到的材料以7.5 ℃/min程序升温至450 ℃保持3 h。
1.2 催化剂表征
采用SEM(S-3400 N,日立,日本),FT-IR(IR-Prestige-21,岛津,日本)观察前驱物对催化剂表观形貌、化学键的影响。
1.3 实验装置
实验系统分为4个模块:配气模块、催化氧化模块、供电模块和分析模块,如图1所示。
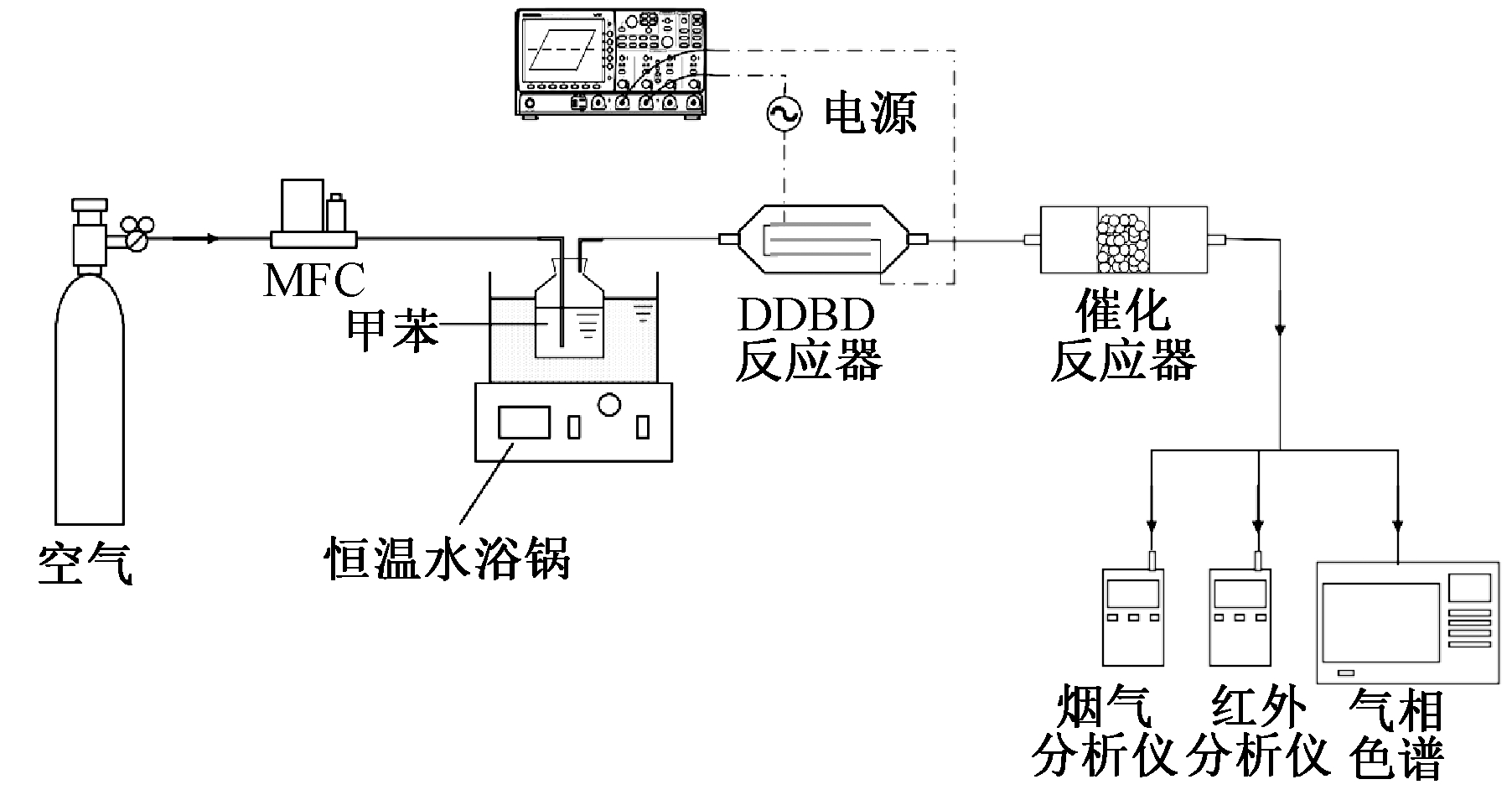
图1 实验流程
Fig.1 Schematic diagram of the experimental facility
1)配气模块由空气钢瓶、气体发生器及质量流量计组成。在控制质量流量计为500 mL/min,温度为15 ℃时,模拟甲苯气体浓度为206 μg/m3。
2)催化氧化模块由DDBD和催化反应器串联组成。DDBD的放电电极为130 mm×130 mm×1 mm的不锈钢板,放电间隙为1.5 mm,如图2所示。催化反应器由内径为15 mm,壁厚为8 mm,长度为240 mm的有机玻璃制成。内置直径为3~5 mm的MnOx/Al2O3催化剂(BET=389 m2/g)。
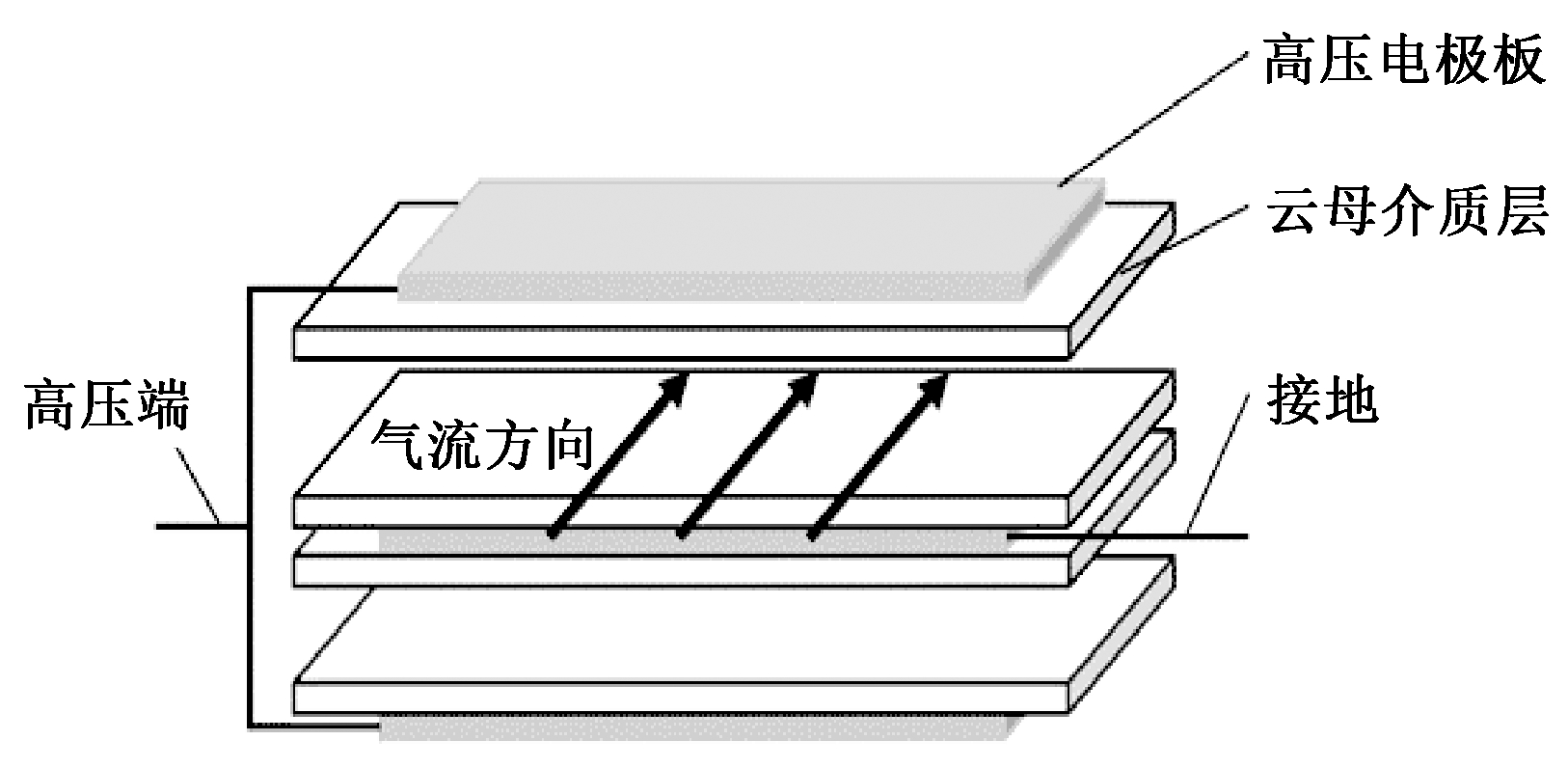
图2 DDBD反应器示意
Fig.2 Schematic view of the DDBD reactor
3)供电模块由高压电源(CTP-2000K,南京苏曼科技有限公司,中国),示波器(TDS2000C,Tektronix,美国)及电压探头(P6139B,Tektronix,美国)组成。
4)分析模块由气相色谱仪(7890A,Agilent,美国),烟气分析仪(905,Kane,英国),红外气体分析仪(GHX-3010H,华云分析仪器,中国),O3检测仪(GM-6000-0EM,Anseros,德国)组成,用于检测甲苯、NOx、COx和O3浓度。
1.4 计算公式
特定输入能量SIE公式为:
![]()
(1)
式中:P为电源输入能量,J;Q为气体流量,mL/min。
甲苯去除率η公式为:
(2)
式中:C0为DDBD进口甲苯浓度,μg/m3;C为系统出口甲苯浓度,μg/m3。
CO2选择率SCO2公式为:
(3)
式中:CCO2为系统出口CO2浓度,μg/m3。
2 结果与分析
2.1 催化剂表征结果
图3a、b分别为MnOx(MA)、MnOx(MS)的SEM结果。可知:负载量为15%的MnOx(MA),MnOx(MS)都具有较大的孔径或腔体。多孔结构的分布有利于催化活性的表达和气态产物的扩散。同时,MnOx(MA)、MnOx(MS)的EDS结果分别为13.31%和10.58%。实验结果均小于理论值,是实验过程中的Mn元素损耗导致。

图3 SEM和FT-IR表征结果
Fig.3 The results of SEM and FT-IR characterization
此外,图3c为MnOx(MA)、MnOx(MS)傅里叶变换红外结果。可知:在3444 cm-1和1644 cm-1处出现的峰,可归因于H2O和OH基团的弯曲振动,有文献指出OH基团是一些VOCs的吸附位点,在氧化降解甲苯过程中起重要作用[16]。MnOx(MA)在1155 cm-1附近出现的新峰为酸酐中的C![]() O键,这是由于在烧结催化剂过程中乙酸根在高温下的相互作用,形成的酸酐附着在催化剂表面而被检测到。在565 cm-1处出现的2个宽峰为MnO6八面体骨架的振动峰,这同锰与氧之间连接的化学键相关[17-18]。以上红外结果证实了MnOx在载体表面被成功合成,且前驱物会通过阴离子在高温下发生反应,产物附着在催化剂表面而影响后续反应进行。且N2吸附-脱附结果显示,在负载量为15%时,MnOx(MA)和MnOx(MS)的比表面积分别为243.2,233.9 m2/g。
O键,这是由于在烧结催化剂过程中乙酸根在高温下的相互作用,形成的酸酐附着在催化剂表面而被检测到。在565 cm-1处出现的2个宽峰为MnO6八面体骨架的振动峰,这同锰与氧之间连接的化学键相关[17-18]。以上红外结果证实了MnOx在载体表面被成功合成,且前驱物会通过阴离子在高温下发生反应,产物附着在催化剂表面而影响后续反应进行。且N2吸附-脱附结果显示,在负载量为15%时,MnOx(MA)和MnOx(MS)的比表面积分别为243.2,233.9 m2/g。
2.2 介质阻挡放电协同催化降解甲苯实验
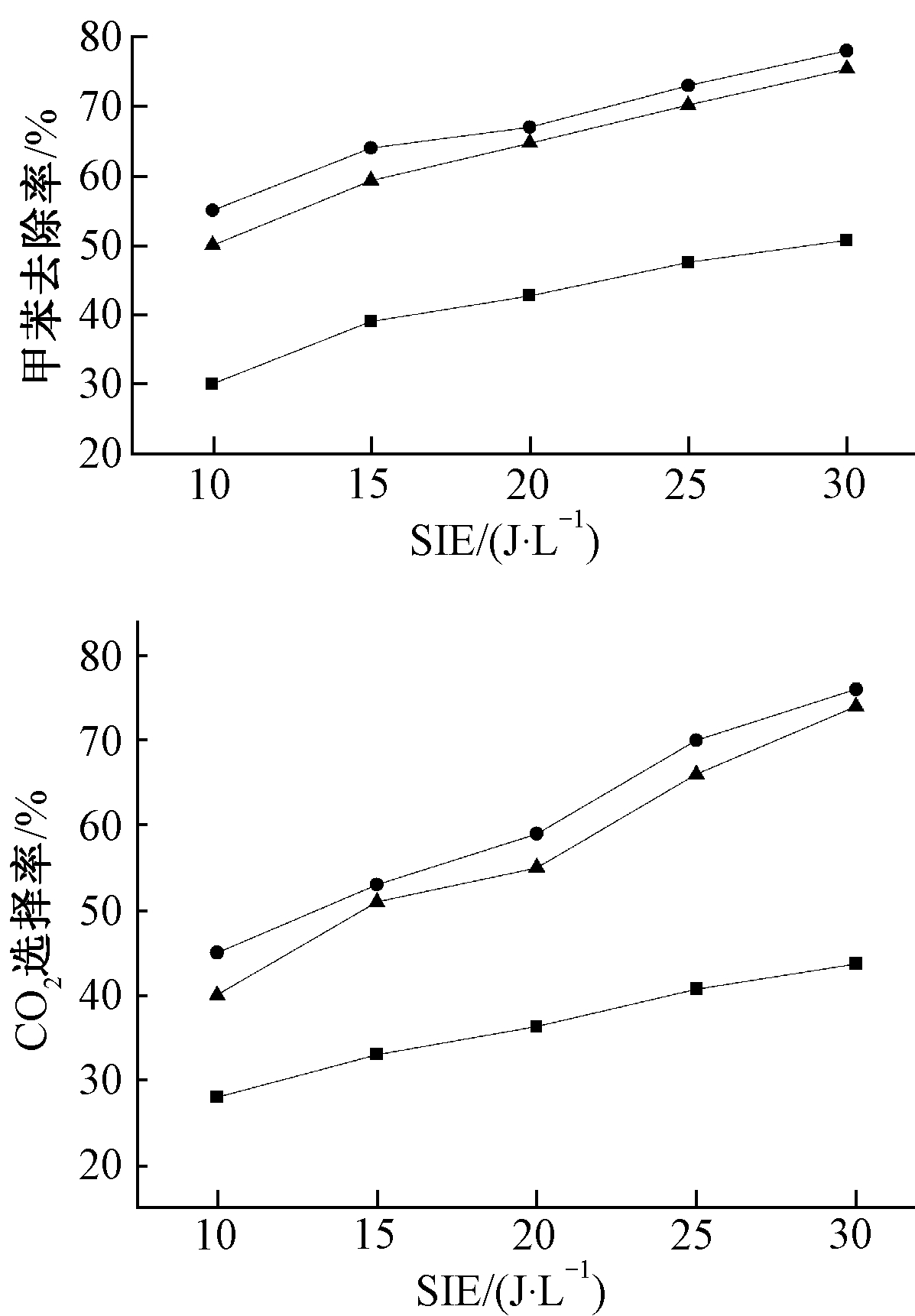
采用DDBD反应器在空气中放电产生等离子体降解甲苯,考察SIE对甲苯去除率、CO2选择率的影响如图4所示。由图4a可知:利用DDBD降解甲苯,随着SIE的增加甲苯去除率增加,甲苯去除率为30%~50.7%,原因在于SIE增加使DDBD反应器内的电场强度和电子密度增加,从而促进了电子和污染物的碰撞概率,使得甲苯的降解率升高。由图4b可知:CO2选择率的规律与甲苯降解相同,且CO2作为甲苯完全矿化的产物在DDBD反应器内浓度并不高,这是由于降解甲苯过程中生成了中间产物。
![]() —DDBD;
—DDBD; ![]() —DDBD-MnOx(MA);
—DDBD-MnOx(MA); ![]() —DDBD-MnOx(MS)。
—DDBD-MnOx(MS)。
注:C0=1.08×10-4,Q=500 mL/min,T=25 ℃,催化剂负载量15%。
图4 前驱物对催化剂性能的影响
Fig.4 The effects of precursor on catalysts performance
不同前驱物制备的MnOx催化剂会影响Mn元素在催化表面的分散性和催化剂的活性[15]。因此,选择硫酸锰和乙酸锰作为前驱物,分别制备MnOx(MS)和MnOx(MA) 2种催化剂,其降解甲苯效果如图4所示。可知:增加2种催化剂后甲苯的去除率得到大幅提升。由此可见,催化剂的增加有助于提高甲苯的分解。DDBD-MnOx(MS)实验中,随着电压增加甲苯去除率平缓地增加;DDBD-MnOx(MA)实验中,随着电压增加甲苯去除率增长迅速。其原因在于DDBD中产生O3等长寿命物质进到催化阶段,在催化表面分解为活性氧原子(·O),促进甲苯进一步分解[19]。此外,MnOx(MA)具有较大的比表面积(见2.1节),有利于Mn元素在催化剂表面均匀分布,高能活性物质和甲苯更好地附着在催化表面使二者进一步发生氧化反应。该结果与Wang等[20]降解邻二甲苯实验的趋势相近。此外,在增加MnOx催化剂后CO2的选择率大幅度增加,表明甲苯在等离子体和MnOx的共同作用下分解得更彻底。
2.3 NOx分析
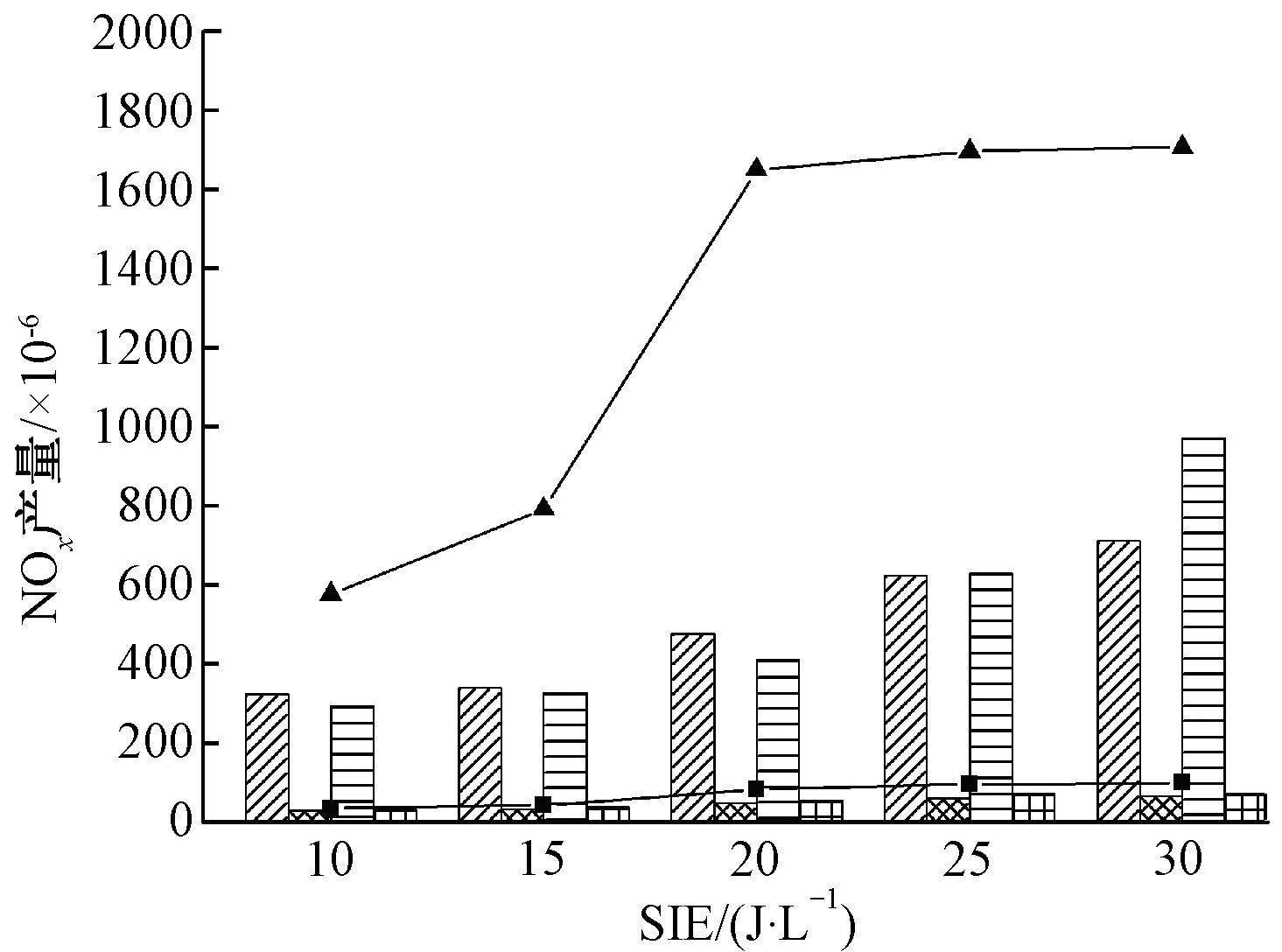
NOx作为等离子体在空气中放电的主要副产物,过多的NOx生成会影响DDBD反应器对甲苯降解的效果。本实验中,在尾气中检测到的NOx主要为NO和NO2,如图5所示。可知:DDBD-MnOx降解甲苯过程中催化剂对NOx生成具有抑制作用。随着峰值电压的增加,DDBD-MnOx系统中产生的NOx先增加后逐渐平稳。在SIE=20 J/L时,DDBD-MnOx(MS)和DDBD-MnOx(MA)抑制 NO2的生成,分别达到74.3%和77.9%,同时对NO抑制分别达到39.7%和47.2%。其原因在于催化剂表面会发生一系列氧化还原反应,使NO氧化成N2或NO2,NO2在有活性物质时进一步转化为![]()
![]() —低温等离子体(NTP)产生NO2;
—低温等离子体(NTP)产生NO2; ![]() —NTP产生NO;
—NTP产生NO; ![]() MnOx(MA)-NO2;
MnOx(MA)-NO2; ![]() MnOx(MA)-NO;
MnOx(MA)-NO; ![]() MnOx(MS)-NO2;
MnOx(MS)-NO2; ![]() MnOx(MS)-NO。
MnOx(MS)-NO。
图5 前驱物对NOx产量的影响
Fig.5 The effects of precursor on NOx yield
2.4 O3分析
在以空气为背景气体(空气-DDBD)时O3的产生是不可避免的。实验中DDBD产生的O3浓度随着峰值电压的增高而增高。由于在10.5 kV时,甲苯的去除率和COx选择性最高,因此选择SIE=25 J/L时,探究DDBD-15%MnOx降解甲苯实验对O3产量的影响。DDBD产生、DDBD消耗和DDBD-MnOx(MA)三种情况下O3浓度分别为7.12×10-4,3.247×10-4,2.2×10-4。由此可知:空气-DDBD反应体系中产生高浓度O3,在通入甲苯后其浓度下降54.4%,说明O3参与了甲苯的氧化降解过程;在DDBD-15%MnOx降解甲苯时O3浓度下降69.1%,说明根据Langmuir-Hinshelwood理论,VOCs和O3会吸附在催化剂表面的Mn原子上,进一步发生氧化反应,且催化剂表面的Mn分散程度高时可以促进O3转化,从而有利于甲苯的氧化分解[22],图6为氧化甲苯的机理。在催化剂氧化降解甲苯时,·O与甲苯反应速率远高于O3与甲苯的反应速率[1,23],此时在催化表面会发生如下反应:
O3+M→MO+O2
(4)
O3+MO→M+2O2
(5)
式中:M为催化剂活性位点。
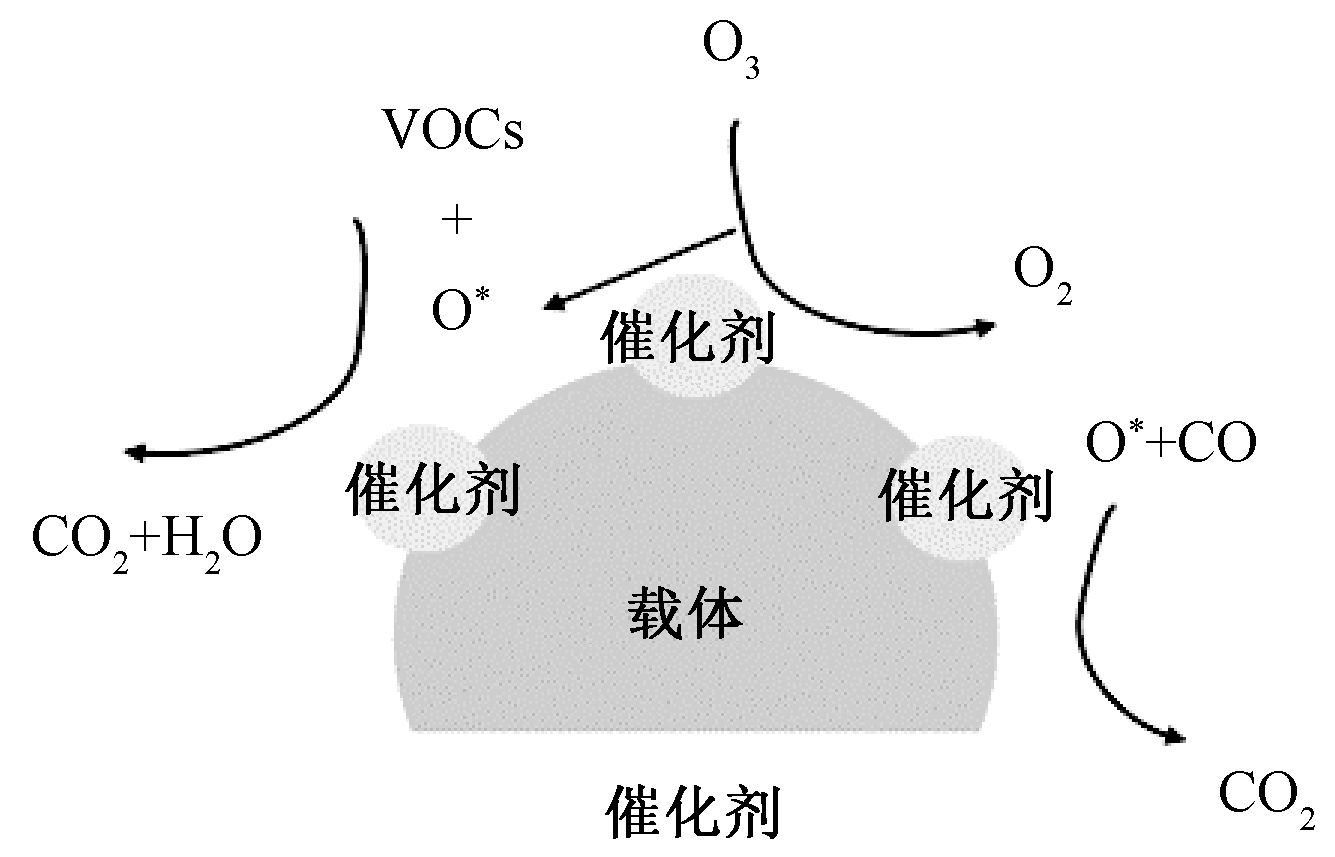
图6 MnOx氧化甲苯的机理示意
Fig.6 Mechanism for oxidation of toluene via MnOx
3 结 论
1)MnOx(MS)和MnOx(MA)催化剂均可在DDBD的基础上提升甲苯的降解率,其中MnOx(MA)具有更强的氧化降解能力。当负载量为15%时,DDBD协同MnOx(MA)处理甲苯效果最佳且NOx产量最少。因其具有较大的比表面积,有利于甲苯和其他物质的吸附;同时,其表面具有—OH和Mn4+为污染物提供更多的催化位点,有利于甲苯的催化氧化;前驱物可通过阴离子之间在高温下发生化学反应,进而影响污染物的降解。
2)甲苯在经过DDBD-MnOx(MA)处理后,相比单独DDBD处理甲苯时,COx转化率提升39.2%,NO降低63.0%,NO2降低28.2%,O3降低33.4%。
综上,等离子体和催化结合具有处理效率高且价格低廉等优点,为低浓度废气处理提供了一种可行的降解手段。
[1] Mustafa M F, Liu Y J, Duan Z H, et al. Volatile compounds emission and health risk assessment during composting of organic fraction of municipal solid waste[J]. Journal of Hazardous Materials, 2017, 327: 35-43.
[2] Hu J, Jiang N, Li J, et al. Discharge characteristics of series surface/packed-bed discharge reactor driven by Bipolar Pulsed Power[J]. Plasma Science and Technology, 2016, 18: 254-258.
[3] Guo T, Li X S, Li J Q, et al. On-line quantification and human health risk assessment of organic by-products from the removal of toluene in air using non-thermal plasma[J]. Chemosphere, 2018, 194: 139-146.
[4] Abbas H F, Daud W W. Hydrogen production by methane decomposition: a review[J]. International Journal of Hydrogen Energy, 2010, 35: 1160-1190.
[5] Schiavon M, Scqpinello M, Tosi P, et al. Potential of non-thermal plasmas for helping the biodegradation of volatile organic compounds(VOCs) released by waste management plants[J]. Journal of Cleaner Production, 2015, 104: 211-219.
[6] 闫克平,李树然,冯卫强,等. 高电压环境工程应用研究关键技术问题分析及展望[J]. 高电压技术,2015,41(8):2025-2544.
[7] 竹涛,和娴娴,陈锐,等. 低温等离子体反应器去除挥发性有机化合物的能效分析[J]. 高电压技术,40(10):2986-2990.
[8] Mustafa M F, Fu X D, Liu Y J, et al. Volatile organic compounds(VOCs) removal in non-thermal plasma double dielectric barrier discharge reactor[J]. Journal of Hazardous Materials, 2018, 347: 317-324.
[9] 姚水良,毛灵爱,张霞,等.等离子体复合微量贵金属催化反应器催化氧化苯的机理分析[J]. 高电压技术,2017,43(12):3973-3980.
[10] Chang T, Shen Z X, Huang Y, et al. Post-plasma-catalytic removal of toluene using MnO2-Co3O4 catalysts and their synergistic mechanism[J]. Chemical Engineering Journal, 2018, 348: 15-25.
[11] Fan X, Zhu T L, Wang M Y, et al. Removal of low-concentration BTX in air using a combined plasma catalysis system[J]. Chemosphere, 2009, 75(10): 1301-1306.
[12] Bo Z, Hao H, Yang S L, et al. Vertically-oriented graphenes supported Mn3O4 as advanced catalysts in post plasma-catalysis for toluene decomposition[J]. Applied Surface Science, 2018, 436: 570-578.
[13] Dhandapani B, Dyama S T. Gas phase ozone decomposition catalysts[J]. Applied Catalysis B: Environmental, 1997, 11: 129-166.
[14] Yu Q J, Gao Y M, Tang X L, et al. Removal of NO from flue gas over HZSM-5 by a cycling adsorption-plasma process[J]. Catalysis Communications, 2018, 110: 18-22.
[15] Rezaei E, Soltan J. Low temperature oxidation of toluene by ozone over MnOx/γ-alumina and MnOx/MCM-41 catalysts[J]. Chemical Engineering Journal, 2012, 198/199: 482-490.
[16] 朱利安 R.H.罗斯. 多相催化:基本原理与应用[M]. 田野,张立红,赵宜成,等译. 北京:化学工业出版,2015:70-75.
[17] Tang X F, Li Y G, Huang X M, et al. MnOx-CeO2 mixed oxide catalysts for complete oxidation of formaldehyde: Effect of preparation method and calcination temperature[J]. Applied Catalysis B: Environmental, 2006, 62(3/4): 265-273.
[18] Zhang C, Liu F, Zhai F, et al. Alkali-metal-promoted Pt/TiO2 opens a more efficient pathway to formaldehyde oxidation at ambient temperatures[J]. Angewandte Chemie International Edition, 2012, 51(38): 9628-9632.
[19] Pangilinan C D C, Kurnianwan W, Hinode H. Effect of MnOx/TiO2 oxidation state on ozone concentration in a nonthermal plasma-driven catalysis reactor[J]. Ozone Science and Engineering, 2016, 38(2): 156-162.
[20] Wang L, He H, Zhang C B, et al. Effects of precursors for manganese-loaded γ-Al2O3 catalysts on plasma-catalytic removal of o-xylene[J]. Chemical Engineering Journal, 2016, 288: 406-413.
[21] Liu Y N, Braci L, Cavadias S, et al. Post-discharge treatment of air effluents polluted by butyl-mercaptan: the role of nitrate radical[J]. Journal of Physics D: Applied Physics, 2011, 44(9): 8.
[22] Subrahmanyam C, Renken A, Kiwi-Minsker L. Novel catalytic non-thermal plasma reactor for the abatement of VOCs[J]. Chemistry Engineering Journal, 2007, 134(1): 78-83.
[23] Rezaei E, Soltan J, Chen N, et al. Catalytic oxidation of toluene by ozone ove alumina supported manganese oxides: effect of catalyst loading[J]. Applied Catalysis B: Environment, 2013, 136/137(3): 239-247.