0 引 言
重金属污染已成为近年来危害最大的水污染问题之一[1]。重金属污染具有持久性、隐蔽性、毒性大、不能被微生物降解等特点,并且可通过生物富集作用破坏生态系统平衡,甚至可通过化学和生物作用与有机物结合,形成毒性更强的有机金属[2-3]。其中铅是常见的重金属中毒性最大的污染物之一,不同工业过程和自然过程会使得铅被释放到水、空气和土壤环境中,对生态系统和人类健康造成损害。它主要来自化石燃料燃烧、硫化矿冶炼、酸性矿山排水和各种金属电镀、炼油等活动[4]。天然或工业废水中存在铅是世界范围内最严重的环境问题之一,并且受到世界各地研究人员的广泛关注[5-9],去除水域和废水中的铅对保证公共卫生与环境安全至关重要[10]。据报道,现阶段已有一些材料可用于去除水中不同的重金属离子,例如稻壳、松树皮、粉煤灰等,但由于制备工艺复杂、吸附稳定性低和不易再生等原因限制并没有被广泛使用[11-22]。
赤泥是氧化铝工业中铝土矿经强碱浸出时产生的固体废渣,因含有大量氧化铁呈红色而得名。赤泥中含有多种金属氧化物,如Fe2O3、SiO2、CaO、Al2O3、TiO2、Na2O、K2O等[23]。因为赤泥具有较好的化学稳定性、机械稳定性和结构属性,所以可经特定的物理、化学方法处理后成为非常具有潜力的水处理材料,如Lakshmi等[24]制备出1种氧化铁涂层的酸处理活化赤泥,实验结果表明,化学改性大大地提高了赤泥的比表面积,对Pb2+的吸附容量得到很大提升。
酸活化后赤泥主要成分是SiO2,而SiO2表面具有大量的化学反应活性的羟基,它可以与有机硅烷(APTES)通过缩合反应引入氨基基团。活性氨基可以与Pb2+等过渡金属离子发生配位或螯合作用,从而大大提高选择性吸附效率。本文依次采用盐酸和3-氨丙基三乙氧基硅烷对赤泥进行改性,制备出1种去除率高、吸附量大、吸附效果好的重金属铅离子吸附剂。通过探讨改性吸附剂对Pb2+的去除性能,为赤泥在水处理中的应用提供参考。
1 实验部分
1.1 主要试剂与仪器
主要试剂:拜耳法赤泥,河南长兴实业有限公司;3-氨丙基三乙氧基硅烷,分析纯,天津市科密欧化学试剂有限公司;硝酸铅,分析纯,天津市大茂化学仪器供应站;甲苯,分析纯,成都市科隆化学品有限公司;浓盐酸,分析纯,成都市科隆化学品有限公司。
主要仪器:CHNOS全能元素分析仪,inductar EL cube型,德国;ICPE-9000,日本岛津制作所;傅里叶变换红外光谱仪(FTIR),Spectrum one型,美国P-E Com;扫描电镜(SEM),EVO 18型,德国蔡司(ZEISS)公司;比表面积及微孔孔径分析仪(BET),BET-201A型,美国PMI公司(中国);X射线衍射仪(XRD),D8 Advance型,德国;电热恒温水浴锅,北京市永光明医疗仪器厂;真空干燥箱,DZF-6090型,上海景迈仪器设备有限公司;恒温摇床,ZWY-240型,上海智诚有限公司;数控超声波清洗器,KQ5200DE型,昆山市超声仪器有限公司。
1.2 改性吸附剂的制备
取5 g新鲜的拜耳法赤泥在105 ℃烘箱中干燥2 h 以去除赤泥中的少量水分,然后取出研磨到80目,将赤泥粉末加入12 mol/L的浓盐酸溶液中,以液固比为5∶1、65 ℃下连续搅拌反应1 h,经洗涤、烘干后得到酸浸后赤泥。
将1.0 g酸浸后赤泥和1 mL APTES,加入50 mL甲苯中,在温度为115 ℃条件下,进行12 h冷凝回流。反应完成后,使用少量甲苯、无水乙醇、蒸馏水各洗涤2次,然后抽滤。最后,将改性好的赤泥于105 ℃真空箱中干燥12 h,制得APTES氨基改性赤泥。
通过 SEM、BET、FTIR、XRD、元素分析和热重分析等方法分析改性前后材料。
1.3 改性赤泥吸附剂吸附Pb2+的实验
含铅废水采用Pb(NO3)2和纯水配制,分别用0.1 mol/L HCl 和NaOH 溶液调节其初始pH值。
取50 mL配制的一定浓度的含铅废水,加入0.1 g 吸附剂,放入恒温摇床中25 ℃振荡3 h,经离心分离后取上清液进行膜滤,并采用电感耦合等离子发射光谱仪测定滤液中Pb2+的浓度。分别考察溶液pH、吸附剂投加量、初始浓度、吸附温度等因素对吸附剂吸附Pb2+的影响。
2 结果与讨论
2.1 材料表征结果
2.1.1 SEM分析
1)酸浸前后样品SEM对比。
浓盐酸酸浸前通过扫描电镜观察到原拜耳法赤泥颗粒(见图1(a),放大5000倍)由一些胶结连接为主、结晶连接为辅的胶凝结构体构成,赤泥颗粒形态不规则,表面粗糙多孔,其孔道主要以片状颗粒堆积而且分布不均匀。观察经浓盐酸酸浸后的赤泥(图1(b),放大5000倍)可看出:改性后赤泥的表面结构紧密,胶结连接消失,出现较多致密小孔,表面出现许多细小的球形颗粒。

图1 酸浸前后赤泥SEM
Fig.1 SEM images of red mud before and after acid leaching
2)有机溶剂改性前后样品SEM对比。
对3-氨丙基三乙氧基硅烷改性前后赤泥进行电镜扫描,改性前赤泥(见图2(a),放大12000倍)表面出现许多致密小孔,孔径变小,孔道变大;经改性后(见图2(b),放大12000倍),赤泥外形轮廓较为粗糙,颗粒之间发生团聚现象,有的甚至团聚成大颗粒。这说明经过有机官能团修饰后,化学反应活性位点增加,表面极性增大,彼此之间易发生反应,产生团聚,说明有机官能团的引入在一定程度上改变了赤泥的表面形貌;改性后的赤泥保留了多孔结构,这是由于前阶段酸活化处理导致了一定程度的扩孔效果。

图2 改性前后赤泥SEM
Fig.2 SEM images of red mud before and after modification
2.1.2 样品XRD和元素分析
酸浸前后赤泥XRD对比见图3。可知:经浓盐酸酸浸后原拜耳法赤泥中部分金属氧化物的衍射峰消失,如方解石(CaCO3)、钙钛矿(CaTiO3)、硅酸二钙(Ca2SiO4)、水钙铝榴石[Ca3Al2(SiO4)(OH)8]、赤铁矿(Fe2O3)、锐钛矿(TiO2),只在2θ=26.56°出现了SiO2的衍射峰。这说明经盐酸处理后去除了大量的金属元素,达到对拜耳法赤泥提纯的目的,对后续吸附剂的改性提供了实验基础。
酸浸前后样品元素分析如表1所示。可知:经浓盐酸酸浸后主要一些金属氧化物含量大幅减少,SiO2含量明显提升,这与上述XRD图谱反映信息一致。
2.1.3 材料的BET分析
由BET分析得,经浓盐酸酸浸后样品的比表面积从12.97 m2/g增加到236.67 m2/g(表2),是由于经过酸浸可以洗脱赤泥表面物质,去除分布于物质通道中的杂质,使赤泥中以凝聚体、集粒体、团聚体为主的结构变得疏松,进而孔道扩大,孔隙结构得到改善,有利于被吸附物质的扩散。此外,由于H+半径较小,较易置换出矿物层间离子半径较大的离子,如K+、Na+、Mg2+、Ca2+等,使孔隙容积变大,比表面积显著增大。但硅烷化改性后比表面积有一定减小,这可能是由于大分子有机物质接枝堵塞了赤泥表面孔道[25]。
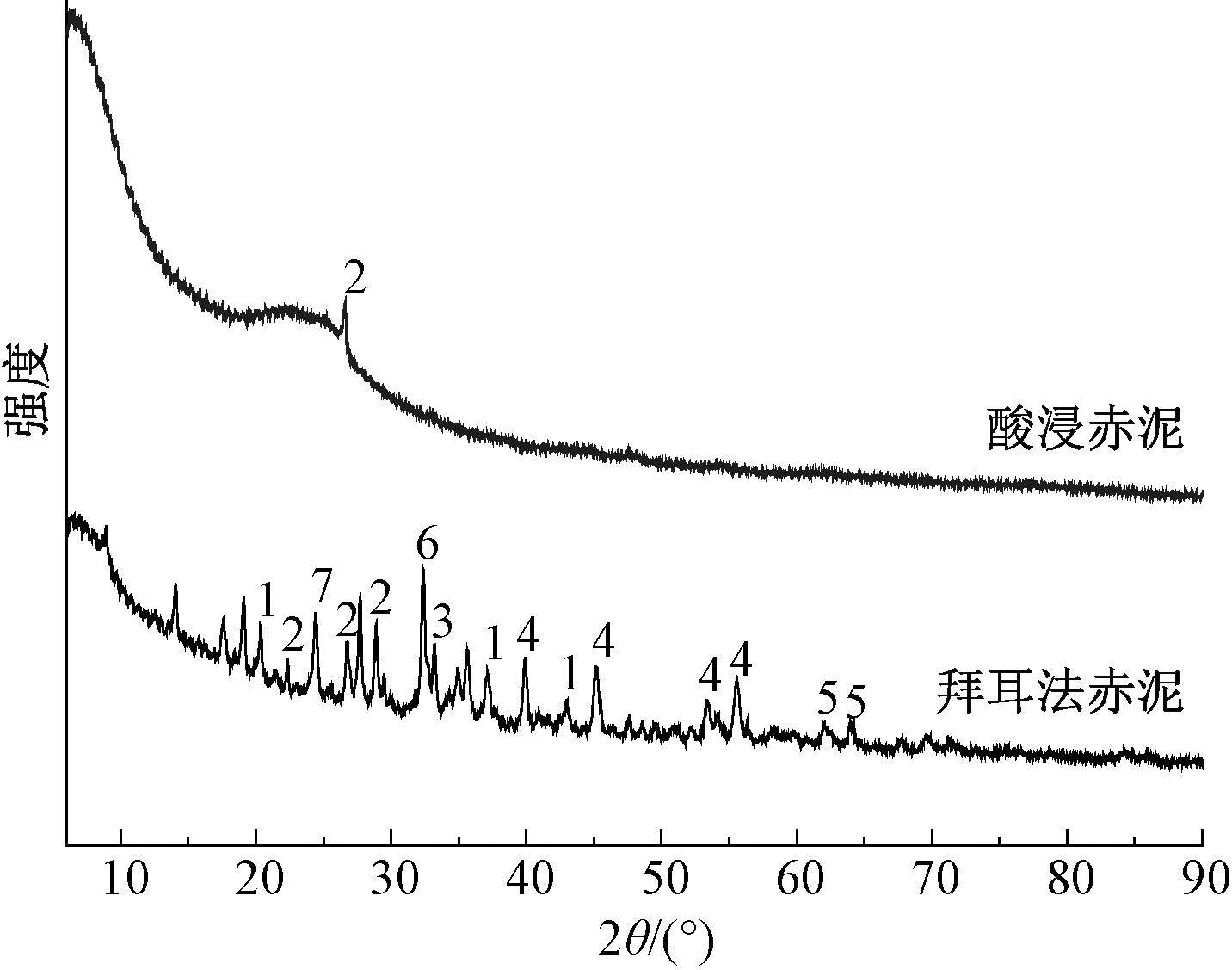
1—CaCO3; 2—SiO2; 3—CaTiO3; 4—Ca3Al2(SiO4)(OH)8;
5—Fe2O3; 6—Ca2SiO4; 7—TiO2。
图3 酸浸前后样品XRD
Fig.3 XRD patterns of samples before and after acid leaching
表1 酸浸前后样品元素分析
Table 1 Analysis of sample elements before and after acid leaching
%
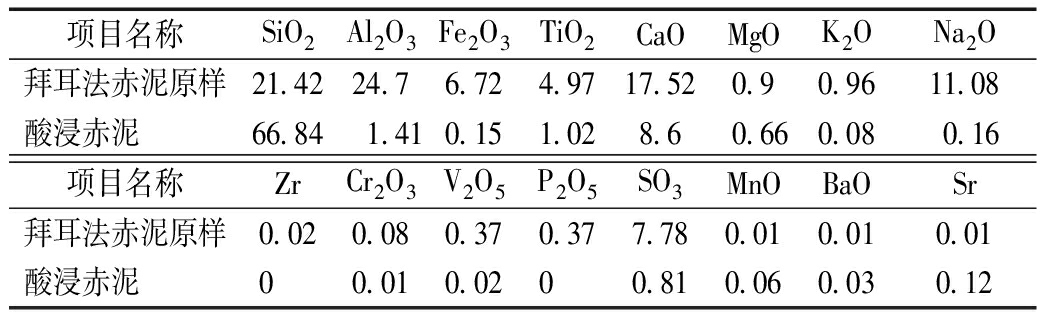
项目名称SiO2Al2O3Fe2O3TiO2CaOMgOK2ONa2O拜耳法赤泥原样21.4224.76.724.9717.520.90.9611.08酸浸赤泥66.841.410.151.028.60.660.080.16项目名称ZrCr2O3V2O5P2O5SO3MnOBaOSr拜耳法赤泥原样0.020.080.370.377.780.010.010.01酸浸赤泥00.010.0200.810.060.030.12
表2 原赤泥、酸浸赤泥和硅烷化赤泥的比表面积分析
Table 2 Analysis of specific surface area of original red mud, acid immersed red mud and silanized red mud

样品SBET/(m2·g-1)V/(cm3·g-1)R/nm拜耳法原赤泥12.970.1624.86酸浸赤泥236.670.958.03硅烷化赤泥227.520.6411.26
2.1.4 材料的FT-IR分析
有机改性前后样品FT-IR分析如图4所示。可知:改性前后在470,800,1109 cm-1左右分别出现Si—O—Si的弯曲振动峰、摇摆伸缩振动峰和反对称伸缩振动峰,说明改性前后SiO2骨架并没有发生变化;2938、2848 cm-1的峰对应3-氨丙基三乙氧基硅烷丙基链上的C—H伸缩振动峰;1500~1600 cm-1的峰对应氨基(N—H)弯曲振动峰。可以证明该吸附材料为3-氨丙基三乙氧基硅烷和赤泥改性产物。
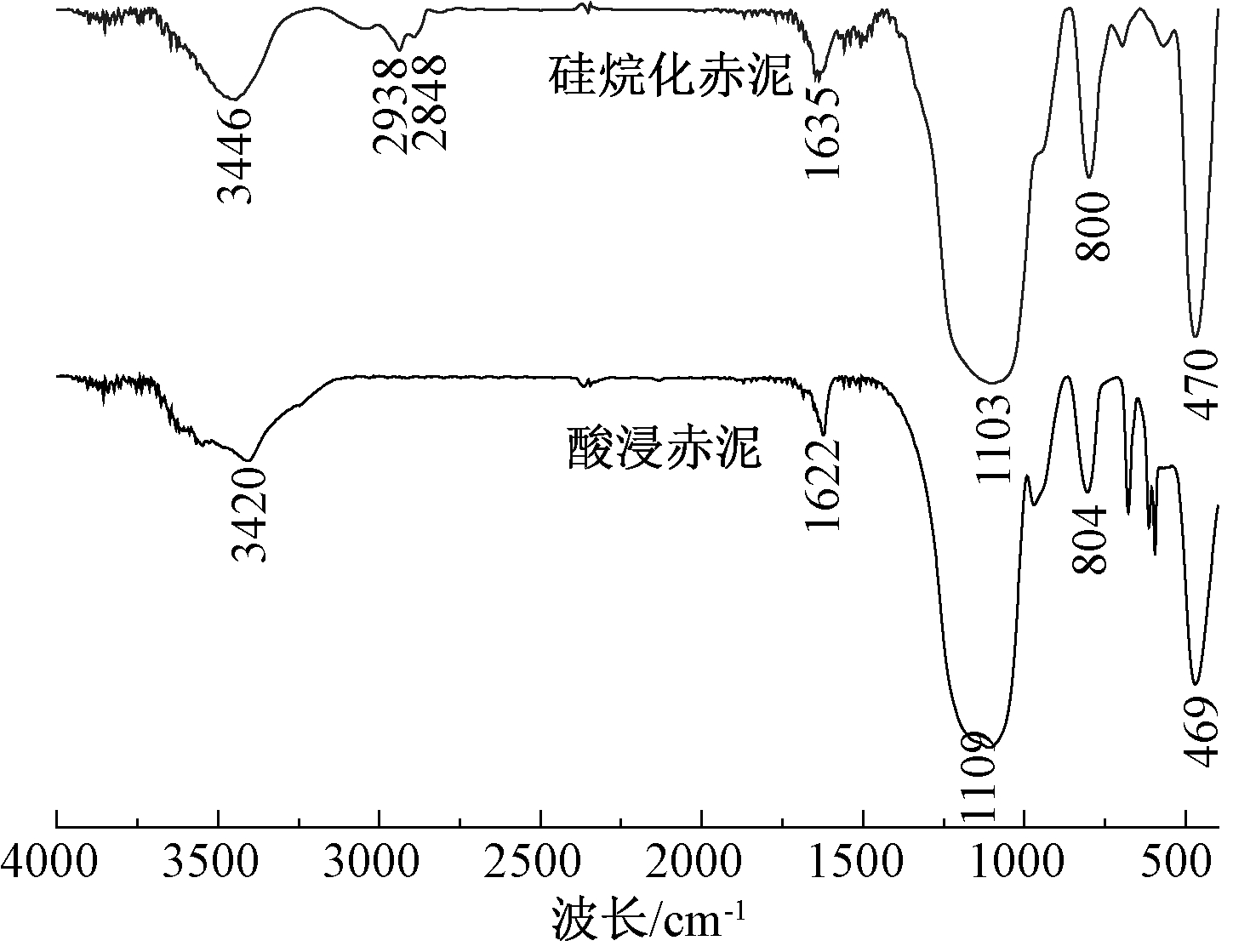
图4 有机改性前后样品FT-IR图谱
Fig.4 FT-IR spectra of samples before and after organic modification
2.1.5 材料的元素分析
对改性前后的赤泥元素进行分析(表3),在浓盐酸改性处理后C、H和N的含量都较小,且差别不大;硅烷化改性后,由于有机基团的导入,C、H和N元素含量比例明显上升。
表3 原赤泥、酸浸赤泥和硅烷化赤泥的元素分析
Table 3 Elemental analysis of original red mud, acid immersed red mud and silanized red mud %
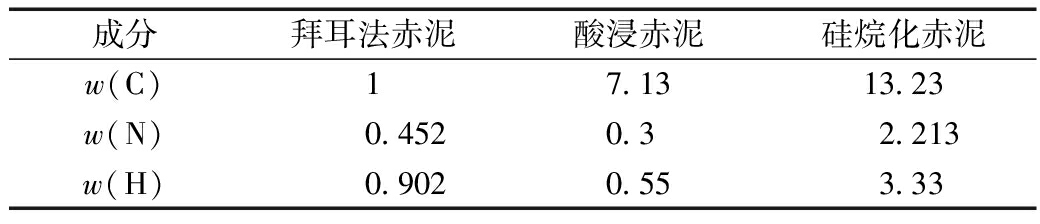
成分拜耳法赤泥酸浸赤泥硅烷化赤泥w(C)17.1313.23w(N)0.4520.32.213w(H)0.9020.553.33
2.1.6 材料的热重分析
为了初步研究温度对材料热稳定性的影响,采用热重(TGA)对改性前后材料的热解性质进行研究,结果如图5所示。可知:当温度从25 ℃上升到800 ℃时,拜耳法赤泥的热失重最多。由于赤泥主要由石英、赤铁矿、方解石、钙霞石、水铝石构成,因此赤泥的热重曲线可以分为3个阶段:第1阶段为25~150 ℃,质量损失为3.5%,这主要是由赤泥表面的吸附水蒸发引起;第2阶段为150~300 ℃,勃姆石、三水铝矿和水草酸钙石中的水化水蒸发失重使得该阶段的赤泥质量减少了2.5%;第3阶段为300~800 ℃,该阶段赤泥的质量减少了18%,这是由于水铝石和三水铝矿中的结合水分解和赤泥中的方解石等矿物成分受热分解释放出CO2造成的质量损失[26]。
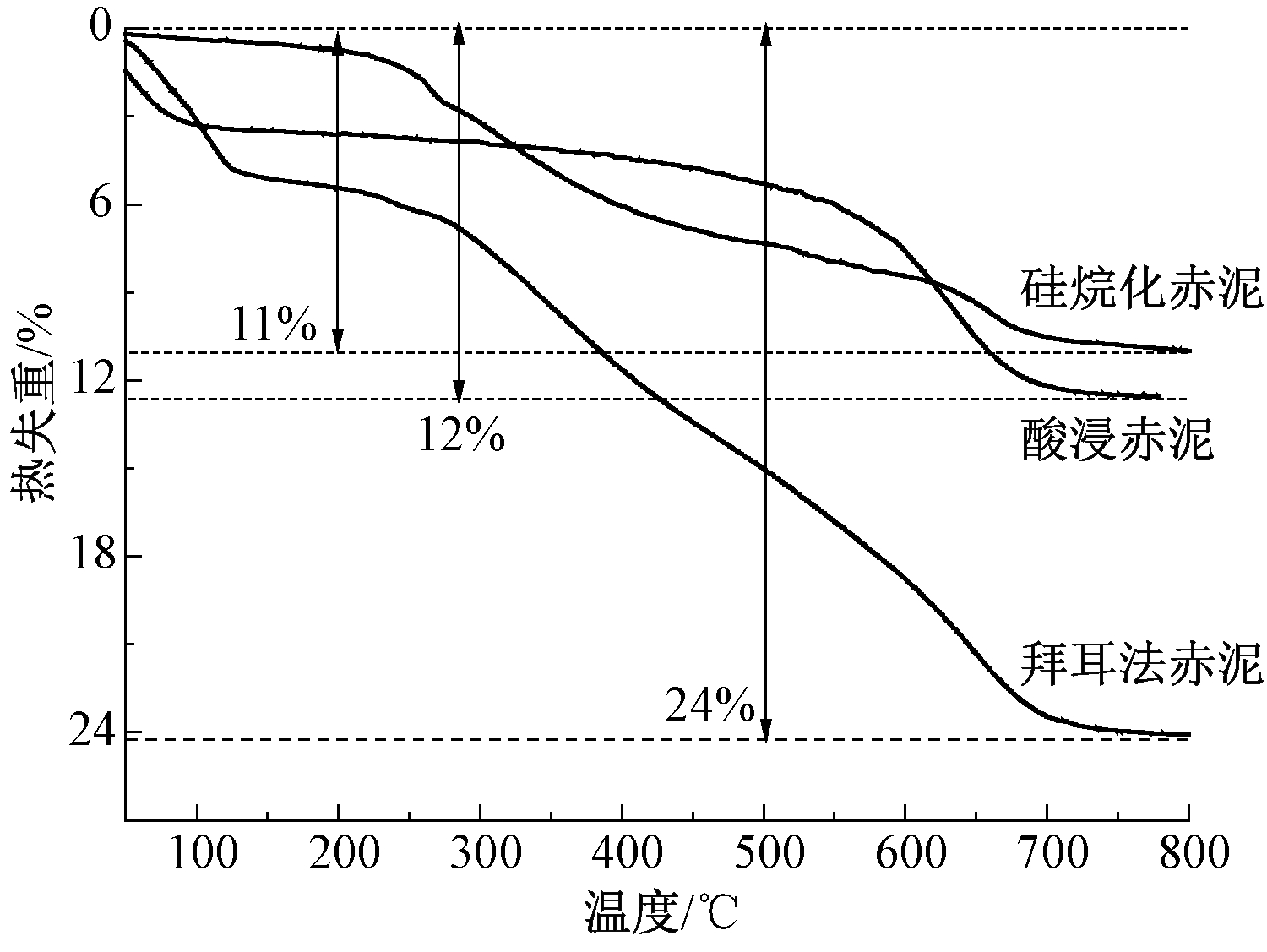
图5 拜耳法赤泥、酸浸赤泥和硅烷化赤泥的TGA图
Fig.5 TGA curves of red mud, acid leaching red mud and silanized red mud
经盐酸酸浸后的赤泥在25~100 ℃内有少量失重,是由于样品中残留水分的蒸发;在200~800 ℃内失重(8%)主要是由于经盐酸酸浸后赤泥主要由SiO2构成,含碳化合物的比例低于拜耳法赤泥,导致在升温过程中酸浸赤泥的质量损失低于拜耳法赤泥。
经有机改性后的硅烷化赤泥在250~650 ℃内失重约10%,主要是少量含碳化合物的热分解和不稳定的含氧或含氮官能团的分解导致材料的质量损失,但对比拜耳法赤泥和酸浸赤泥结果可知氨基功能化后的赤泥具有更好的热稳定性。
2.2 改性材料吸附Pb2+性能分析
2.2.1 pH对Pb2+吸附的影响
溶液pH不仅影响吸附剂表面电荷,还会影响其表面官能团的性质以及溶液中重金属离子的状态,不同重金属对应不同的最佳吸附pH值。当Pb2+初始浓度为200 mg/L,吸附达到饱和状态时,在不同pH条件下,硅烷化赤泥对Pb2+的去除率如图6所示。硅烷化赤泥对Pb2+的去除率随pH升高而升高,当pH>4.0时,Pb2+去除率>80%,而在pH为2.0和3.0时,其去除率<50%。主要原因是,在较低pH条件下,H+浓度高,活性较强,会与Pb2+竞争吸附位点,不利于Pb2+的吸附,并且在低pH下硅烷化赤泥表面的氨基官能团会被水中高浓度的氢离子质子化而带上正电荷,带正电荷的吸附剂与同样带正电荷的Pb2+发生排斥作用,从而大大降低与Pb2+的络合能力,这种质子化作用会随着pH的升高而减弱。当pH>4.0时,硅烷化赤泥对Pb2+的吸附作用已达到较为理想的状态,其中当pH=6.0时,其吸附去除率可高达95%以上。因此,确定实验最佳pH为6.0。
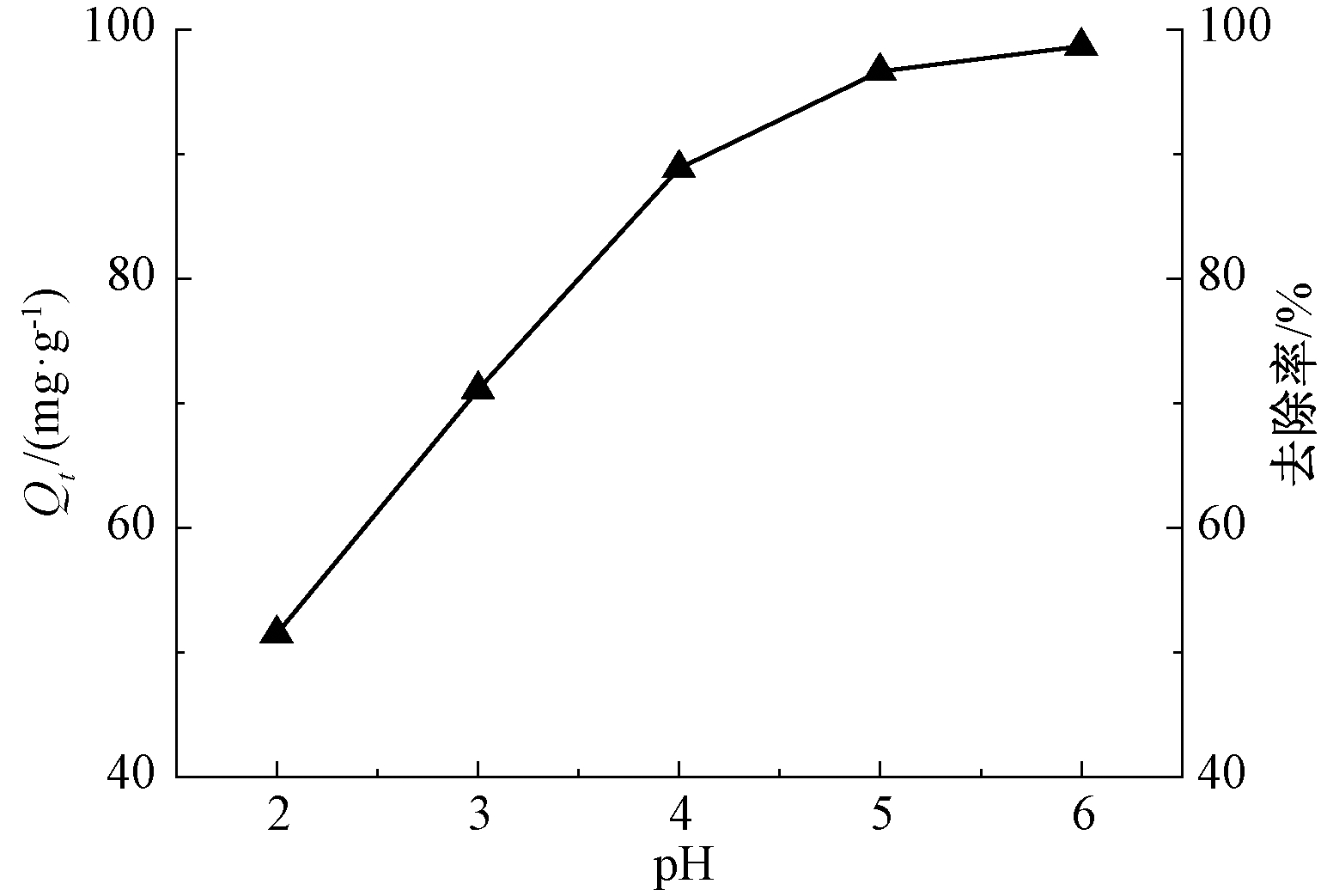
注:在对应pH下,吸附去除率和吸附量值相同。![]() —吸附量、去除率。
—吸附量、去除率。
图6 pH对Pb2+吸附过程的影响
Fig.6 Effect of initial pH values on adsorption process of Pb2+
2.2.2 投加量对Pb2+吸附的影响
取一系列10 mL初始浓度为200 mg/L、pH=6的Pb2+溶液,分别投加不同质量的吸附剂,在25 ℃下振荡3 h,抽滤后分别测定滤液中Pb2+的剩余浓度结果如图7所示。可知:在投加量为1 g/L时,去除率仅为80%;当吸附剂投加量增大到2 g/L以上时,Pb2+去除率基本保持在95%以上。这是因为吸附剂用量增加后,吸附剂总比表面积增大,表面吸附位点增多,从而能够吸附更多的Pb2+。兼顾去除效果和成本因素,设定实验投加量为2 g/L。
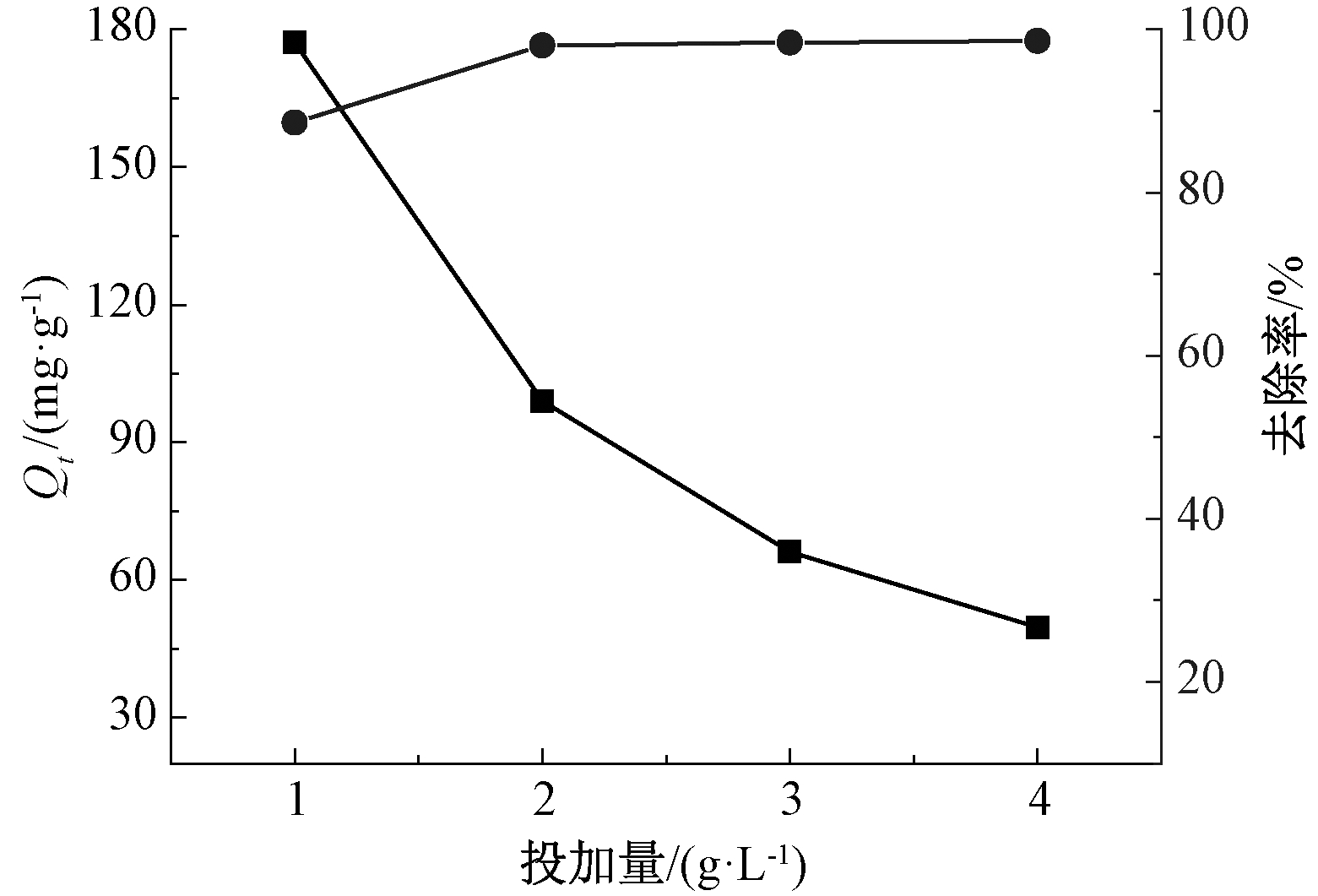
![]() —吸附量;
—吸附量; ![]() —去除率。
—去除率。
图7 吸附剂投加量对Pb2+吸附的影响
Fig.7 Effect of adsorbent’s dosage on Pb2+ adsorption
2.2.3 温度和初始浓度对Pb2+吸附的影响
为了研究吸附过程中温度对吸附时间及吸附平衡的影响,在3个温度水平研究了硅烷化赤泥对Pb2+的吸附去除率的变化如图8所示。可知:硅烷化赤泥对同一浓度100 mg/L的Pb2+吸附去除率随温度的升高而略微增加,同时温度的升高使得平衡吸附时间也缩短。因此认为,升温有利于吸附且可以提高吸附去除率。
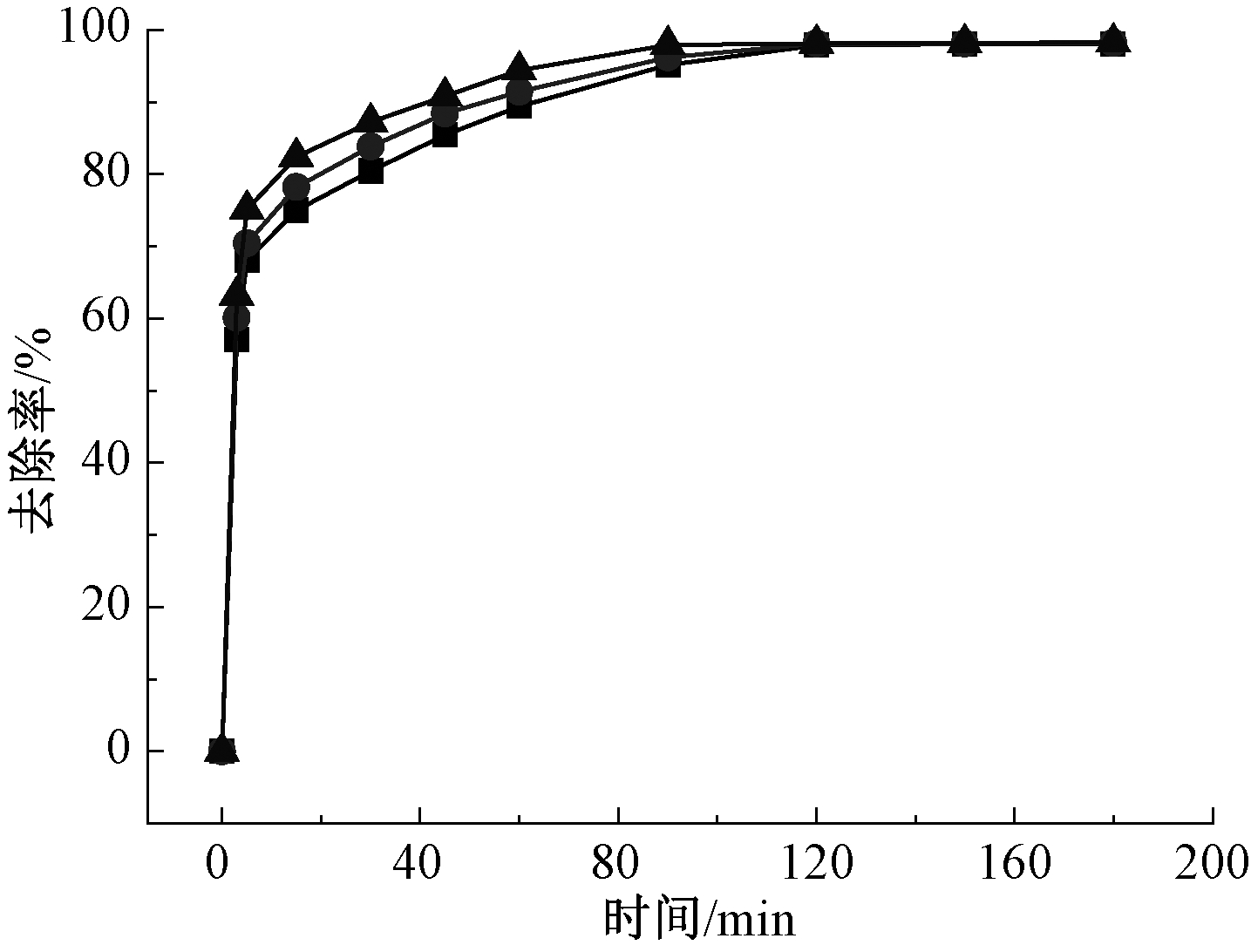
![]() —288 K;
—288 K; ![]() —298 K;
—298 K; ![]() —308 K。
—308 K。
图8 温度对硅烷化赤泥吸附去除效率的影响
Fig.8 Effect of temperature on adsorption and removal efficiency of silanized red mud
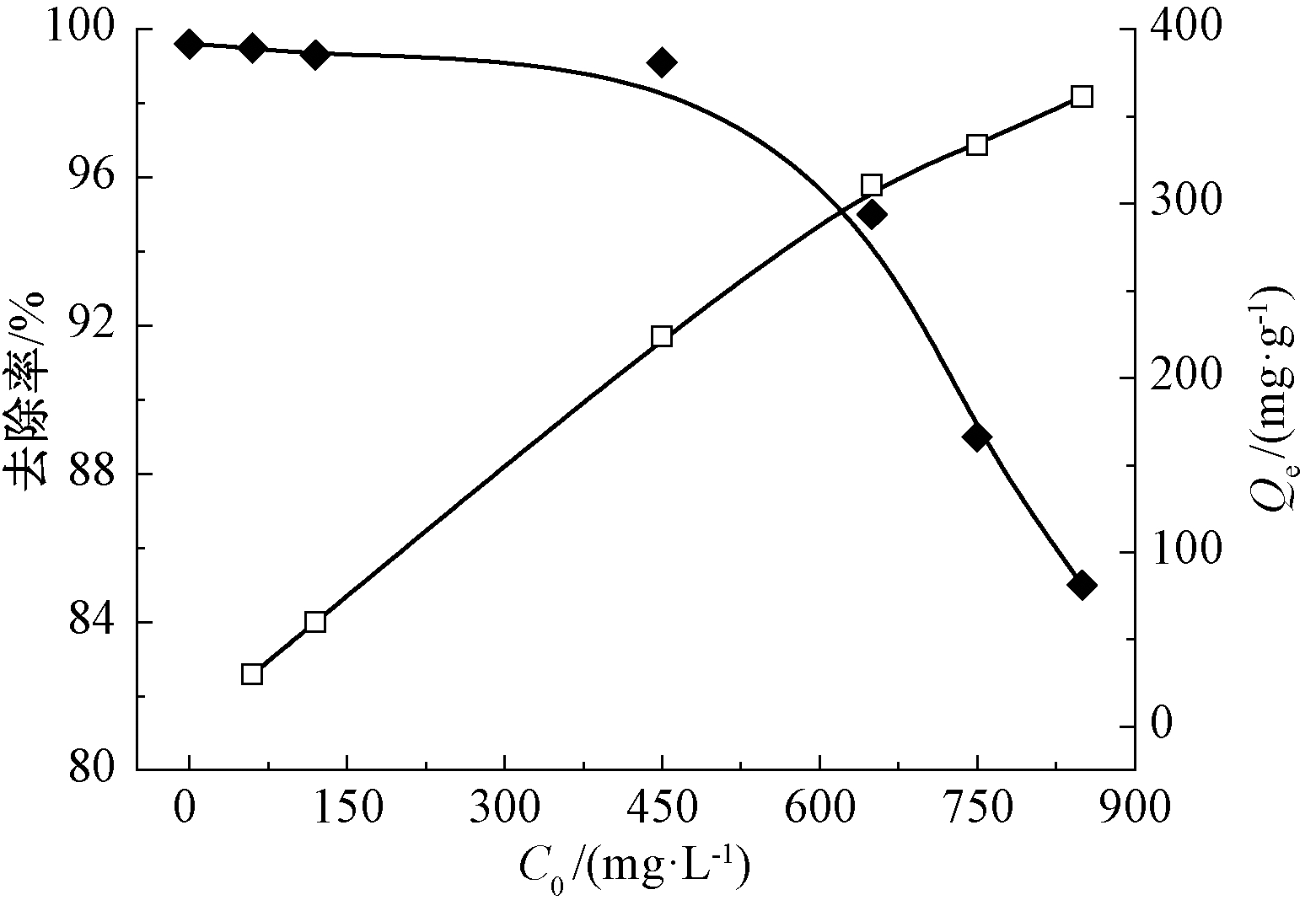
图9为不同初始浓度下,硅烷化赤泥对Pb2+吸附去除率的变化和平衡吸附量的变化。可知:硅烷化赤泥对Pb2+的吸附去除率随着初始浓度升高而降低,但是平衡吸附量逐渐升高,且有饱和吸附的趋势。
![]() —去除率;
—去除率; ![]() —吸附量。
—吸附量。
图9 Pb2+初始浓度对硅烷化赤泥吸附去除率和平衡吸附量的影响
Fig.9 Effect of initial concentration of Pb2+ on adsorption rate and equilibrium adsorption capacity of silanized red mud
2.2.4 吸附动力学研究
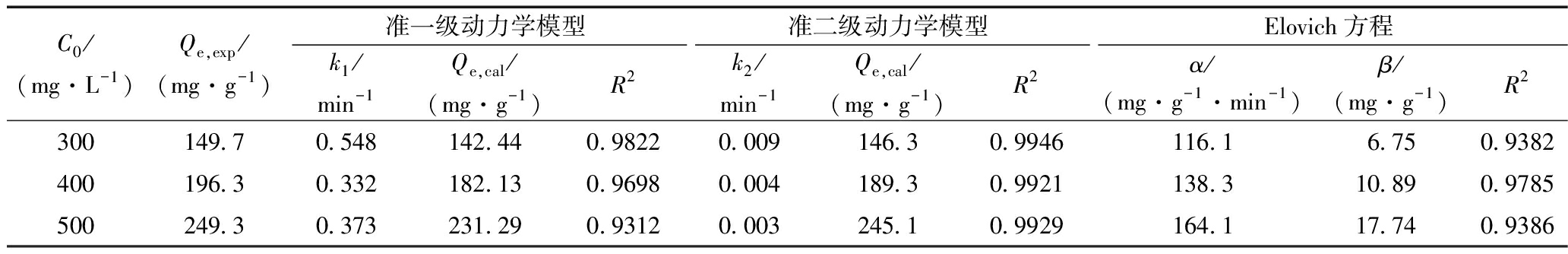
利用准一级动力学模型、准二级动力学模型和Elovich方程用于拟合3种不同初始浓度的Pb2+(300,400,500 mg/L)的实验动力学参数,其结果如图10和表4所示。从拟合的3个模型中对比可看出:准二级动力学方程更好地拟合Pb2+的吸附,拟合系数达到0.995,并且该模型拟合出的平衡吸附量更接近实测值,而准一级动力学模型和Elovich模型与实测值偏差较大,所以硅烷化赤泥对Pb2+的吸附更加符合准二级动力学模型,表明该吸附速率主要受化学吸附机制控制。
2.2.5 吸附等温线
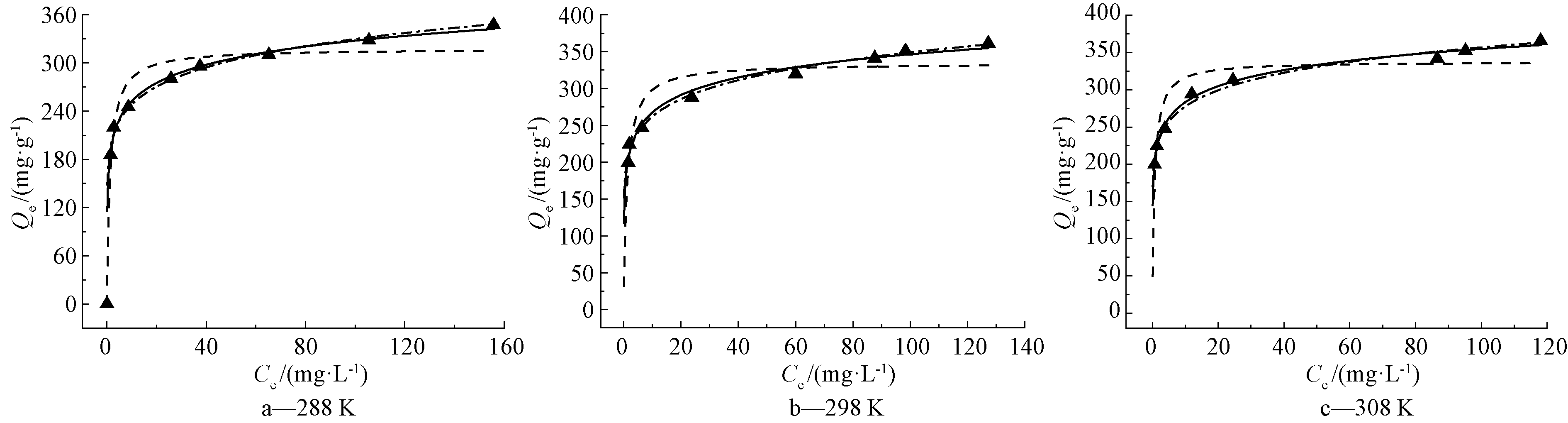
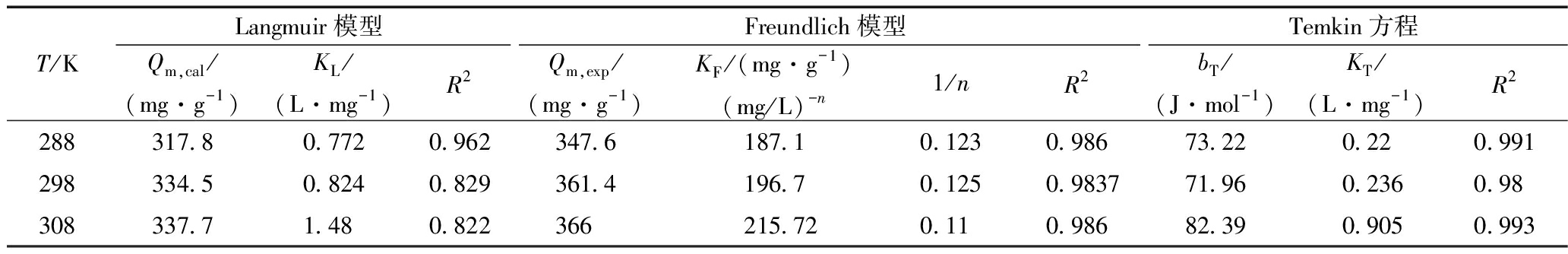
利用Langmuir、Freundlich和Temkin模型对不同温度下实验数据进行等温线模型拟合,拟合数据如图11和表5所示。可知:Freundlich等温模型拟合R2要优于Langmuir模型和Temkin模型,且Freundlich等温模型在不同温度下的1/n为0.11~0.125(<0.5),表明吸附过程较易进行,并且Pb2+在硅烷化赤泥表面的吸附过程主要为化学非均质吸附。KF值随着温度的升高而增大,也表明温度升高有利于Pb2+去除,且整个吸附过程为吸热反应[27]。

![]() 实验数据; — —准一级动力学模型; ——准二级动力学模型; —·—Elovich方程。
实验数据; — —准一级动力学模型; ——准二级动力学模型; —·—Elovich方程。
图10 不同初始浓度Pb2+准一级、准二级和Elovich的动力学模型拟合曲线
Fig.10 Kinetics plots of Pb2+ adsorption with initial concentrations of 300,400,and 500 mg/L fitting with pseudo-first-order, pseudosecond-order and Elovich models
表4 不同初始Pb2+浓度下吸附的动力学参数
Table 4 Kinetics parameters for Pb2+ adsorption at different initial Pb2+ concentrations
C0/(mg·L-1)Qe,exp/(mg·g-1)准一级动力学模型准二级动力学模型Elovich方程k1/min-1Qe,cal/(mg·g-1)R2k2/min-1Qe,cal/(mg·g-1)R2α/(mg·g-1·min-1)β/(mg·g-1)R2300149.70.548142.440.98220.009146.30.9946116.16.750.9382400196.30.332182.130.96980.004189.30.9921138.310.890.9785500249.30.373231.290.93120.003245.10.9929164.117.740.9386
![]() 实验数据; — —准一级动力学模型; ——准二级动力学模型; —·—Elovich方程。
实验数据; — —准一级动力学模型; ——准二级动力学模型; —·—Elovich方程。
图11 不同初始温度的Pb2+ Langmuir、Freundlich和Temkin吸附等温线模型拟合曲线
Fig.11 Adsorption isotherms for Pb2+ adsorption at temperature of 288, 298, and 308 K fitting with Langmuir, Freundlich and Temkin model
表5 在不同温度下Pb2+吸附的等温线参数
Table 5 Isotherm parameters for Pb2+ adsorption at different temperature
T/KLangmuir模型Freundlich模型Temkin方程Qm,cal/(mg·g-1)KL/(L·mg-1)R2Qm,exp/(mg·g-1)KF/(mg·g-1)(mg/L)-n1/nR2bT/(J·mol-1)KT/(L·mg-1)R2288317.80.7720.962347.6187.10.1230.98673.220.220.991298334.50.8240.829361.4196.70.1250.983771.960.2360.98308337.71.480.822366215.720.110.98682.390.9050.993
2.2.6 吸附热力学研究
由表6所示的热力学参数可见,ΔG0为负值,表明Pb2+在硅烷化赤泥表面上的吸附过程是自发的;ΔH0和ΔS0为正值说明该吸附过程为吸热反应。随着温度的升高,ΔG0值降低,表明升温对Pb2+吸附有积极影响,随着反应温度的升高,反应的自发性愈加增强。
表6 硅烷化赤泥吸附Pb2+热力学参数
Table 6 Thermodynamic parameters of Pb2+ adsorption on silanized red mud

T/KΔH0/(KJ·mol-1)ΔS0/(J·mol-1·K-1)ΔG0/(KJ·mol-1)288-4.9298107.3436.8-5.52308-6.04
3 吸附机理分析
3.1 吸附前后SEM表征
为了研究改性后赤泥吸附Pb2+前后的吸附剂表面形貌变化,对吸附前后的样品进行SEM表征,结果如图12所示,EDS元素分析数据列于表7。

图12 硅烷化赤泥吸附Pb2+前后SEM表征
Fig.12 SEM images of silanization red mud before and after adsorbing Pb2+
表7 硅烷化赤泥吸附Pb2+前后EDS元素分析
Table 7 Analysis of EDS elemental of silanization red mud before and after adsorbing Pb2+%

样品w(C)w(N)w(O)w(Si)w(Pb)吸附前赤泥6.9919.7524.646.69—吸附后赤泥7.539.4525.147.418.21
由图12可知:硅烷化赤泥吸附Pb2+前后形貌没有发生明显变化,但是吸附引起硅烷化赤泥吸附剂表面颗粒的团聚现象。表7为EDS面扫数据,改性后赤泥在吸附Pb2+后检测到Pb元素,对比吸附前后样品的元素组成及含量可以看出,对Pb2+的吸附引起N元素的明显降低。分析其原因:1)重金属离子的吸附覆盖了吸附剂中的N,所以吸附剂表面N含量降低;2)N可能为吸附位点,重金属与N成键,降低N元素的检出量。
3.2 吸附前后FT-IR和XPS表征分析
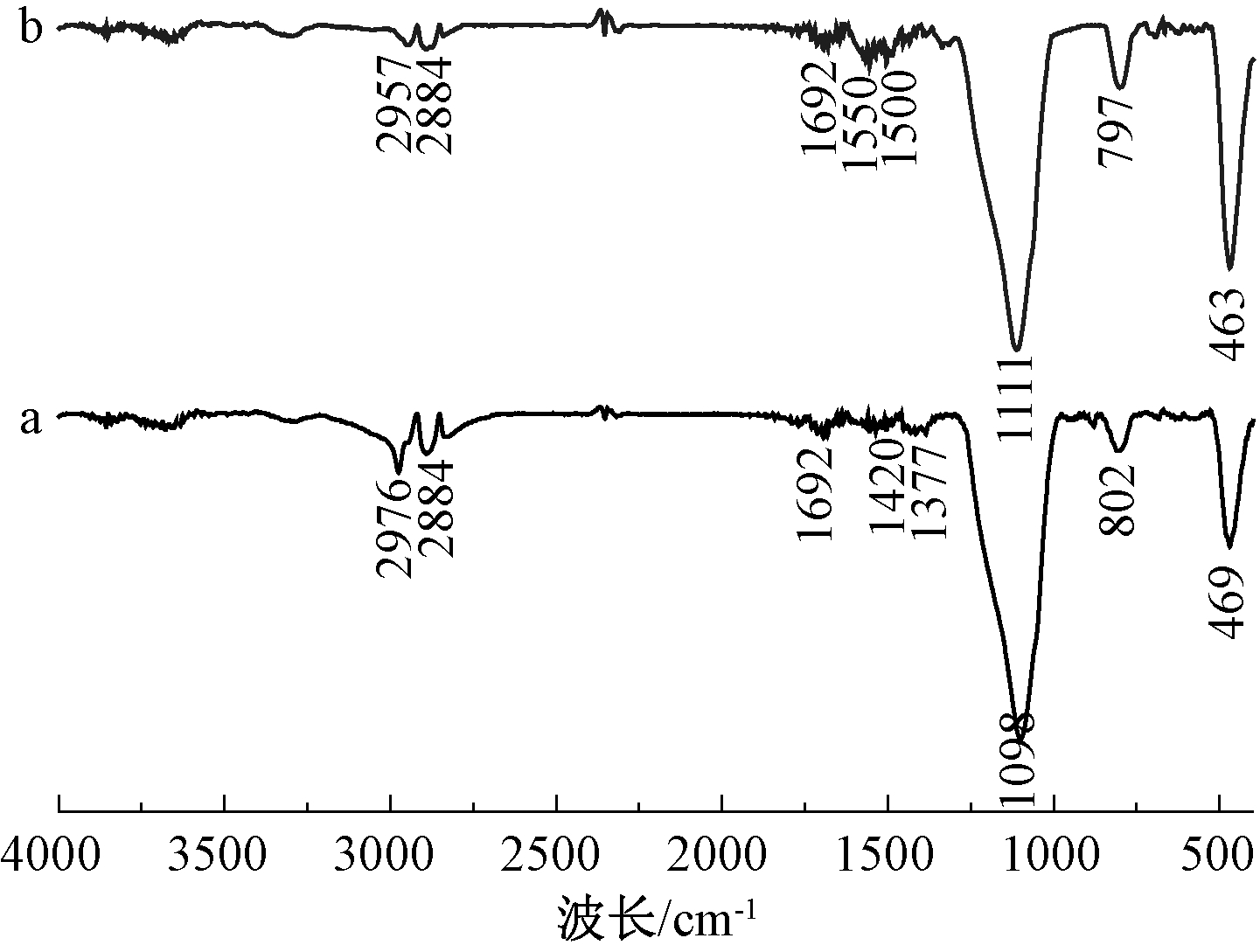
对硅烷化赤泥吸附Pb2+前后的红外谱图进行表征,以研究吸附前后的吸附剂基团变化,FT-IR结果见图13。
a—硅烷化赤泥; b—吸附Pb2+后硅烷化赤泥。
图13 硅烷化赤泥对Pb2+吸附前后样品FT-IR图谱
Fig.13 FT-IR spectrum of silanization red mud before and after adsorbing Pb2+
由图13可看出:硅烷化赤泥吸附Pb2+前后红外图谱发生位移。吸附Pb2+后,氨基(—NH2)的弯曲振动峰由原来的1550 cm-1和1500 cm-1迁移到1420 cm-1和1377 cm-1,这些红外峰的偏移证明氨基上的氮原子可能是Pb2+的主要吸附位点。
XPS通常用于识别吸附物与吸附剂表面官能团的相互作用,因为它们之间产生化学键会改变相应原子周围电子的分布(图14)。由图14a、b可知:吸附后出现了铅元素的XPS的特征峰。图14c、d展示了硅烷化赤泥对Pb2+吸附前后N 1s XPS谱图。图14c表示吸附前硅烷化赤泥的XPS光谱,399.5,400.1 eV处出现的峰归因于—NH2中的氮(—NH—)和![]() 图14d为在吸附Pb2+后,对应于掺杂态—NH—和
图14d为在吸附Pb2+后,对应于掺杂态—NH—和![]() 的N 1s电子结合能均向低频偏移了0.6 eV,说明Pb2+与氨基中的N原子可能发生了较强的化学作用。因此其吸附机理主要是氨基上的氮原子存在的孤对电子可以与Pb2+形成配位键,通过与硅烷化赤泥表面氨基(—NH—和
的N 1s电子结合能均向低频偏移了0.6 eV,说明Pb2+与氨基中的N原子可能发生了较强的化学作用。因此其吸附机理主要是氨基上的氮原子存在的孤对电子可以与Pb2+形成配位键,通过与硅烷化赤泥表面氨基(—NH—和![]() 发生螯合作用来吸附Pb2+,其反应式为[28]:—NH2+Pb2+→—NH2—Pb2+ 或者—NH2—Pb2+—NH2—。
发生螯合作用来吸附Pb2+,其反应式为[28]:—NH2+Pb2+→—NH2—Pb2+ 或者—NH2—Pb2+—NH2—。
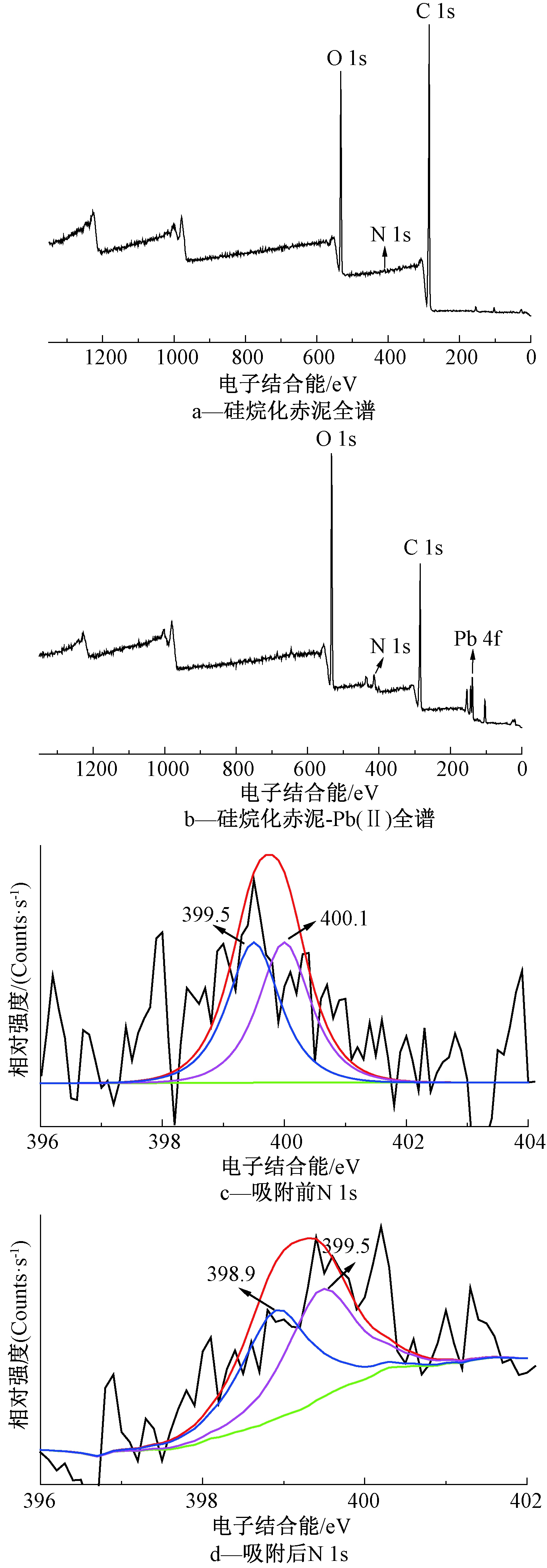
图14 硅烷化赤泥对Pb2+吸附前后的XPS表征结果及各元素分峰
Fig.14 Characterization of XPS of silanization red mud before and after adsorbing Pb2+ and peak of each element
4 结 论
1)通过对合成过程中材料的表征,证明在合成过程中,赤泥表面有一定的—NH2被接枝上。并且经改性后赤泥对Pb2+具有较好的吸附能力。改性的硅烷化赤泥对Pb2+的吸附在80 min达到平衡,其最佳吸附pH为6,最佳吸附剂投加量为2 g/L,饱和吸附量为361 mg/g。
2)溶液pH对硅烷化赤泥的吸附性能有重要影响。随着pH的升高,Pb2+的去除率逐渐升高,当pH≥4时,去除率达到80%以上。由于在pH值较低时氨基发生质子化作用,与同样带正电的Pb2+发生排斥作用,阻碍了吸附剂对Pb2+的吸附,当pH升高,质子化减弱,对重金属离子的静电排斥作用减小,吸附效果明显提升。
3)硅烷化赤泥对Pb2+的吸附过程符合准二级动力学模型以及Freundlich吸附等温模型,说明该吸附属于化学非均质吸附;从热力学参数表明该吸附剂对Pb2+的吸附是吸热、自发过程。
4)经XPS光谱分析证实,吸附机理主要是硅烷化赤泥表面嫁接氨基,氨基上的氮原子存在孤对电子,可通过与Pb2+的螯合作用而有效去除Pb2+。
[1] Srivastava N K, Majumder C B. Novel biofiltration methods for the treatment of heavy metals from industrial wastewater [J]. Journal of Hazardous Materials, 2008, 151(1): 1-8.
[2] 张烨, 王平, 王韬远,等. 钡盐沉积改性硅藻土的制备及其吸附Pb2+的研究 [J]. 环境污染与防治, 2011, 33(11): 49-53.
[3] 杨福欣, 欧维平, 时胜男,等. Dyella ginsengisoli LA-4吸附Cu2+特性及其动力学研究 [J]. 环境污染与防治, 2011, 33(11): 58-62.
[4] Sahu M K, Mandal S, Dash S S, et al. Removal of Pb(Ⅱ) from aqueous solution by acid activated red mud [J]. Journal of Environmental Chemical Engineering, 2013, 1(4): 1315-1324.
[5] Federal-Provincial-Territorial Committee on Drinking Water of the Federal-Provincial-Territorial Committee on Health and the Environment. Health Canada, Guidelines for Canadian Drinking Water Quality[EB/OL].2010. [2019-03-26]. http://www.healthcanada.gc.ca/waterquality.
[6] U.S. EPA.Current Drinking Water Standards[EB/OL]. 2002.[2019-03-26]. http://www.epa.gov/safewater/mcl.
[7] Nurivnlü, Ersoz M. Adsorption characteristics of heavy metal ions onto a low cost biopolymeric sorbent from aqueous solutions[J]. Journal of Hazardous Materials, 2006, 136(2):272-280.
[8] Ajmal M, Rao R A K, Anwar S, et al. Adsorption studies on rice husk: removal and recovery of Cd(Ⅱ) from wastewater[J]. Bioresource Technology, 2003, 86(2):147-149.
[9] Panday K K, Prasad G, Singh V N. Copper(Ⅱ) removal from aqueous solutions by fly ash[J]. Water Research, 1985, 19(7):869-873.
[10] Al-Asheh S, Duvnjak Z. Binary metal sorption by pine bark: study of equilibria and mechanisms[J]. Separation Science and Technology, 1998, 33(9):1303-1329.
[11] Ajmal M, Rao R A K, Anwar S, et al. Adsorption studies on rice husk: removal and recovery of Cd(Ⅱ) from wastewater[J]. Bioresource Technology, 2003, 86(2):147-149.
[12] Panday K K, Prasad G, Singh V N. Copper(Ⅱ) removal from aqueous solutions by fly ash[J]. Water Research, 1985, 19(7):869-873.
[13] Al-Asheh S, Duvnjak Z. Binary metal sorption by pine bark: study of equilibria and mechanisms[J]. Separation Science and Technology, 1998, 33(9):1303-1329.
[14] Bulut Y, Tez Z. Removal of heavy metals from aqueous solution by sawdust adsorption[J]. Journal of Environmental Sciences, 2007, 19(2):160-166.
[15] Bertocchi A F, Ghiani M, Peretti R, et al. Red mud and fly ash for remediation of mine sites contaminated with As, Cd, Cu, Pb and Zn[J]. Journal of Hazardous Materials, 2006, 134(1/2/3):112-119.
[16] Gupta V K, Gupta M, Sharma S. Process development for the removal of lead and chromium from aqueous solutions using red mud-an aluminium industry waste[J]. Water Research, 2001, 35(5):1125-1134.
[17] Cengeloglu Y, Tor A, Ersoz M, et al. Removal of nitrate from aqueous solution by using red mud[J]. Separation and Purification Technology, 2006, 51(3):374-378.
[18] Tor A, Cengeloglu Y, Ersoz M. Increasing the phenol adsorption capacity of neutralized red mud by application of acid activation procedure[J]. Desalination, 2009, 242(1/2/3):19-28.
[19] Tor A, Cengeloglu Y. Removal of congo red from aqueous solution by adsorption onto acid activated red mud[J]. Journal of Hazardous Materials, 2006, 138(2):409-415.
[20] Al-Asheh S, Banat F, Mohai F. Sorption of copper and nickel by spent animal bones[J]. Chemosphere, 1999, 39(12):2087-2096.
![]() A, et al. Removal of lead(Ⅱ) ions from aqueous solutions by adsorption onto pine cone activated carbon[J]. Desalination, 2011, 276(1/2/3):53-59.
A, et al. Removal of lead(Ⅱ) ions from aqueous solutions by adsorption onto pine cone activated carbon[J]. Desalination, 2011, 276(1/2/3):53-59.
[22] Rao M M, Ramesh A, Rao G P C, et al. Removal of copper and cadmium from the aqueous solutions by activated carbon derived from Ceiba pentandra hulls[J]. Journal of Hazardous Materials, 2006, 129(1/2/3):123-129.
[23] 高鹏杰. 氧化铝赤泥改性及对废水中Cr(Ⅵ)的吸附研究[D]. 郑州: 郑州大学, 2016.
[24] Lakshmi N S, Venkatesan G, Vetha P I. Equilibrium studies on removal of lead (Ⅱ) ions from aqueous solution by adsorption using modified red mud[J]. International Journal of Environmental Science and Technology, 2018,15(8):1687-1698.
[25] 石太宏, 吕灿, 左莉娜. 硅烷化改性沸石对重金属离子的吸附性能 [J]. 环境工程学报, 2013, 7(3): 1045-1052.
[26] 王小娟. 赤泥颗粒吸附剂的制备及其对重金属的去除研究[D]. 济南:山东大学, 2013.
[27] Lyu W, Yu T, Feng J T, et al. Highly crystalline polyaniline nanofibers coating with low-cost biomass for easy separation and high efficient removal of anionic dye ARG from aqueous solution [J]. Applied Surface Science, 2018, 458:413-424.
[28] Niu L, Deng S, Yu G, et al. Efficient removal of Cu(Ⅱ), Pb(Ⅱ), Cr(Ⅵ) and As(Ⅴ) from aqueous solution using an aminated resin prepared by surface-initiated atom transfer radical polymerization[J]. Chemical Engineering Journal, 2010, 165(3):751-757.