0 引 言
随着全球工业化进程加快,生产流程产生的工业废水对环境造成的污染日益加剧。苯酚及其化学衍生物是废水中最普遍、最顽固的污染物之一,属于芳香族化合物并对生物体有毒害作用[1-2]。现有的含酚废水处理方法如生物降解和吸附法,无法完全去除水体中的酚类[3]。光催化法作为高级氧化法的一种,具有绿色可持续、低成本优点,利用半导体催化剂实现光催化法是具有前景的研究方向之一。半导体催化剂与光照作用产生羟基自由基(·OH),能够持续地将酚类分解成CO2和H2O,其反应可以被太阳光激活。常用的半导体有氧化锌(ZnO)、二氧化钛(TiO2)、溴氧化铋(BiOBr)、钨酸铋(Bi2WO6)等。Bi2WO6属于Aurivillius型氧化物的一种,是少数能在可见光范围内响应的材料之一,WO6钙钛矿片层具有八面体共顶角联结而成,此结构对光催化性有决定性影响[4]。Tang等[5]报道Bi2WO6能够在可见光下矿化CHCl3和CH3CHO,自此Bi2WO6得到广泛研究,但单体Bi2WO6目前存在两大缺点:纯Bi2WO6吸收波长仅短于约450 nm的可见光,其次带隙较宽(2.8~3.2 eV)导致光生电子和空穴对的快速复合,限制了光能转换效率[6]。掺杂改性可以提高光催化性能,其中与窄隙催化剂复合产生协同效应是研究较多热门课题[7-8]。
二硫化锡(SnS2)作为重要的分层过渡金属硫化物和n型窄隙半导体,已被证明是最有前景的可见光激发的光催化剂之一,具有优异的可见光敏感性、无毒、稳定性强且成本低廉,相比于正常氢电极(NHE),它的导带边缘电位约为-0.9 eV,使其具有强大的光催化还原能力。作为一种窄隙半导体,能够与带隙较宽的Bi2WO6合成复合材料,当受到光照射时,窄隙半导体会首先被激发产生电子,光生电子在电场的作用下容易迁移到Bi2WO6的导带上,增加光生电子与空穴的分离,进而达到提高催化效率的目的。SnS2目前在光催化领域研究还较少[9-10],研究其在光催化领域的应用以及用以改良光催化剂Bi2WO6,开发新型高效的光催化剂复合材料很有必要。
1 实验部分
1.1 试剂及仪器
试剂:五水硝酸铋Bi(NO3)3·5H2O,钨酸钠Na2WO4·2H2O, 乙酸 CH3COOH,乙醇 CH3CH2OH,硫代乙酰胺 CH3CSNH2,去离子水,苯酚C6H5OH,氯化锡SnCl4·5H2O。
仪器:LabX-6000型X射线粉末衍射仪(Shimadzu公司);JSM-5600 LV型扫描电子显微镜(SEM,电子光学公司);JEOL JEM-2100型透射电子显微镜(TEM,电子光学公司);UV-550型紫外可见分光光度计(DRS,JASCO公司);PLS-SXE300氙灯光源(北京泊菲莱公司)带有滤紫外光的滤光片,光强为200 mW/cm2;
1.2 Bi2WO6/SnS2材料的制备
制备Bi2WO6:称取3.92 g Bi3(NO3)2·5H2O(8 mol)溶解于30 mL 5mol/L的CH3COOH水溶液中,1.33 g Na2WO4·2H2O溶解于48 mL去离子水中,将两液混合磁力搅拌6 min,继续搅拌用氨水调节pH至7,移至100 mL反应釜中,200 ℃反应22 h,冷却至室温,清洗后烘干于60 ℃以下。得到干燥粉末放入马弗炉400 ℃煅烧2 h。
复合光催化剂Bi2WO6/SnS2:采用水热法合成。称取5 mmol的SnCl4· 5H2O溶解于2 mL乙酸与38 mL 乙醇混合溶液中,搅拌溶解后加入制备好的Bi2WO6粉末(按照质量比分别加入20%、30%、40%、50%的纯Bi2WO6)。加入完成后进行15 min的超声处理以完全溶解混合药品,再加入10 mmol硫代乙酰胺于上述溶液中,用磁力搅拌器室温搅拌5 h。搅拌完成后将混合溶液放入50 mL高温反应釜中,于180 ℃的条件下的高温加热12 h后自然冷却至室温。高温反应结束后,将样品从反应釜中倒入烧杯,对产物进行过滤。将过滤产物用去离子水和乙醇反复洗涤,洗涤后放入培养箱于80 ℃干燥4 h,得到灰黑色粉末状固体即为Bi2WO6/SnS2。
1.3 Bi2WO6/SnS2材料的表征
SEM:使用扫描电子显微镜观察催化剂样品的微观形貌;XRD:获得材料样品的成分和晶格信息(Cu靶, 扫描范围为10°~80°,扫描速率为2°/min,λ=0.15406 nm);DRS:通过紫外-漫反射光谱分析催化剂的光吸收带边与带隙宽度;PL:分析光催化降解过程中光生电子-空穴对的迁移和重组过程;FT-IR:利用拉曼散射的红外光光谱分析物质组成;XPS:测量光电子的能量,以光电子的动能为横坐标,相对强度(脉冲/s)为纵坐标可得光电子能谱图,从而获得各元素的价态。
1.4 催化剂的活性评价方法
在可见光的照射下降解苯酚溶液,以降解率表征光催化剂活性高低。操作方法如下:称取0.1 g样品溶解于100 mL苯酚溶液中,先在磁力搅拌器中暗反应搅拌1 h达到吸附平衡,然后以500 W氙灯(200 mW/cm2)为光源照射,照射的同时放置磁力搅拌器匀速搅拌,每隔15 min吸取3 mL悬浊液。悬浊液在离心机中离心,设置参数为3000 r/min,取上清液在510 nm处以水为参比测量其吸光度,并记录下数据。
2 结果与讨论
2.1 催化剂的表征
2.1.1 XRD的表征结果及分析
图1为Bi2WO6/SnS2的XRD图。SnS2峰谱与卡片库中 PDF#40-1467号卡片相对应,在2θ为28.199°、32.081°、41.916°、50.020°、52.503°出现了较为明显、尖锐的特征峰,对应晶型为(100)、(101)、(102)、(110)、(111)。根据PDF#73-2020[6]可知,在28.520°、32.089°、46.31°、56.381°的特征峰与Bi2WO6的(113)、(101)、(220)、(200)晶型相对应。SnS2/Bi2WO6原材料的峰形发生一些变化,是由于掺杂物质光催化剂的骨架原子进入了晶格内部,高度分散于表面,特征衍射峰值逐渐减弱[11]。特征衍射峰的降低可归因于Bi2WO6、SnS2的负载,弱化了层间堆积力,这也间接表明Bi2WO6和SnS2成功复合到一起。
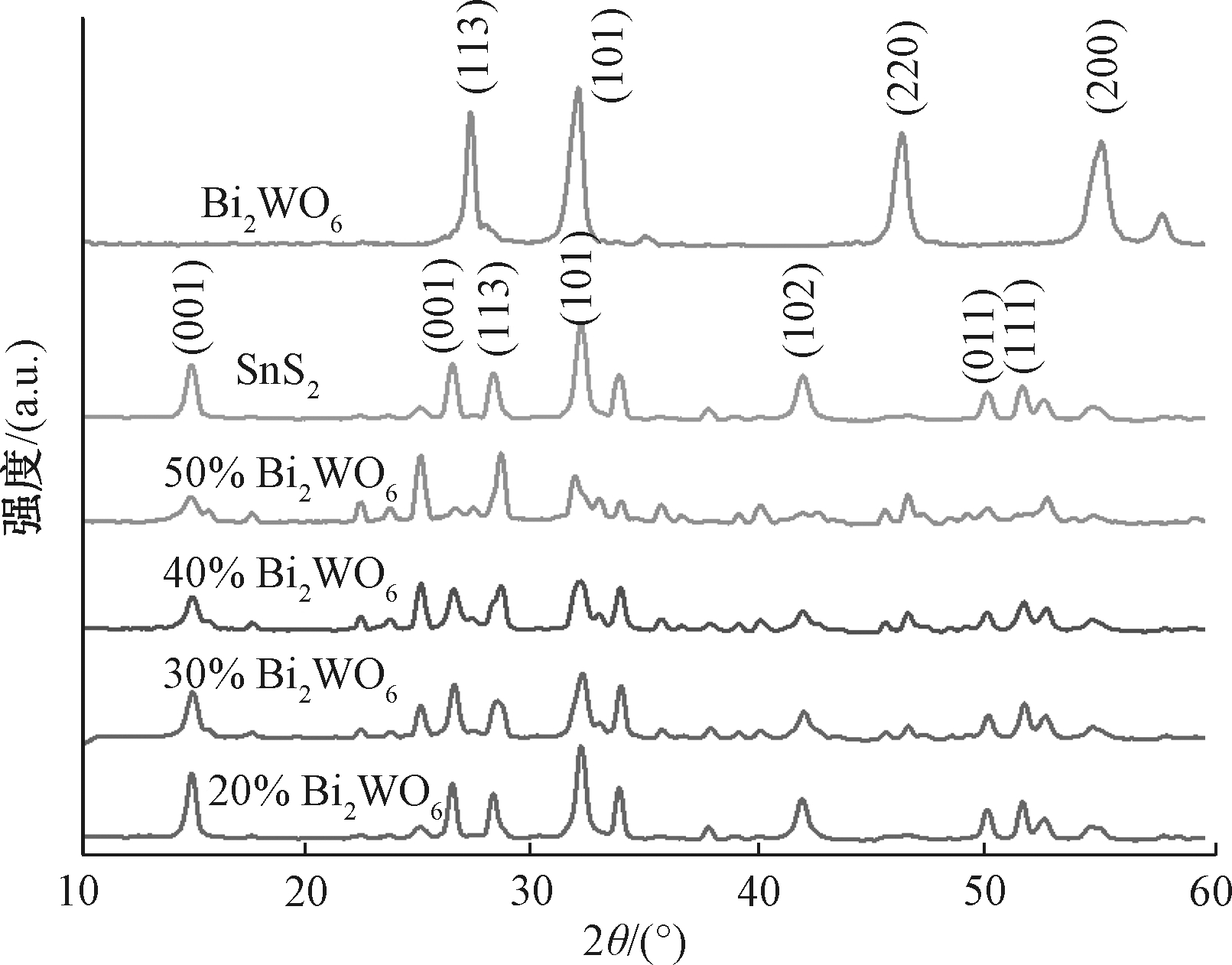
图1 纯Bi2WO6、纯SnS2和不同配比的SnS2/Bi2WO6样品的XRD
Fig.1 XRD patterns of pure Bi2WO6,pure SnS2 and different ratios of SnS2/Bi2WO6 samples
2.1.2 SEM的表征结果及分析
图2为SnS2和50% Bi2WO6/SnS2的SEM图。可知:Bi2WO6为堆积紧密的光滑不规则片状物,粒径为50~200 nm。与SnS2复合后物质发生了团聚现象并且高度分散于SnS2表面,团聚可能是由于干燥箱中空气湿度较大,催化剂干燥过程中内部掺入结晶水,导致团聚现象发生[12]。Bi2WO6高度分散于SnS2表面,可以解释XRD谱图中复合物特征峰位置偏移的现象[13]。细小颗粒状物体附着在SnS2的表面,结合XRD的图像可以分析出,复合样品由Bi2WO6与SnS2组成,Bi2WO6已经成功复合到SnS2上。

图2 Bi2WO6和50% Bi2WO6/SnS2的SEM图
Fig.2 SEM image of SnS2 and 50% Bi2WO6/SnS2
2.1.3 FT-IR的表征结果及分析
图3为Bi2WO6/SnS2的FT-IR光谱图。400~1000 cm-1低波数区间是Bi2WO6特有吸收带,这主要由W—O、Bi—O的伸缩振动以及W—O—W伸缩振动所决定,而最大吸收峰 671 cm-1对应的是WO6八面体中的W—O伸缩振动。1637 cm-1和3462 cm-1对应的吸收峰催化剂表面微量水的存在,引起—OH的伸缩和弯曲振动。对于656 cm-1处,出现了明显的Sn—S伸展振动峰[14-15]。样品的红外光谱峰位置不随Bi2WO6掺杂浓度的改变而发生变化,这也与XRD数据表征结果一致,表明2种物质成功复合。
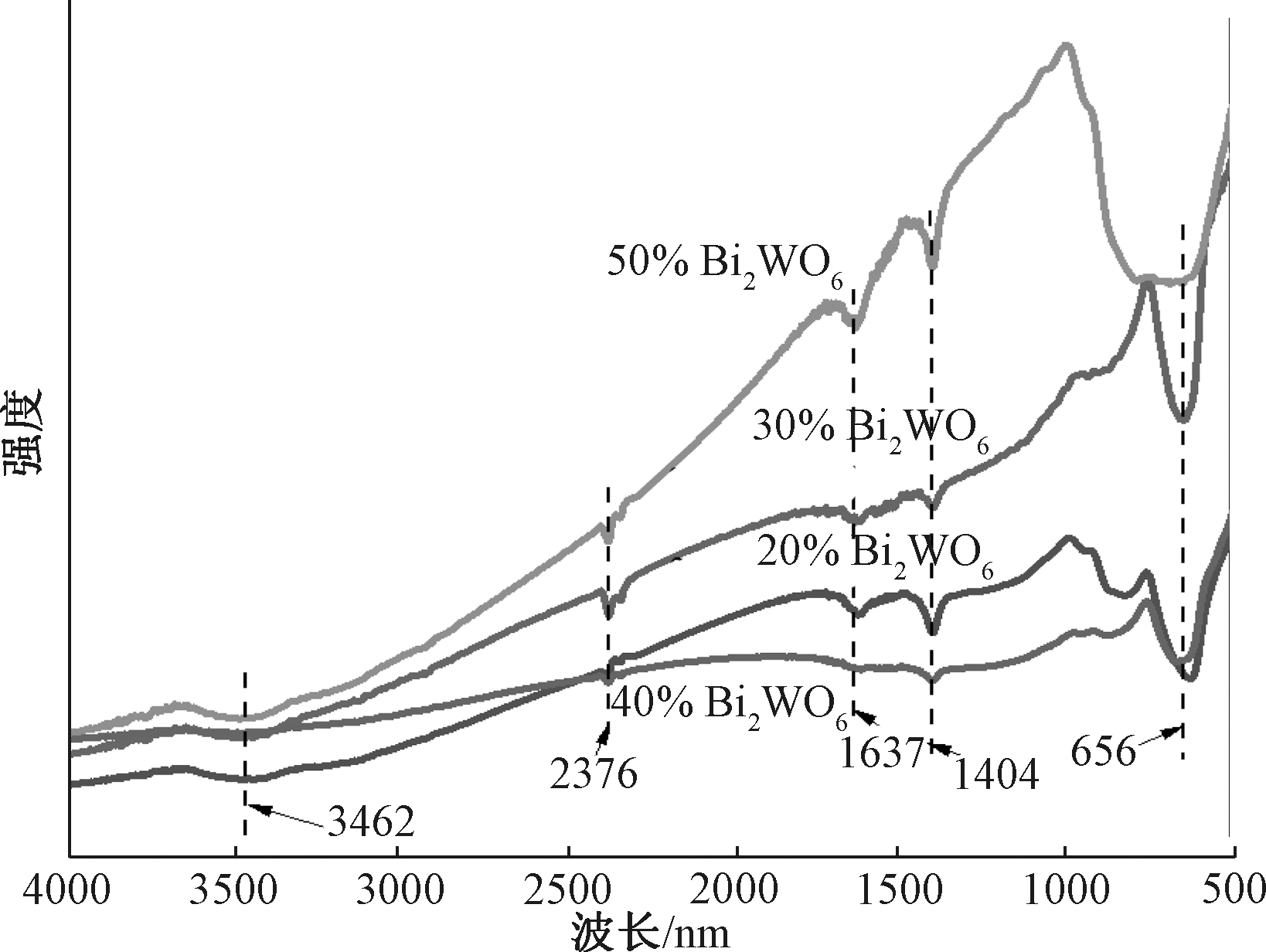
图3 不同配比的Bi2WO6/SnS2的FT-IR光谱
Fig.3 FT-IR spectra of different ratios of Bi2WO6/SnS2
2.1.4 XPS的表征结果及分析
图4为XPS表征Bi2WO6/SnS2谱图。可看出:制备样品中无其他杂质元素的干扰,图4b是Bi 4f区域的XPS光谱图,在155.6 eV出现了明显的特征峰,Bi以+3价态存在,与预期价态相符合[16]。W 4f图谱中33.0 eV与35.4 eV处的峰可以证明W以+6价态存在[17]。
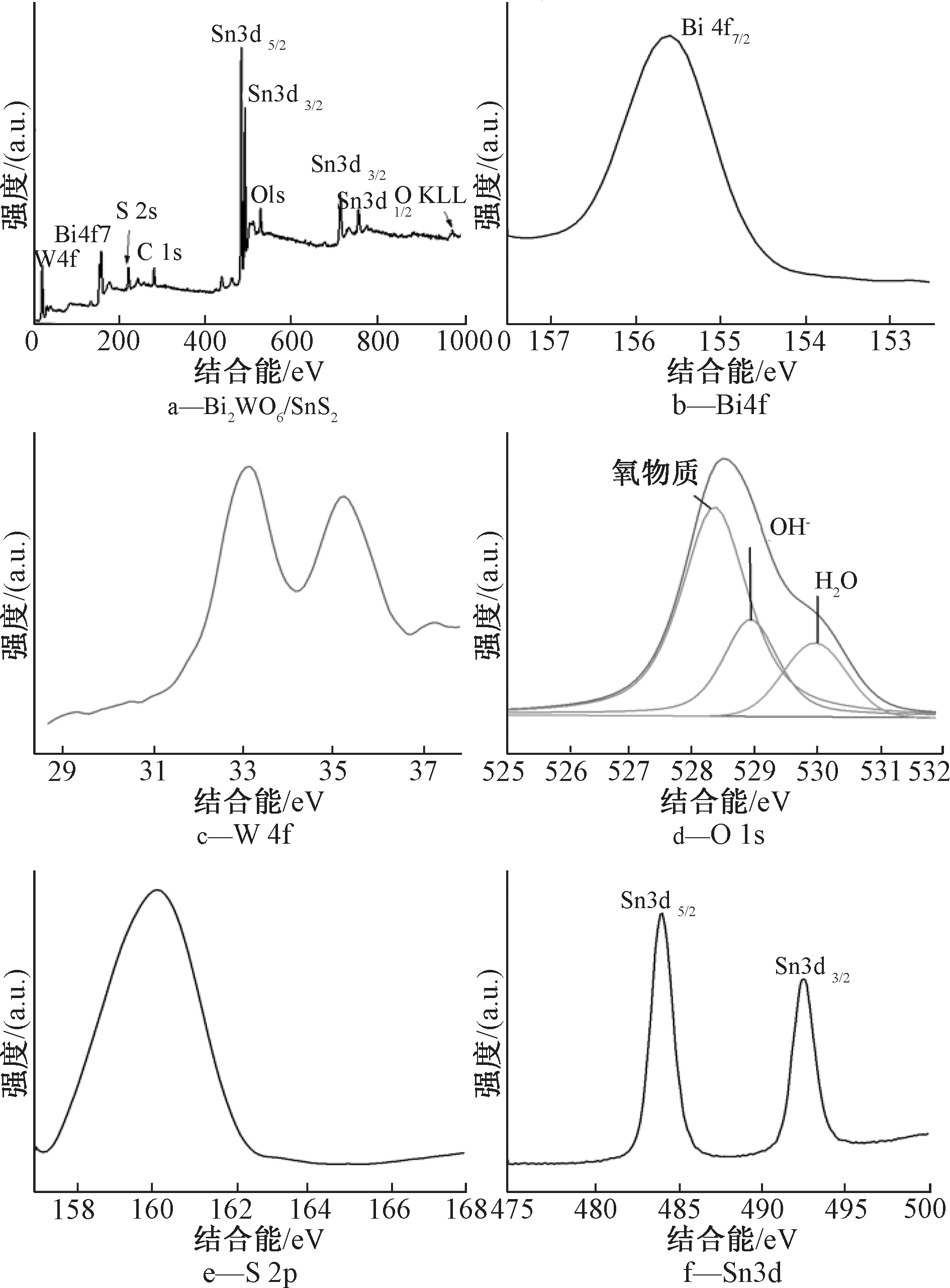
图4 Bi2WO6/SnS2、Bi 4f 、W 4f、O 1s 、S 2p、Sn 3d的XPS光谱图
Fig.4 XPS spectra of Bi2WO6/SnS2、Bi 4f、W 4f、O 1s、S 2p、Sn 3d、
图4d为样品O1s区域的XPS光谱,可以拟合成3个峰,分别为晶格氧中的氧528.7 eV、化学吸附水(H2O)530.1 eV和羟基(—OH)529.0 eV[18]。对应于图4e、4f分别为S 2p、Sn 3d的XPS光谱,S以S2-形式存在于化合物中,因为在图4e中160.4 eV处存在明显的对称峰;Sn 3d谱图中484.6 eV和493.4 eV的峰对应于Sn 3d5/2和Sn 3d3/2,这表明Sn以+4价态存在[19]。XPS谱图得到的结果与XRD分析的结果相匹配,证明Bi2WO6与SnS2已经成功复合。
2.1.5 DRS的表征结果及分析
图5为Bi2WO6/SnS2的DRS光谱图。可知:在400~550 nm可见光区域内出现了明显的吸收带边。纯Bi2WO6在UV区域存在强吸收,切线与X轴在430 nm处相交,在波长<430 nm有明显的吸收,但在>430 nm波段的可见光中无吸收;而SnS2在UV光和可见光中显示出强吸收,这归因于Bi2WO6带隙较宽,而SnS2带隙较窄,所以电子更容易发生跃迁,材料复合后Bi2WO6/SnS2在可见光区域的吸收更宽更强,与纯Bi2WO6相比,可观察到明显红移。该结果表明:对比纯Bi2WO6,Bi2WO6/SnS复合材料可以更有效地吸收和利用可见光。从Kubelka-Munk(式(1))可计算不同配比Bi2WO6/SnS2的禁带宽度[20]:
αhν=(hv-Eg)n
(1)
式中:α为吸收系数;hv为光电子能量;Eg为禁带宽度。以hv为横坐标,以(αhv)2为纵坐标,将所得曲线直线部分延长至与横坐标相交,即为禁带宽度。SnS2、30% Bi2WO6/SnS2、40% Bi2WO6/SnS2、50% Bi2WO6/SnS2、Bi2WO6的带隙宽度分别为1.96,2.52,2.36,2.01,2.90 eV。Bi2WO6/SnS2的带隙能量低于纯Bi2WO6,但高于纯SnS2,复合材料可以更有效地利用太阳能。
2.2 光催化性能评价与机理分析
2.2.1 降解苯酚实验的分析
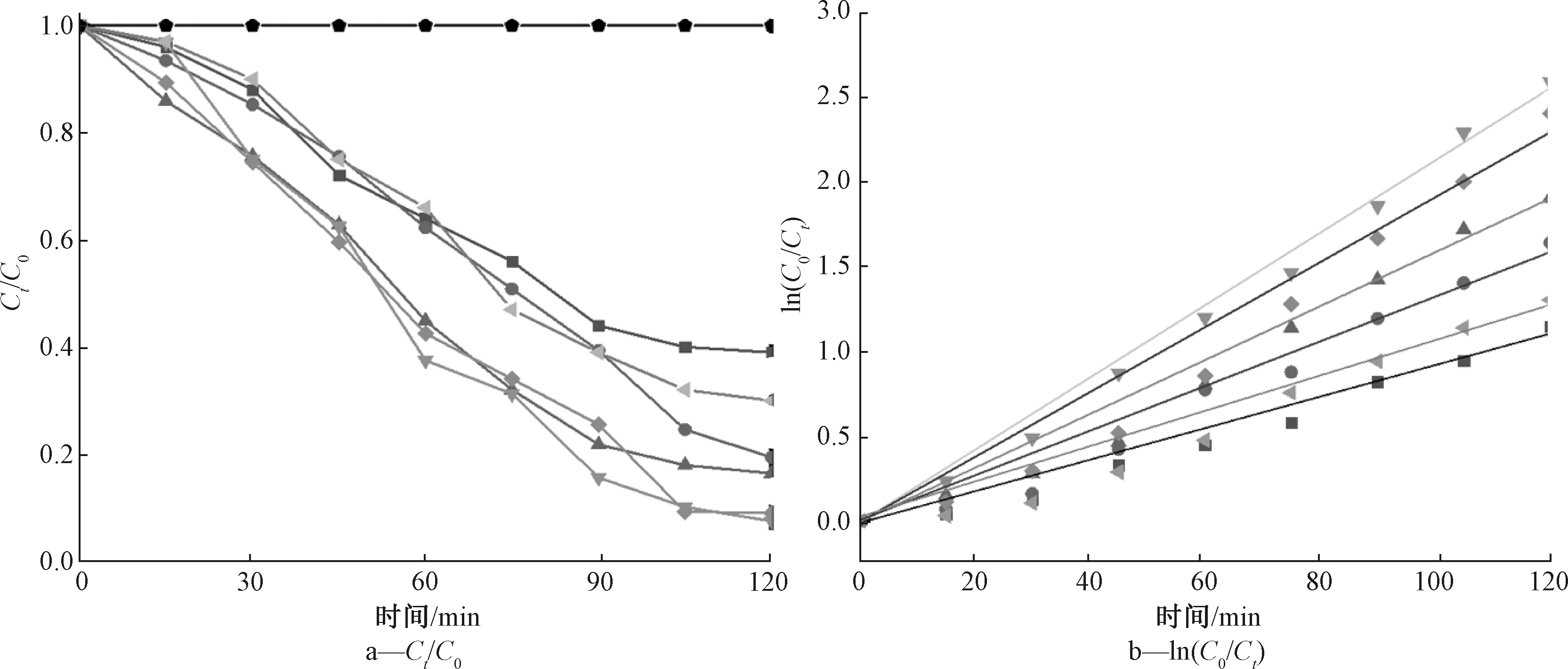
在可见光照射(λ>420 nm)下,不同质量比的光催化剂Bi2WO6/SnS2对苯酚的降解率曲线如图6a所示。空白实验表明:苯酚在无催化剂的情况下不会脱色,纯Bi2WO6和纯SnS2均表现出光催化性,氙灯照射120 min后脱色率为61%和70%,而复合材料的脱色在可见光照射下显著增加,表明Bi2WO6/SnS2有优异的光催化活性,脱色率分别为81.7%、85.6%、92.5%、91.0%,其中40% Bi2WO6的苯酚脱色效率最高,120 min降解率达到92.5%,但50% Bi2WO6的脱色率开始降低。
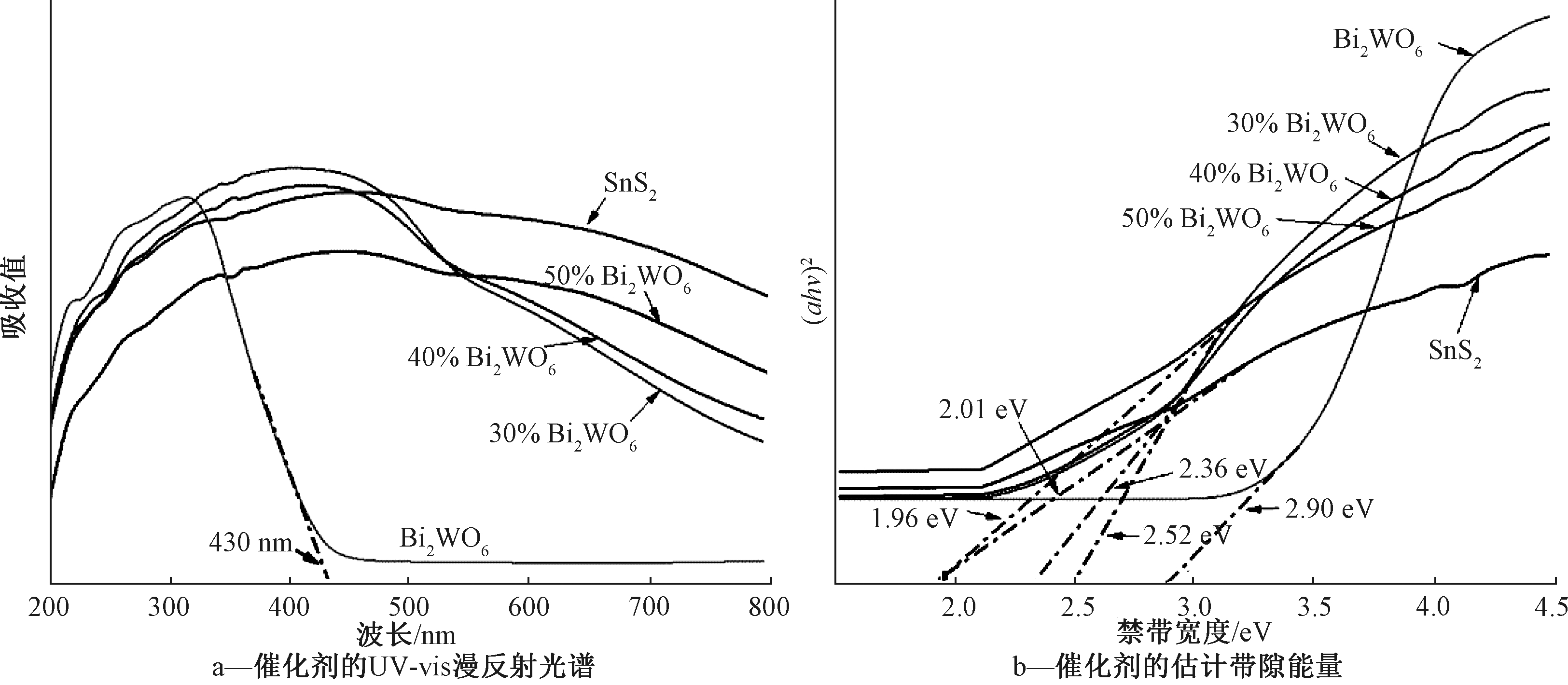
图5 UV-vis漫反射光谱:纯Bi2WO6、纯SnS2和不同配比的SnS2/Bi2WO6估计带隙能量
Fig.5 UV-vis diffuse reflectance spectra and estimated band gap energies of Bi2WO6, SnS2, and Bi2WO6/SnS2
![]() —Bi2WO6;
—Bi2WO6;![]() —20% Bi2WO6;
—20% Bi2WO6;![]() —30% Bi2WO6;
—30% Bi2WO6;![]() —40% Bi2WO6;
—40% Bi2WO6;![]() —50% Bi2WO6;
—50% Bi2WO6;![]() —SnS2;
—SnS2;![]() —苯酚。
—苯酚。
图6 不同催化剂光催化降解苯酚的Ct/C0和降解苯酚的ln(C0/Ct)的动力学
Fig.6 Kinetic diagram of C0/Ct and ln(C0/Ct)of photocatalytic degradation of phenol
苯酚脱色符合一级动力学方程ln(C0/Ct)=kapp,kapp为动力学速率常数,h-1;C0和Ct为苯酚初始浓度和实时浓度,mg/L。从线性回归的斜率可计算出Bi2WO6、SnS2、20% Bi2WO6/SnS2、30% Bi2WO6/SnS2、40% Bi2WO6/SnS2、50% Bi2WO6/SnS2的速率常数分别为0.446,0.475,0.773,0.801,1.19,0.854 h-1。其中,40% Bi2WO6/SnS2速率常数最高,为1.19 h-1,是纯Bi2WO6的2.66倍,SnS2的2.5倍。光催化效率的提高主要是因为加入了窄隙半导体,调节了晶体结构和能带结构,增加了电子-空穴的分离,但是随着Bi2WO6掺杂比例的增加,苯酚的脱色率出现了降低。
为了更好地研究光催化降解过程中光生电子-空穴对的迁移和重组过程,在室温下以382 nm的激发波长测量所制备样品的光致发光(PL)谱,如图7所示。光催化过程中激发的空穴和电子重组次数越多,光催化活性越低。纯Bi2WO6在382 nm处显示出强而宽的峰,这意味着电荷载体的快速复合。

图7 在380 nm激发光下纯Bi2WO6、20% Bi2WO6/SnS2、30% Bi2WO6/SnS2、40% Bi2WO6/SnS2和50% Bi2WO6/SnS2的PL光谱
Fig.7 PL spectra of pure Bi2WO6, 20% Bi2WO6/SnS2, 30% Bi2WO6/SnS2, 40% Bi2WO6/SnS2 and 50% Bi2WO6/SnS2 at 380 nm excitation
纯SnS2比复合Bi2WO6/SnS2强度低,但复合材料Bi2WO6/SnS2 PL强度更低,这可归因于Bi2WO6和SnS2之间的电子跃迁,Bi2WO6和SnS2的异质结构有助于抑制光诱导电子的组合。40% Bi2WO6/SnS2的PL强度最低,这清楚地表明该配比最有利抑制电子-空穴复合过程,实现苯酚的高降解率[21-22]。
根据表征数据,Bi2WO6/SnS2可促进光催化活性也可归因于以下2个因素:1)SnS2比Bi2WO6具有更窄的带隙,可以更有效地利用太阳能吸收光子并提供各种激发位置。2)SnS2片状结构和表面附着的Bi2WO6可提供相当大的接触面积,用于光激发电子和空穴的有效转移和分离。SnS2和Bi2WO6复合光催化剂将在改善电荷分离和延长其寿命方面发挥重要作用,提高复合材料的光催化性能[23]。
通常,2个半导体导带之间的差异越大,电子注入的驱动力就越高。光致电子和空穴的迁移方向和有效分离取决于各个半导体的带隙位置。半导体的CB和价带VB的位置可通过Mulliken公式确定[24]:
ECB=X-Ee+0.5Eg
(2)
EVB=ECB-Eg
(3)
式中: X为半导体的电负性;Ee为氢标度上的自由电子能量(Ee=4.5 eV);Eg为半导体带隙能量。Mulliken方程用于确定平带电位。EVB和ECB分别为VB和CB的边缘电位值。
由式 (1)—(3),结合DRS谱图计算带隙能,可以得出:Bi2WO6的ECB=-0.14 eV,EVB=2.76 eV;SnS2 的EVB=-0.815 eV,ECB=1.145 eV。由此可绘制机理图,SnS2(-0.815 eV)的ECB、EVB低于Bi2WO6(-0.14 eV)[24]。当照射可见光时,SnS2和Bi2WO6都被激发产生电子-空穴对[25],SnS2价带与Bi2WO6的导带之间形成了一种新的光生电子迁移路径[26,27]。
2.2.2 光催化机理分析
图8为Bi2WO6和SnS2价带与导带。SnS2的导带负于Bi2WO6的导带,因此,当SnS2被可见光激发时,光诱导电子从SnS2的价带转移到Bi2WO6,而空穴则停留在SnS2的导带中,符合Z型光催化剂特点。因此,Z型光催化剂的光诱导电子和空穴在转移过程中容易分离,从而提高了光催化剂对苯酚降解的性能,阻碍了电子空穴对的复合,这与PL结果是一致的。电子迁移到催化剂表面,具有还原性,可与水和氧气发生反应,生成羟基自由基和超氧自由基。由于电子迁移,Bi2WO6上VB价带的强氧化性空穴可直接将苯酚降解[28]。由于SnS2的价带电位低于O2电位,因此,SnS2价带上积累的电子可以直接将O2还原为污染物降解的强氧化剂![]()
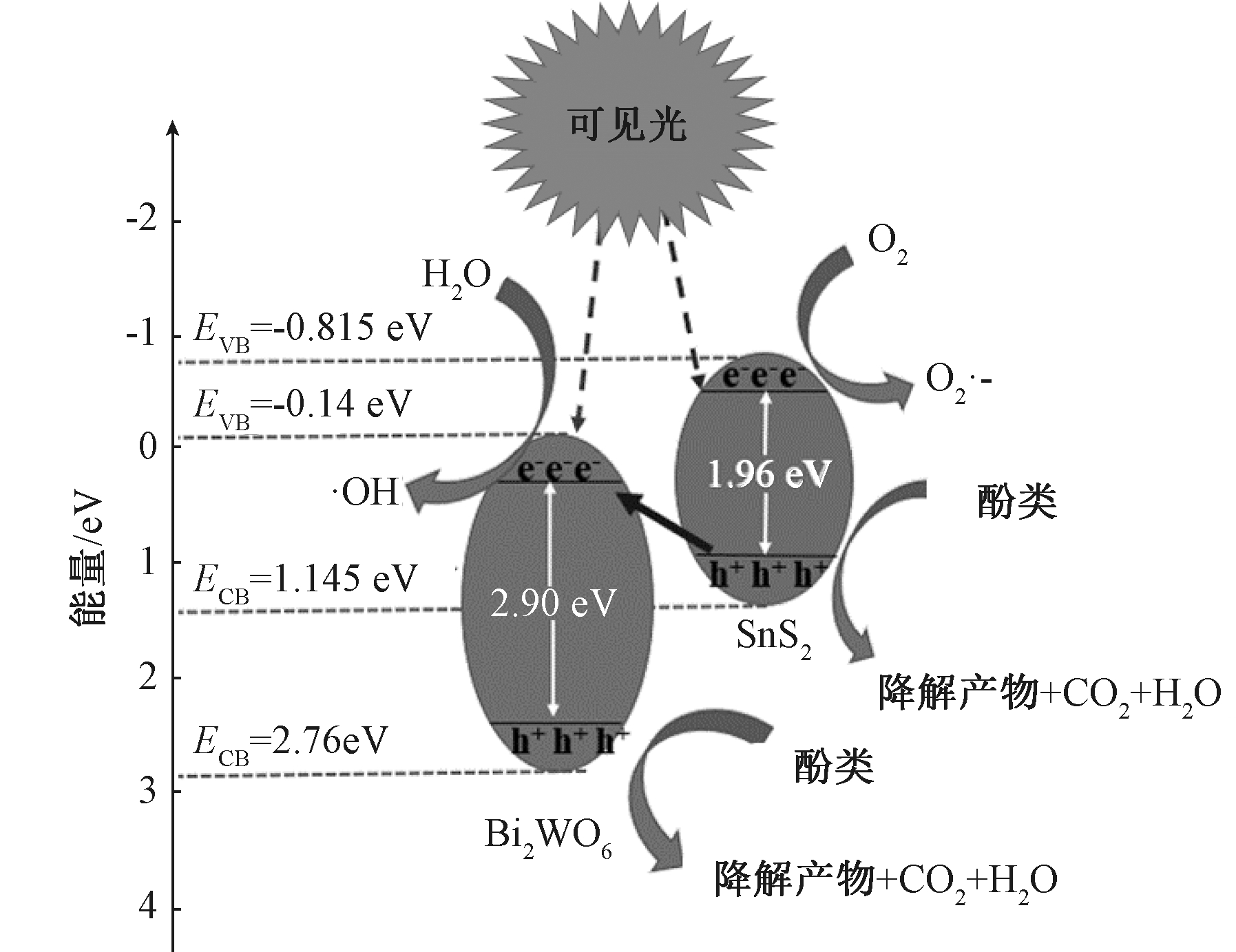
图8 可见光照射下Bi2WO6/SnS2处理污染物的机理
Fig.8 Mechanism diagram of Bi2WO6/SnS2 treatment of pollutants under visible light irradiation
3 结 论
1)采用简便绿色的水热法开发了一系列Z型Bi2WO6/SnS2催化剂。通过水热法将Bi2WO6颗粒状均匀地分散在SnS2片层上。
2)在可见光照射下,Bi2WO6/SnS2复合材料比纯SnS2和Bi2WO6具有更好的光催化活性。其中,质量比为40%的Bi2WO6/SnS2复合材料表现出最佳的光催化活性:苯酚120 min的降解率达到92.5%;通过一级动力学方程可知:40%Bi2WO6/SnS2速率常数是纯Bi2WO6的2.66倍,是纯SnS2的2.5倍。
3)光催化活性的改善归因于SnS2和Bi2WO6之间的带隙结构,宽窄带隙的结合降低了光生电子和空穴复合速率,Z型结构改善了SnS2和Bi2WO6复合材料中电子空穴对的分离,有助于提高光催化活性。该结果为高效可见光光催化剂的设计和开发提供了简便绿色的方法。
[1] Tong H, Ouyang S X, Bi Y P, et al.Nano-photocatalytic materials: possibilities and challenges[J].Advanced Materials, 2012, 24(2):229-251.
[2] Liu Y P, Fang L, Lu H P, et al.Highly efficient and stable Ag/Ag3PO4, plasmonic photocatalyst in visible light[J].Catalysis Communications, 2012, 17(1):200-204.
[3] Qian X F, Yue D J, Tian Z Y, et al.Carbon quantum dots decorated Bi2WO6, nanocomposite with enhanced photocatalytic oxidation activity for VOCs[J].Applied Catalysis B:Environmental, 2016, 193:16-21.
[4] Tang L, Wang J J, Zeng G M, et al.Enhanced photocatalytic degradation of norfloxacin in aqueous Bi2WO6 dispersions containing nonionic surfactant under visible light irradiation[J].Journal of Hazardous Materials, 2016, 306:295-304.
[5] Tang J W, Zou Z G, Ye J H.Photocatalytic decomposition of organic contaminants by Bi2WO6 under visible light irradiation[J].Catalysis Letters, 2004, 92(1/2):53-56.
[6] Kadeer K, Tursun Y, Dilinuer T, et al.Sonochemical preparation and photocatalytic properties of CdS QDs/Bi2WO6 3D heterojunction[J].Ceramics International, 2018.
[7] Yu S X, Zhang Y H, Li M, et al.Non-noble metal Bi deposition by utilizing Bi2WO6 as the self-sacrificing template for enhancing visible light photocatalytic activity[J].Applied Surface Science, 2017, 391:491-498.
[8] Huang H W, Liu K, Chen K, et al.Ce and F comodification on the crystal structure and enhanced photocatalytic activity of Bi2WO6 photocatalyst under visible light irradiation[J].The Journal of physical Chemistry C, 2014, 118(26):14379-14387.
[9] Ge L, Han C C, Liu J.Novel visible light-induced g-C3N4/Bi2WO6 composite photocatalysts for efficient degradation of methyl orange[J].Applied Catalysis B:Environmental, 2011, 108/109(none):100-107.
[10] Ge M, Li Y F, Liu L, et al.Bi2O3-Bi2WO6 composite microspheres: hydrothermal synthesis and photocatalytic performances[J].The Journal of Physical Chemistry C, 2011, 115(13):5220-5225.
[11] He M, Yuan L X, Huang Y H.Acetylene black incorporated three-dimensional porous SnS2 nanoflowers with high performance for lithium storage[J].RSC Advances, 2013, 3(10):3374-3383.
[12] 崔洪梅, 刘宏, 王继扬,等.纳米粉体的团聚与分散[J].机械工程材料, 2004, 28(8):38-41.
[13] Zou Y Q, Wang Y.Microwave solvothermal synthesis of flower-like SnS2 and SnO2 nanostructures as high-rate anodes for lithium ion batteries[J].Chemical Engineering Journal, 2013, 229(4):183-189.
[14] Kiruthigaa G, Manoharan C, Raju C, et al.Solid state synthesis and spectral investigations of nanostructure SnS2[J].Spectrochimica Acta Part A Molecular & Biomolecular Spectroscopy, 2014, 129(129):415-420.
[15] Jing L Q, Xu Y G, Chen Z G, et al.Different morphologies of snS2 Supported on 2D g-C3N4 for excellent and stable visible light photocatalytic hydrogen generation[J].ACS Sustainable Chemistry & Engineering, 2018, 6(4):5132-5141.
[16] Xiao Q, Zhang J, Xiao C, et al.Photocatalytic degradation of methylene blue over Co3O4/Bi2WO6 composite under visible light irradiation[J].Catalysis Communications, 2008, 9(6):1247-1253.
[17] Guo S, Li X F, Wang H Q, et al.Fe-ions modified mesoporous Bi2WO6 nanosheets with high visible light photocatalytic activity[J].Journal of Colloid & Interface Science, 2012, 369(1):373-380.
[18] Yu J G, Wang G H, Cheng B, et al.Effects of hydrothermal temperature and time on the photocatalytic activity and microstructures of bimodal mesoporous TiO2 powders[J].Applied Catalysis B: Environmental, 2007, 69(3/4):171-180.
[19] Zhao W H, Wei Z Q, Zhang L, et al.Cr doped SnS2 nanoflowers: preparation, characterization and photocatalytic decolorization[J].Materials Science in Semiconductor Processing, 2018, 88:173-180.
[20] Fakhri A, Behrouz S, Pourmand M.Synthesis, photocatalytic and antimicrobial properties of SnO2, SnS2 and SnO2/SnS2 nanostructure[J].Journal of Photochemistry & Photobiology B Biology, 2015, 149:45-50.
[21] Liu X, Zhou M, Yao G, et al.Hydrothermal synthesis and enhanced visible-light photocatalytic activity of octahedral Bi2WO6 modified with CdSe quantum dots[J].RSC Advances, 2014, 4(35):18264-18269.
[22] Li J Z, Yu K, Tan Y H, et al.Facile synthesis of novel MoS2@SnO2 hetero-nanoflowers and enhanced photocatalysis and field-emission properties[J].Dalton Transactions, 2014, 43(34):13136-13144.
[23] Wang L N, Ma Y, Yang M, et al.One-pot synthesis of 3D flower-like heterostructured SnS2/MoS2 for enhanced supercapacitor behavior[J].RSC Advances, 2015, 5(108):89069-89075.
[24] Zhou X L, Zhou T E, Hu J C, et al.Controlled strategy to synthesize SnO2 decorated SnS2 nanosheets with enhanced visible light photocatalytic activity[J].Cryst Eng Comm, 2012, 14(17):5627-5633.
[25] Fakhri A, Kahi D S.Synthesis and characterization of MnS2/reduced graphene oxide nanohybrids for with photocatalytic and antibacterial activity[J].Journal of Photochemistry & Photobiology B:Biology, 2017, 166:259-263.
[26] Ke J, Duan X G, Luo S, et al.UV-assisted construction of 3D hierarchical rGO/Bi2MoO6 composites for enhanced photocatalytic water oxidation[J].Chemical Engineering Journal, 2017, 313:1447-1453.
[27] Huang H W, Liu L Y, Zhang Y H, et al.One pot hydrothermal synthesis of a novel BiIO4/Bi2MoO6, heterojunction photocatalyst with enhanced visible-light-driven photocatalytic activity for rhodamine B degradation and photocurrent generation[J].Journal of Auoys and compounds Characterization, 2015, 6(9):807-811.
[28] Lu X Y, Che W J, Hu X F, et al.The facile fabrication of novel visible-light-driven Z-scheme CuInS2/Bi2WO6 heterojunction with intimate interface contact by in situ hydrothermal growth strategy for extraordinary photocatalytic performance[J].Chemical Engineering Journal, 2018:DOI:10.1016/j.cej.2018.09.087.