0 引 言
在污水处理厂二沉池和深度处理单元等构筑物中,藻类会利用水中的氮、磷及其他无机盐进行光合作用,大量繁殖,并黏附、生长在出水堰、深度处理的斜管或斜板等位置。目前,污水处理厂主要采取人工清捞、机械洗刷等方式清理黏附藻类,然而人工清捞清理效率低,机械洗刷则可能使构筑物表面粗糙度增大,进一步加重藻类污染现象,现有措施未能使藻类黏附生长问题得到有效解决。因此,研发高效抑制藻类黏附与生长技术对于维持污水处理构筑物的稳定运行具有重要意义,也是污水处理厂运行优化的迫切需求。
季铵盐(quaternary ammonium compounds, QAC)已应用于消毒领域50余年[1],具有优良的抑菌杀菌性能,而QAC与涂料技术的结合亦逐渐成为季铵盐应用研究的前沿热点。大量研究成果表明:涂覆了含QAC涂层的表面对多种微生物均有抑制和杀灭作用,包括革兰氏阳性革兰氏阴性细菌、酵母菌、霉菌等[1-5]。QAC改性涂层表面具有较高的正电荷密度,可与带负电荷的微生物细胞存在较强的静电作用,因此当微生物细胞吸附在QAC改性涂层表面时,QAC会破坏微生物细胞膜,引发微生物生理功能紊乱(如K+和H+的外泄),进而导致微生物死亡[6-8]。
基于已有研究的启发,本文采用水处理设施常用的环氧树脂涂料作为基体材料,利用共混方法将QAC与环氧树脂涂料进行复合,得到QAC/环氧树脂复合涂层,同时探究QAC投加量对QAC/环氧树脂复合涂层基本性能和抑藻性能的影响,为污水处理厂构筑物抗藻生长及黏附提供新的解决思路和参考。
1 实验部分
1.1 材料与试剂
环氧底漆购自上海环材实业有限公司;十二烷基二甲基苄基氯化铵(DDBAC),质量分数≥99.0%,Sigma-Aldrich;乙醇,质量分数≥99.5%,Sigma-Aldrich;普通小球藻(Chlorella vulgaris),中国科学院水生生物研究所。
1.2 仪器设备
X射线光电子能谱分析仪(XPS),Thermo ESCALAB 250XI;傅里叶变换衰减全反射红外光谱(ATR-FTIR),Thermo Nicolet 5700;原子力显微镜(AFM),Bruker Multimode Ⅳ;接触角测量仪,OCA 15 Plus;固体表面Zeta电位分析仪,SurPASS3;真空干燥箱,DZF-6050;共聚焦激光扫描显微镜(CLSM),Nikon A1。
1.3 涂层的制备
实验采用DDBAC作为模型季铵盐(QAC),其结构式如图1所示。
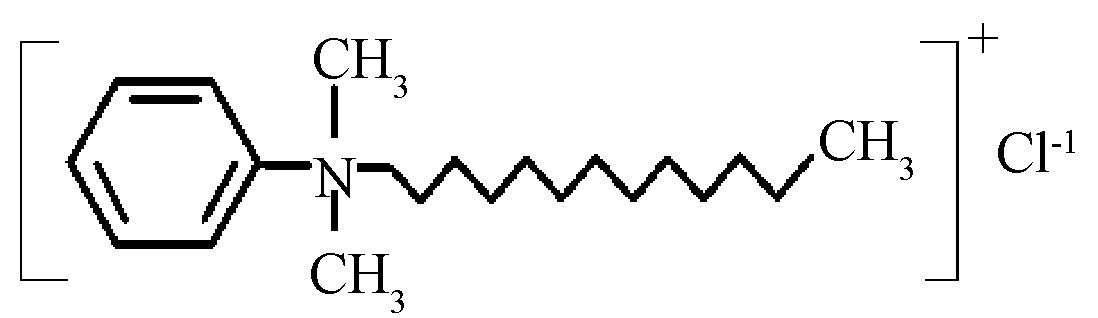
图1 DDBAC分子结构式
Figure 1 Molecular structure of DDBAC
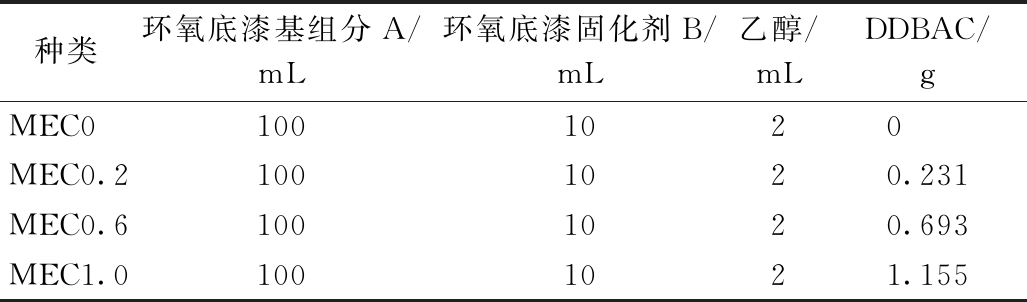
购置的环氧底漆含基本组分A和固化剂B,采用共混方法制备QAC/环氧树脂复合涂层,具体方法如下:于2 mL无水乙醇中加入适量DDBAC后超声溶解、分散30 min,在磁力搅拌(1200 r/min)条件下缓慢滴加上述溶液至100 mL环氧底漆基本组分A(密度为1.05 g/mL)中,室温搅拌(1200 r/min)60 min。然后缓慢加入10 mL环氧底漆固化剂B,磁力搅拌(1200 r/min)5 min后,超声10 min 以去除QAC乙醇溶液-环氧底漆基本组分A-固化剂B体系中的气泡,静置1 min使体系中的各成分反应完全。最后采用刷涂法将QAC/环氧树脂复合油漆涂于不锈钢上,室温干燥12 h后,再于40 ℃条件下真空干燥12 h以保证溶剂完全挥发。表1为不同质量分数QAC的QAC/环氧树脂复合涂层的配方。
表1 各涂层样品配方
Table 1 Composition of different coatings
种类环氧底漆基组分A/mL环氧底漆固化剂B/mL乙醇/mLDDBAC/gMEC01001020 MEC0.21001020.231MEC0.61001020.693MEC1.01001021.155
1.4 涂层的表征及性能测试
1)表面元素含量测试:采用X射线光电子能谱(XPS)测定涂层表面元素含量,测定过程中以Al Kα(hv=1486.6 eV)为射线源,能谱范围为0~1201 eV。扫描结果用碳峰校正(hv=284.6 eV),所有特征谱图元素高斯峰等半宽维持稳定。
2)表面官能团分析:采用傅里叶变换衰减全反射红外光谱(ATR-FTIR)分析涂层表面的官能团组成,ATR-FTIR扫描分辨率为4 cm-1,扫描范围为4000~500 cm-1。
3)粗糙度测试:通过原子力显微镜(AFM)对涂层粗糙度进行测试,选用平均粗糙度(Ra)、表面均方根粗糙度(Rq)和最大粗糙度(Rmax)对涂层粗糙度进行表征,每个样品测试3次后取平均值。
4)表面接触角:采用接触角测量仪测量室温下涂层表面亲水性接触角以反映涂层的亲疏水性,每个样品测量7次取平均值[9]。
5)表面Zeta电位:采用固体表面Zeta电位分析仪测试涂层表面Zeta电位,测试选用KCl溶液(10 mol)作为测量介质,并用NaOH(1 mol)和盐酸(1 mol)将溶液pH调至7,每个样品测试3次后取平均值。
6)耐水性:实验采用5 cm2的样品测试涂层耐水性。首先测量样品质量(M0),然后将其浸泡在50 mL的纯水中30 d,用镊子取出并用滤纸吸干样品表面的水分,测量此时样品质量(Ms);再将样品置于40 ℃真空干燥箱中进行干燥,直至样品质量不再变化,称量其质量(Mf)。涂层样品的吸水率(Ws)和失重率(Wl)的计算如式(1)—(2)所示[10, 11]:
![]()
(1)
![]()
(2)
7)污染实验:样品在污染实验前经紫外杀菌30 min,测试使用的玻璃器皿在实验前均使用高温高压灭菌。将涂层样品(1.1 cm2)放入装有2 mL小球藻悬浮液(107 cells/mL)的多孔板中,在25 ℃光照培养箱中,光照/黑暗比为12 h/12 h的培养条件下培养7 d,取出涂层,用PBS溶液漂洗去除表面未黏附的小球藻后进行如下操作:①将样品置于1 mL PBS 溶液中,超声10 min将表面黏附/生长的小球藻脱落下来;取出涂层样品,获得含有涂层表面黏附/生长小球藻的悬浮液,测试藻液的OD680值,以表征样品表面黏附/生长藻细胞数量。②采用激光共聚焦显微镜(CLSM)观察样品表面的叶绿素自发荧光,以表征样品表面黏附/生长的藻细胞分布[12,13]。同时,利用ImageJ软件对从CLSM测试中获得的最大叶绿素自发荧光强度投影图进行涂层表面藻黏附率分析,将黏附率定义为显微镜视野中藻细胞黏附的面积与样品表面积的比值[13]。
2 结果与讨论
2.1 涂层表面化学组成表征
实验采用傅里叶变换衰减全反射红外光谱(ATR-FTIR)和X射线光电子能谱(XPS)对涂层表面化学组成进行分析。MEC0—MEC1.0的ATR-FTIR光谱图见图2,与环氧树脂涂层(MEC0)相比,QAC改性环氧树脂涂层(MEC0.2—MEC1.0)均在1541 cm-1检测到季铵基团(R4N+)的特征吸收峰[14],说明MEC0.2~MEC1.0表面含有QAC。
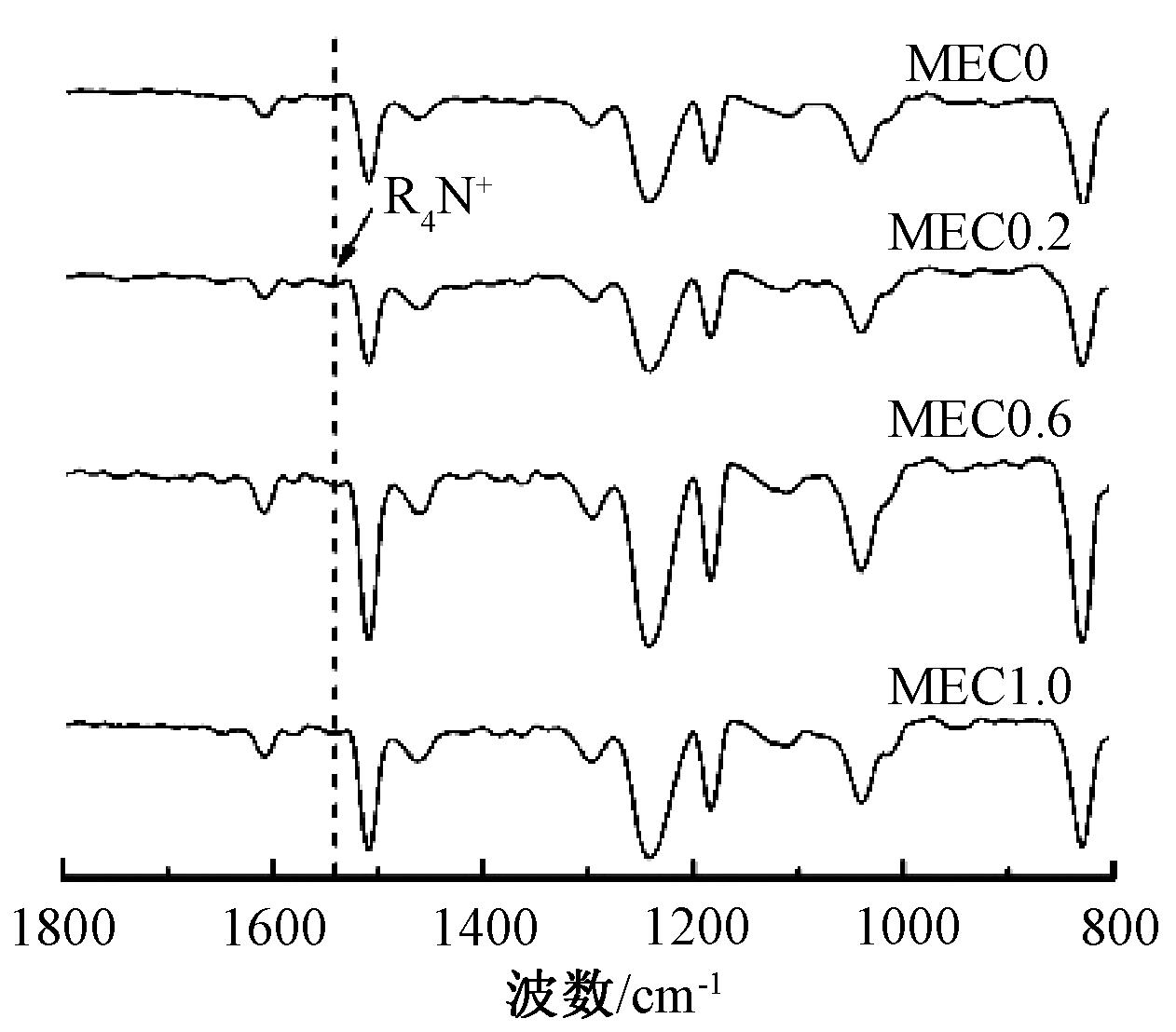
图2 MEC0—MEC1.0的ATR-FTIR光谱
Figure 2 ATR-FTIR spectra of MEC0—MEC1.0
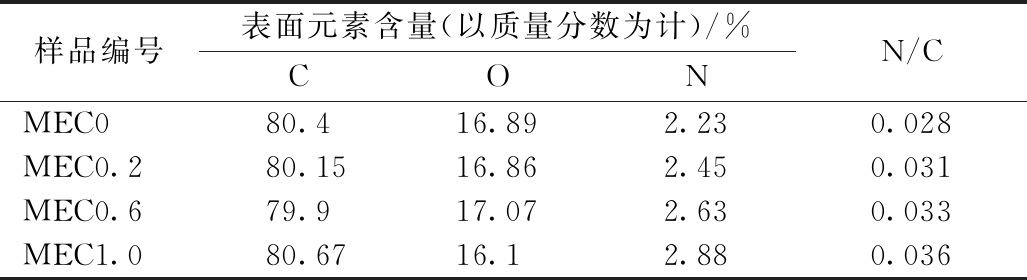
通过XPS进一步表征分析涂层表面元素组成。XPS全谱图(图3a)显示环氧树脂涂层和QAC/环氧树脂复合涂层均有C 1s、N 1s、O 1s峰,说明在QAC改性前后,涂层有基本相同的元素。对各样品的C 1s分峰拟合,结果如图3b—e所示。可知:所有涂层样品的C 1s谱均能分为3个峰,分别为284.6 eV的C—C/C—H、286.2 eV的C—N/C—O、288 eV附近的C![]() O。QAC改性后,涂层的C—N/C—O峰(286.2 eV)的强度随QAC浓度的增加而增大,说明QAC改性涂层的含氮基团/含氧基团数量增多。进一步对各样品的N 1s分峰拟合,结果如图3f—i所示,其中,400.0 eV为中性胺类(R3N)的结合能,402.0 eV为季铵类(R4N+)的结合能[15,16]。可以看出:R4N+的峰强随QAC浓度的增加逐渐增大,说明R4N+含量逐渐增多。由各涂层表面元素含量分布数据(表2)可知:随着QAC投加量的增加,样品表面的N/C值逐渐增大,由MEC0的0.028增加到MEC1.0的0.036,说明样品表面含氮基团的数量随QAC浓度的增加而增多,与C 1s和N 1s谱图反映的结果一致。XPS的测试结果表明,与环氧树脂涂层相比,QAC/环氧树脂复合涂层表面的季铵基团(R4N+)更多,且R4N+的数量随QAC投加量的增加而增加。
O。QAC改性后,涂层的C—N/C—O峰(286.2 eV)的强度随QAC浓度的增加而增大,说明QAC改性涂层的含氮基团/含氧基团数量增多。进一步对各样品的N 1s分峰拟合,结果如图3f—i所示,其中,400.0 eV为中性胺类(R3N)的结合能,402.0 eV为季铵类(R4N+)的结合能[15,16]。可以看出:R4N+的峰强随QAC浓度的增加逐渐增大,说明R4N+含量逐渐增多。由各涂层表面元素含量分布数据(表2)可知:随着QAC投加量的增加,样品表面的N/C值逐渐增大,由MEC0的0.028增加到MEC1.0的0.036,说明样品表面含氮基团的数量随QAC浓度的增加而增多,与C 1s和N 1s谱图反映的结果一致。XPS的测试结果表明,与环氧树脂涂层相比,QAC/环氧树脂复合涂层表面的季铵基团(R4N+)更多,且R4N+的数量随QAC投加量的增加而增加。
ATR-FTIR和XPS的测试结果表明,QAC已经成功与环氧树脂涂料基体进行复合,且涂层表面的R4N+含量与QAC投加量呈正相关。
2.2 涂层基本性能测试
各涂层的接触角、表面Zeta电位和粗糙度的测试结果如图4所示。MEC0、MEC0.2、MEC0.6、MEC1.0表面与纯水的接触角分别为(91.5°±6.3°)、(91.4°±1.7°)、(90.0°±1.4°)、(90.1°±2.9°),四者没有明显的区别,说明所有涂层都呈疏水性,且不同浓度QAC的投加对涂层疏水性没有显著影响。由Zeta电位的测试结果可知:随着QAC浓度的增加,涂层表面Zeta电位向正电性偏移,MEC0—MEC1.0的Zeta电位由(-28.7±2.7) mV增加至(-20.4±1.0) mV,说明QAC的正电性季铵基团对涂层表面电位产生影响[17,18]。图4c的Ra、Rq和Rmax分别表示平均粗糙度、表面均方根粗糙度和最大粗糙度。由粗糙度的结果可看出:所有涂层的粗糙度都比较小,说明涂层表面光滑;随着QAC投加量的增加,涂层表面粗糙度略有降低。涂层的粗糙度与其聚合物的交联度相关,当涂层聚合物交联度减小时,涂层表面粗糙度会随之减小[19],因此,QAC/环氧树脂复合涂层粗糙度的略微减小可能由于QAC的投加对环氧树脂的交联度有一定影响。
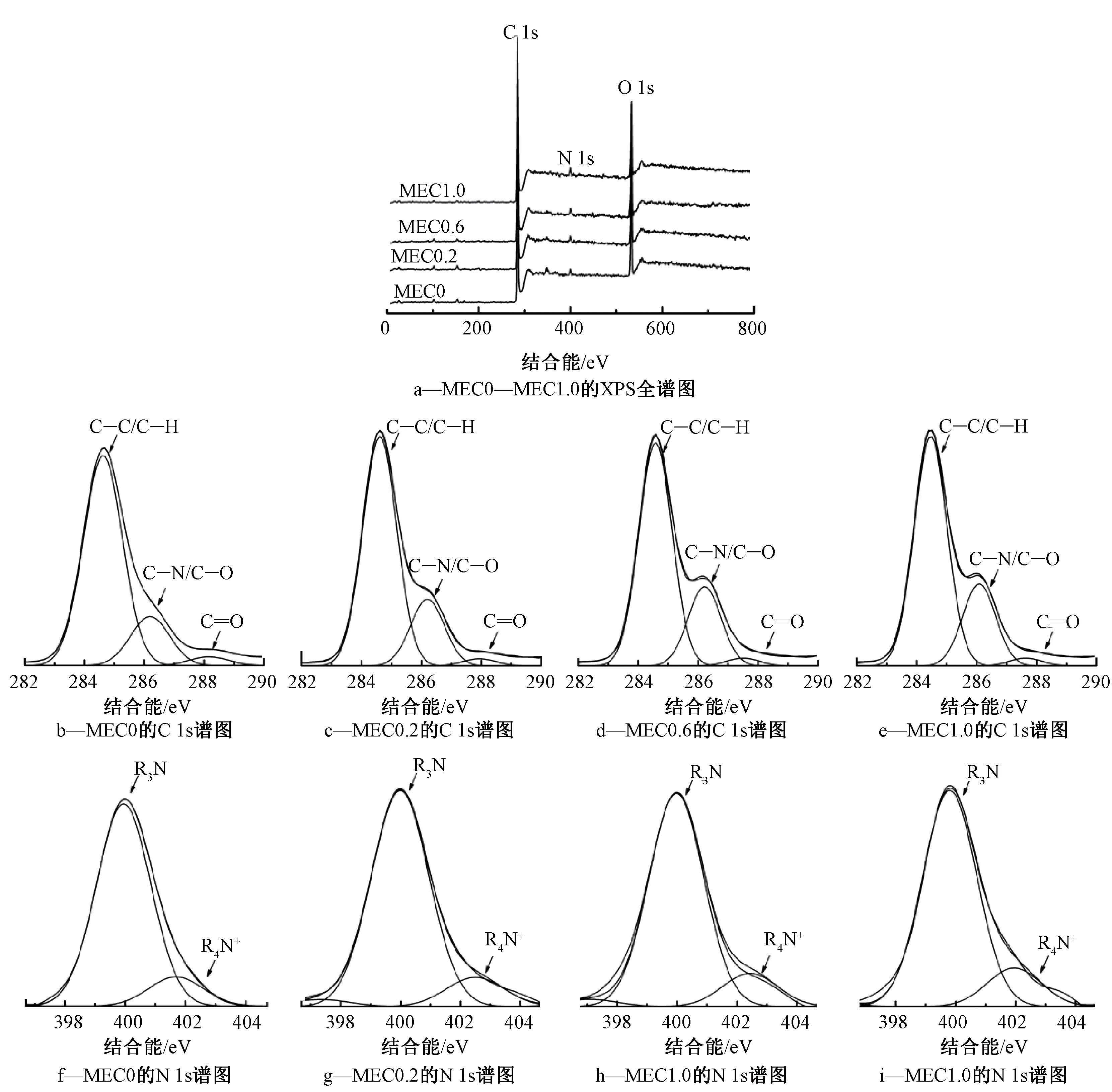
图3 MEC0—MEC1.0的XPS分析结果
Figure 3 XPS analysis result of MEC0—MEC1.0
表2 MEC0—MEC1.0表面元素含量分布
Table 2 Surface elemental composition of MEC0—MEC1.0
样品编号表面元素含量(以质量分数为计)/%CONN/CMEC080.416.892.230.028MEC0.280.1516.862.450.031MEC0.679.917.072.630.033MEC1.080.6716.12.880.036
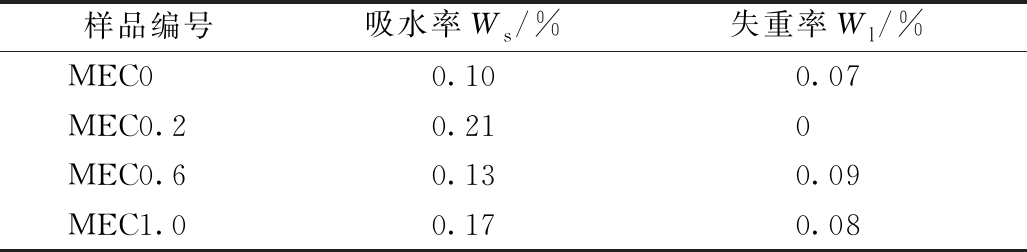
为研究QAC改性涂层在水环境的稳定性,实验将各涂层样品浸泡在水中30 d后进行吸水率和失重率测试,测试结果如表3所示。在水中浸泡30 d后,MEC0—MEC1.0均无明显的溶胀和质量损失现象,这是由于涂层表面疏水性较强以及涂层聚合物交联度较高[11]导致。此现象说明各涂层均具有良好的耐水性,QAC改性对环氧树脂涂层在水中的稳定性无显著影响,因此QAC/环氧树脂复合涂层适用于水处理构筑物。
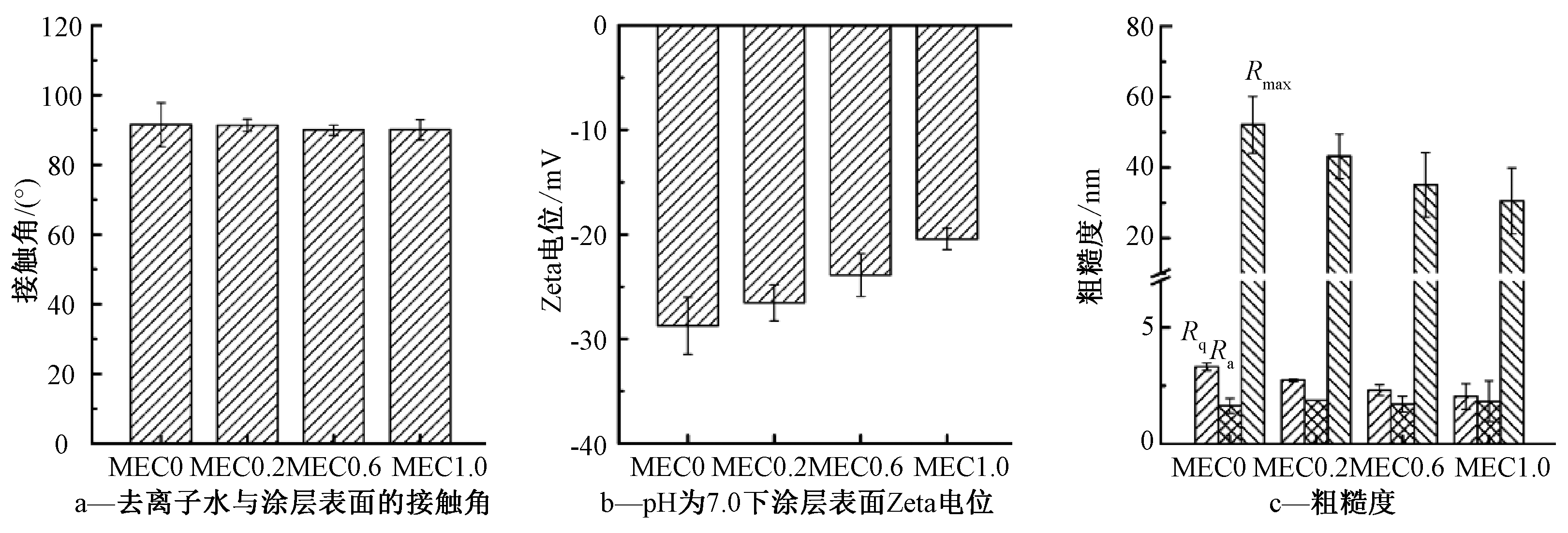
图4 MEC0—MEC1.0的基本性质
Figure 4 Basic properties of MEC0—MEC1.0
表3 涂层的耐水性
Table 3 The stability of the coatings under water
样品编号吸水率Ws/%失重率Wl/%MEC00.100.07MEC0.20.210MEC0.60.130.09MEC1.00.170.08
2.3 涂层抑藻性能测试
实验采用小球藻作为模型藻类对涂层表面进行污染,为了便于观察小球藻在涂层表面的黏附/生长情况,采用涂覆在无纺布表面的涂层样品进行抗污染实验,并利用浊度法和激光共聚集显微镜(CLSM)评估涂层抗藻类黏附/生长性能。为量化涂层表面黏附/生长的小球藻数量,实验将MEC0—MEC1.0涂层表面的小球藻脱附下来后重悬于1 mL PBS溶液中,并测试藻液的OD680值,结果如图5所示。可知:随着QAC投加量增加,藻液的OD680值逐渐减小,说明QAC/环氧树脂复合涂层表面黏附/生长的小球藻数量减少,QAC改性有利于提高涂层的抑藻性能,且QAC浓度越高,抑藻效果越明显。此趋势同样可见于CLSM的测试结果(图6)中。由涂层表面小球藻黏附情况的3D CLSM图(图6a—d)可看出:当QAC投加量增加到1.0%(质量分数)时,涂层表面的小球藻显著减少。为进一步量化小球藻在不同环氧树脂涂层表面的黏附情况,采用ImageJ软件对各样品的表面最大叶绿素自发荧光强度投影图(图6e—h)进行分析处理,得到小球藻的黏附率,结果如图5b所示。MEC0、MEC0.2、MEC0.6、MEC1.0的小球藻黏附率分别为16.6%、4.0%、3.8%、1.1%,其中,MEC1.0的小球藻黏附率仅为MEC0的6.7%,即MEC1.0的小球藻去除率为93.3%,说明其具有明显的抗藻污染性能。
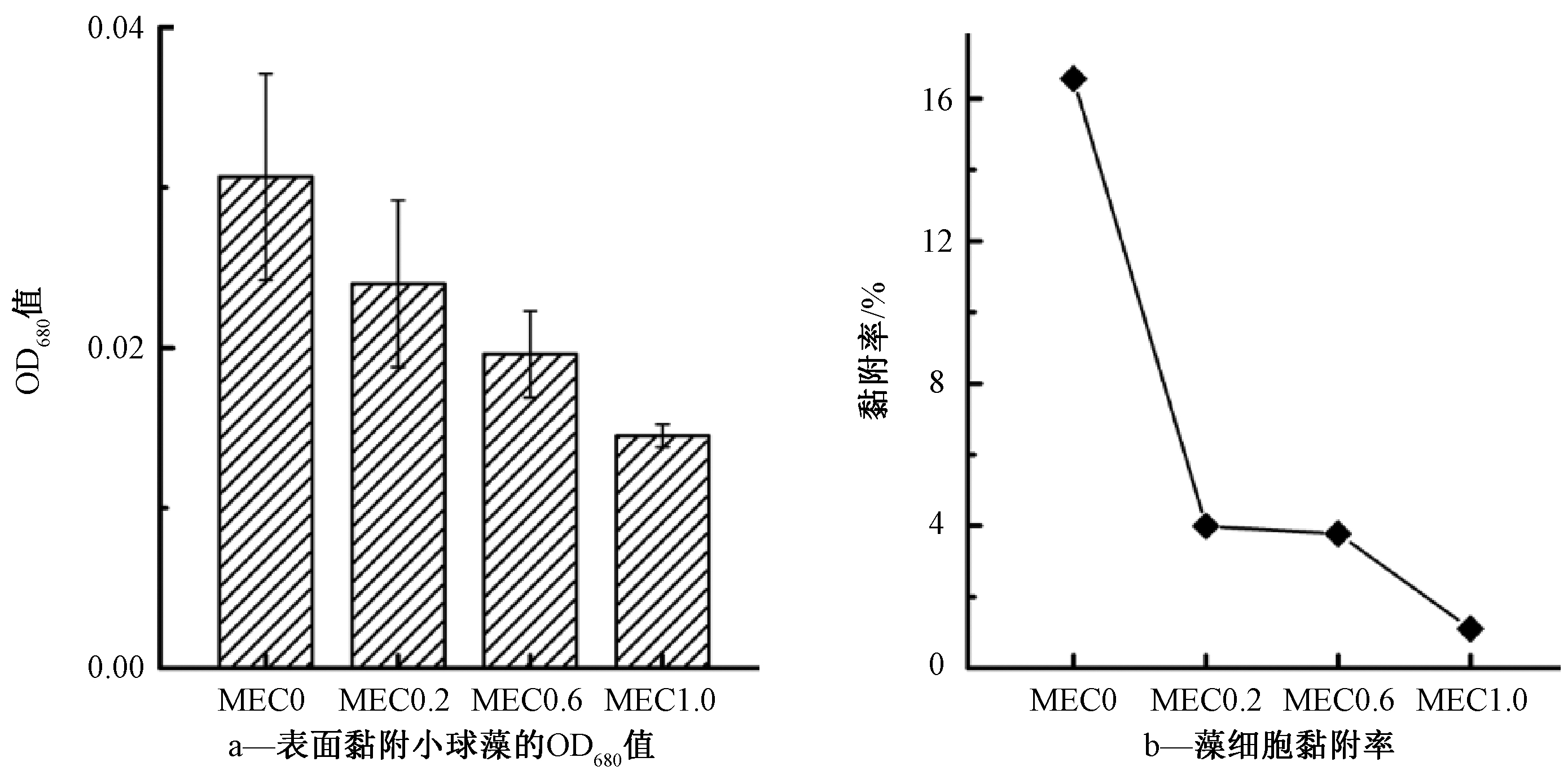
图5 MEC0—MEC1.0抗藻污染性能
Figure 5 Anti-algae performance of MEC0—MEC1.0
QAC/环氧树脂复合涂层的抑藻性能推测是由于其表面负载的季铵基团(R4N+)带正电,可以吸附带负电的藻细胞,同时R4N+的疏水长链会破坏藻细胞的细胞膜,进而导致细胞死亡[20]。此外,Zhang等[15]的研究表明,涂层抑制微生物的活性与其表面R4N+含量呈正相关,因此与环氧树脂涂层相比,QAC/环氧树脂复合涂层可以明显抑制藻类在涂层表面的黏附和生长,而且随着QAC投加量增多,涂层抗藻污染性能越好。

图6 各涂层表面小球藻细胞黏附现象的3D CLSM图以及表面最大叶绿素自发荧光强度投影图像
Figure 6 3D CLSM images of Chlorella vulgaris attached on surfaces of MEC0—MEC1.0 and maximum chlorophyll autofluorescence intensity projection images of MEC0—MEC1.0
3 结 论
本文利用DDBAC作为模型季铵盐(QAC)与水处理构筑物中常用的环氧树脂涂料共混得到QAC/环氧树脂复合涂层,并探究QAC投加量对复合涂层基本性能和抑藻性能的影响:
1)ATR-FTIR和XPS的测试结果表明,QAC成功与环氧树脂涂料基体进行复合,且涂层表面的季铵基团(R4N+)的数量与QAC投加量呈正相关。
2)QAC改性对涂层的疏水性、耐水性不产生显著影响,但随着QAC浓度的增加,涂层表面Zeta电位向正电性偏移,粗糙度略微减小。
3)采用小球藻作为模型藻类,对比分析QAC改性前后的环氧树脂涂层的抑藻性能。结果显示:QAC改性可以有效改善涂层的抗藻污染性能,且QAC浓度越高,涂层表面黏附/生长的小球藻数量越少,抑藻性能越明显。QAC/环氧树脂复合涂层的抑藻性能是由于其表面的R4N+可导致黏附/生长在涂层表面的小球藻死亡,且R4N+基团含量越多,涂层抑制藻类黏附/生长的性能越好。
4)当QAC投加量为1.0%时,QAC/环氧树脂复合涂层表现出良好的抗藻污染的性能,且涂层耐水性能良好,适用于污水处理构筑物中。
[1] SAUVET G, FORTUNIAK W, KAZMIERSKI K, et al. Amphiphilic block and statistical siloxane copolymers with antimicrobial activity[J]. Journal of Polymer Science Part A Polymer Chemistry, 2003, 41(19): 2939-2948.
[2] GOTTENBOS B, BUSSCHER H J, VAN DER MEI H C. Pathogenesis and prevention of biomaterial centered infections[J]. Journal of Materials Science: Materials in Medicine, 2002, 13(8): 717-722.
[3] GOTTENBOS B, VAN DER MEI H C, KLATTER F, et al. In vitro and in vivo antimicrobial activity of covalently coupled quaternary ammonium silane coatings on silicone rubber[J]. Biomaterials, 2002, 23(6): 1417-1423.
[4] LENOIR S, PAGNOULLE C, DETREMBLEUR C, et al. Antimicrobial activity of polystyrene particles coated by photo-crosslinked block copolymers containing a biocidal polymethacrylate block[J]. E-Polymers, 2005, 74: 1-11.
[5] MAJUMDAR P, LEE E, PATEL N, et al. Combinatorial materials research applied to the development of new surface coatings Ⅸ: an investigation of novel antifouling/fouling-release coatings containing quaternary ammonium salt groups[J]. Biofouling, 2008, 24(3): 185-200.
[6] NURDIN N, HELARY G, SAUVET G. Biocidal polymers active by contact. Ⅱ. Biological evaluation of polyurethane coatings with pendant quaternary ammonium salts[J]. Journal of Applied Polymer Science, 1993, 50(4): 663-670.
[7] TASHIRO T. Antibacterial and bacterium adsorbing macromolecules[J]. Macromolecular Materials & Engineering, 2001, 286(2): 63-87.
[8] MURATA H, KOEPSEL R R, MATYJASZEWSKI K, et al. Permanent, non-leaching antibacterial surfaces-2: how high density cationic surfaces kill bacterial cells[J]. Biomaterials, 2007, 28(32): 4870-4879.
[9] 张文涛, 张庆华, 詹晓力, 等. 季铵盐修饰有机硅改性聚氨酯的制备与杀菌性能[J]. 化工新型材料, 2012, 40(9): 116-119.
[10] JELLALI R, KROMKAMP J C, CAMPISTRON I, et al. Antifouling action of polyisoprene-based coatings by inhibition of photosynthesis in microalgae[J]. Environmental Science & Technology, 2013, 47(12): 6573-6581.
[11] CONESKI P N, WEISE N K, FULMER P A, et al. Development and evaluation of self-polishing urethane coatings with tethered quaternary ammonium biocides[J]. Progress in Organic Coatings, 2013, 76(10): 1376-1386.
[12] VILLACORTE L O, EKOWATI Y, NEU T R, et al. Characterisation of algal organic matter produced by bloom-forming marine and freshwater algae[J]. Water Research, 2015, 73: 216-230.
[13] HE X Y, SUO X K, BAI X Q, et al. Functionalizing aluminum substrata by quaternary ammonium for antifouling performances[J]. Applied Surface Science, 2018, 440: 300-307.
[14] MENG J Q, ZHANG X, NI L, et al. Antibacterial cellulose membrane via one-step covalent immobilization of ammonium/amine groups[J]. Desalination, 2015, 359: 156-166.
[15] ZHANG Q H, LIU H L, ZHAN X L, et al. Microstructure and antibacterial performance of functionalized polyurethane based on polysiloxane tethered cationic biocides[J]. RSC Advances, 2015, 5(95): 77508-77517.
[16] YUAN S J, GU J T, ZHENG Y, et al. Purification of phenol-contaminated water by adsorption with quaternized poly(dimethylaminopropyl methacrylamide)-grafted PVBC microspheres[J]. Journal of Materials Chemistry A, 2015, 3(8): 4620-4636.
[17] LIU C X, ZHANG D R, HE Y, et al. Modification of membrane surface for anti-biofouling performance: effect of anti-adhesion and anti-bacteria approaches[J]. Journal of Membrane Science, 2010, 346(1): 121-130.
[18] ZHANG X R, WANG Z W, CHEN M, et al. Polyvinylidene fluoride membrane blended with quaternary ammonium compound for enhancing anti-biofouling properties: effects of dosage[J]. Journal of Membrane Science, 2016, 520: 66-75.
[19] JELLALI R, KROMKAMP J C, CAMPISTRON I, et al. Antifouling action of polyisoprene-based coatings by inhibition of photosynthesis in microalgae[J]. Environmental Science & Technology, 2013, 47(12): 6573-6581.
[20] MAJUMDAR P, LEE E, PATEL N, et al. Development of environmentally friendly, antifouling coatings based on tethered quaternary ammonium salts in a crosslinked polydimethylsiloxane matrix[J]. Journal of Coatings Technology and Research, 2008, 5(4): 405-417.