亚铁氧化反硝化(nitrate-dependent anaerobic ferrousiron oxidation,NAFO)过程,是指以亚铁和硝态氮分别为电子供体和受体进行反硝化反应,其中硝态氮主要还原产物为N2,具有脱氮效应,因此该过程已经被研究应用于污水脱氮[1]。例如,Nielsen等[2]发现,不同污水处理厂反硝化污泥投加亚铁后,脱氮效率普遍提高;王苏艳等[3]研究发现,亚铁作为反硝化的电子供体能够显著提高人工湿地反硝化效率;王梦月等[4]构建铁-氮的SBR反应器能够高效地处理低C/N废水,而Zhou等[5,6]则进一步开发了完全基于NAFO过程的废水脱氮工艺。对于低C/N污水,NAFO菌可使用更廉价的亚铁作为电子供体,替代较昂贵的有机碳源,有效地降低运行成本,因此基于NAFO过程的污水处理具有更好的经济性[7]。
NAFO微生物在中性环境中催化亚铁氧化,生成的铁氧化物以矿物形式沉积积累,是典型的生物成矿过程[8]。NAFO过程的生物成矿呈现多种形式,既有晶体结构的针铁矿、磁铁矿、纤铁矿等,也有无定形态的三价铁氧化物[9-14]。这种生物成矿通常受到NAFO菌的胞外多聚物(extracellular polymeric substances,EPS)影响,胞外多聚物通过与初步形成的铁氧化物矿物结合,促进亚铁的进一步氧化以及矿物沉淀的形成,因此,在NAFO过程中生物成矿的形式受多种条件影响,包括参与的微生物类型、反应液组成和pH等[15, 16]。目前,关于NAFO过程生物成矿,关注较多的仍是以NAFO菌代谢为研究目的的小规模序批式反应条件下形成的铁氧化物矿物[17]。随着NAFO过程被应用于污水脱氮处理,这种生物成矿必然在相应的污水处理反应器中不断出现,这也意味着反应器同时也是一个铁氧化物矿物的连续生产装置。同时,污水处理的反应条件往往与序批式不同,特别是一些连续流处理方式,所形成的铁矿物形式也有待探索。
一些工业废水中含有的Cd等高毒性重金属,进入水体或土壤环境后,不仅会危害野生动物、抑制微生物酶的活性,而且通过食物链的途径进入人体内,威胁人体健康[18-20]。铁氧化物矿物对水中的Cd、Cr和As等具有较强的吸附去除能力,可作为这些无机物去除的有效吸附剂[21-28]。而一些研究发现, NAFO生物成矿过程形成的铁矿物对Cd等重金属同样具有较好的吸附去除效果[17, 24, 29]。NAFO过程为主的污水脱氮反应器,有可能也是一个潜在重金属吸附剂的生产装置,形成的铁氧化物矿物的重金属吸附特性值得探索。
本研究首先构建了亚铁氧化反硝化生物膜反应器,采用连续流污水脱氮处理并分别收集反应器中不同部分含铁的沉积颗粒物,然后利用SEM、XRD、FITR等方法分析其颗粒形态、表面特征和化学活性基团等性质,最后通过吸附等温线和吸附动力学实验,探究基于NAFO过程的连续流式生物膜反应器生成的含铁颗粒物对重金属Cd的吸附机制。
本研究所使用的反应器构造如图1所示。反应装置主体为透明亚克力材料制成的圆桶,高度和内直径分别为33,10 cm,总容积为2.5~2.6 L。实验装置内部设置支架支撑载体填料,载体选用软性束状材料。反应器底部设置2个进水管,分别输入含氮的污水和亚铁溶液,顶部设置出水管和排气口各1个,进水口连接水泵和封闭水箱,出水排放至塑料水箱,该反应器以连续式进行运作。
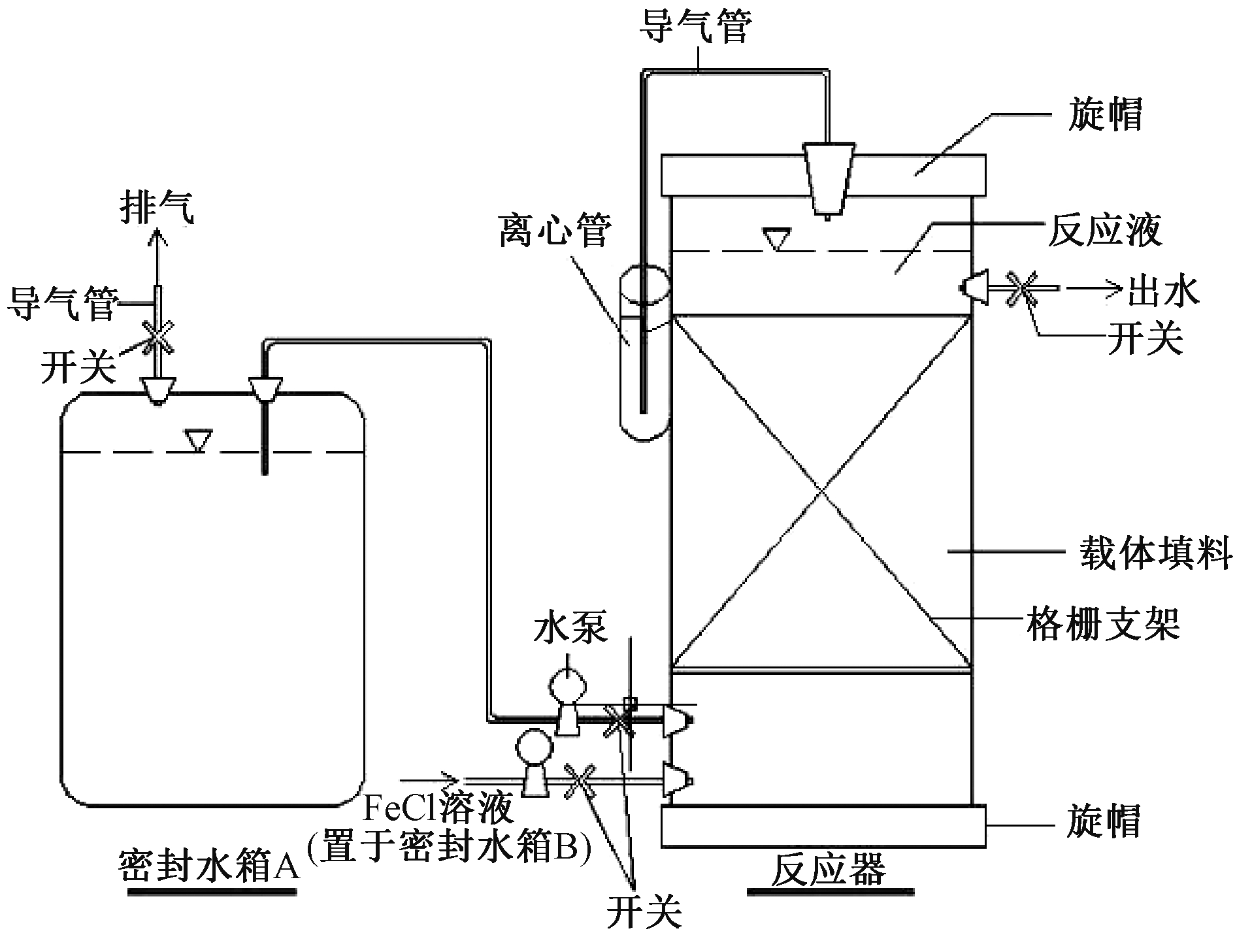
图1 亚铁氧化反硝化生物膜反应器
Figure 1 Nitrate-dependent anaerobic ferrous iron oxidation biofilm reactor
反应装置接种的NAFO菌是能够高效进行NAFO反应的富集培养液,来源于广州车陂涌底泥[17]。
含氮污水以单蒸水为基础,加入化学试剂人工配制而成。反应器启动初期,为了促进NAFO菌生长,采用较高浓度的磷25 mg/L,具体组成如下(每升):KH2PO4,100 mg;K2HPO4,100 mg;NaNO3,152 mg;CH3COONa,82 mg;NaHCO3,1680 mg;MgSO4·7H2O,200 mg;反应器可稳定进行脱氮反应后,降低磷浓度到5 mg/L。
亚铁溶液:采用FeCl2·4H2O配制,浓度为1772.8 mg/L。
1)运行方式。
含氮污水和亚铁溶液分别输入反应器。含氮污水亚铁溶液水力负荷均设定为1.2 m3/(m3·d)。反应器内亚铁浓度维持在9.0 mmol/L左右。
反应装置进水开始使用高磷浓度(25 mg/L),连续运行25 d后出水的亚铁和硝酸盐氮浓度基本稳定,而且硝酸盐氮也可被有效去除,此时将进水改为低磷浓度(5~7 mg/L),继续连续运行1个月。运行期间继续监测进水和出水的亚铁、硝酸盐氮和pH,并收集出水中的固体颗粒(EP组)。
运行结束后,将反应器内的水排尽,对上、中、下3个部位的填料分别取样,然后将填料上附着的固体颗粒(含铁氧化物)分离下来。上、中、下部固体颗粒分别对应TP、MP、BP组。
2)测定方法。
傅里叶红外光谱(FTIR)分析、X射线衍射(XRD)分析和吸附比表面积:取适量样品自然风干,研磨,过300目筛,保存在干燥皿中待测。
扫描电镜(SEM)分析:取适量样品,用2 mL离心管,5000 r/min离心10 min,保存在4 ℃冰箱中待测。
零电荷点(pHpzc):取适量样品于锥形瓶中,并添加浓度为0.1 mol/L的KCl溶液,调节初始pH分别为2~11,测定24 h后的pH。
亚铁和总铁含量的测定:沉积物形成后,由于含水率高达90%以上(一般单个培养容器中沉积物混合液约为200 mL,其中含1~2 g沉积物),故需要先取适量沉积物于100 mL离心管,2500 r/min离心10 min,倒掉上清液,再测定沉积物中的亚铁、总铁含量。根据预实验结果,最终确定使用1 mol/L盐酸、液固比为100、转速为200 r/min、35 ℃下进行浸提60 min后,测定沉积物中亚铁含量(湿重)和总铁含量(湿重)。
溶液pH采用pH测定仪(上海雷磁)进行测定。溶液中Cd含量采用火焰原子吸收分光光度计(Z-2000,HITACHI)测定。亚铁用邻菲罗林分光光度法(HJ/T 345─2007)测定。固体的铁含量采用硝酸-高氯酸-氢氟酸消煮,原子吸收分光光度计(Z-2000,HITACHI)测定。
比表面积及孔径采用BET/N2吸收法和比表面及孔隙分析仪(GEMINIⅦ2390,USA)进行测定。
颗粒粒径范围使用HORIBALA-960S型激光粒度仪进行测定。晶体结构用X射线粉末衍射仪(XD-2/3,Beijing Purkinje General,China)检测,颗粒表面结构用扫描电镜(SEM-EDS)(Zeiss LEO1530VP,German)分析。
硝酸盐氮![]() 亚硝酸盐氮
亚硝酸盐氮![]() 和氨氮(NH3-N)测定分别采用SL 84—1994 《硝酸盐氮的测定(紫外分光光度法)》、GB/T 7493—1987《水质 亚硝酸盐氮的测定 分光光度法》和HJ 535—2009 《水质 氨氮的测定 纳氏试剂分光光度法》。
和氨氮(NH3-N)测定分别采用SL 84—1994 《硝酸盐氮的测定(紫外分光光度法)》、GB/T 7493—1987《水质 亚硝酸盐氮的测定 分光光度法》和HJ 535—2009 《水质 氨氮的测定 纳氏试剂分光光度法》。
吸附动力学实验:称取0.5 g固体颗粒装入150 mL锥形瓶中,加入浓度为2 mg/L的100 mL Cd溶液,分别于0 min、30 min、1 h、3 h、5 h、10 h、24 h、48 h、72 h抽取5 mL上清液进行过滤,向滤液中滴加浓硝酸进行保存,随后测定滤液中Cd的浓度值。
吸附等温线实验:称取0.2 g固体颗粒装入100 mL锥形瓶中,分别加入80 mL Cd浓度为0,0.1,0.3,0.5,0.8,1,1.5,2 mg/L的溶液,在180 r/min下振荡数小时后,抽取5 mL上清液进行过滤,然后向滤液中滴加浓硝酸进行保存,随后测定滤液中Cd的浓度值。
在低磷浓度下,反应器出水亚铁虽然有波动,但反应器平均亚铁去除率仍在80%以上(图2),而出水中的硝态氮去除率高达90%以上,运行过程中反应器内呈弱碱性,并且几乎未产生NH3-N和![]() 等中间产物,说明构建的NAFO反应器在低磷浓度下具有较好的脱氮效果。
等中间产物,说明构建的NAFO反应器在低磷浓度下具有较好的脱氮效果。
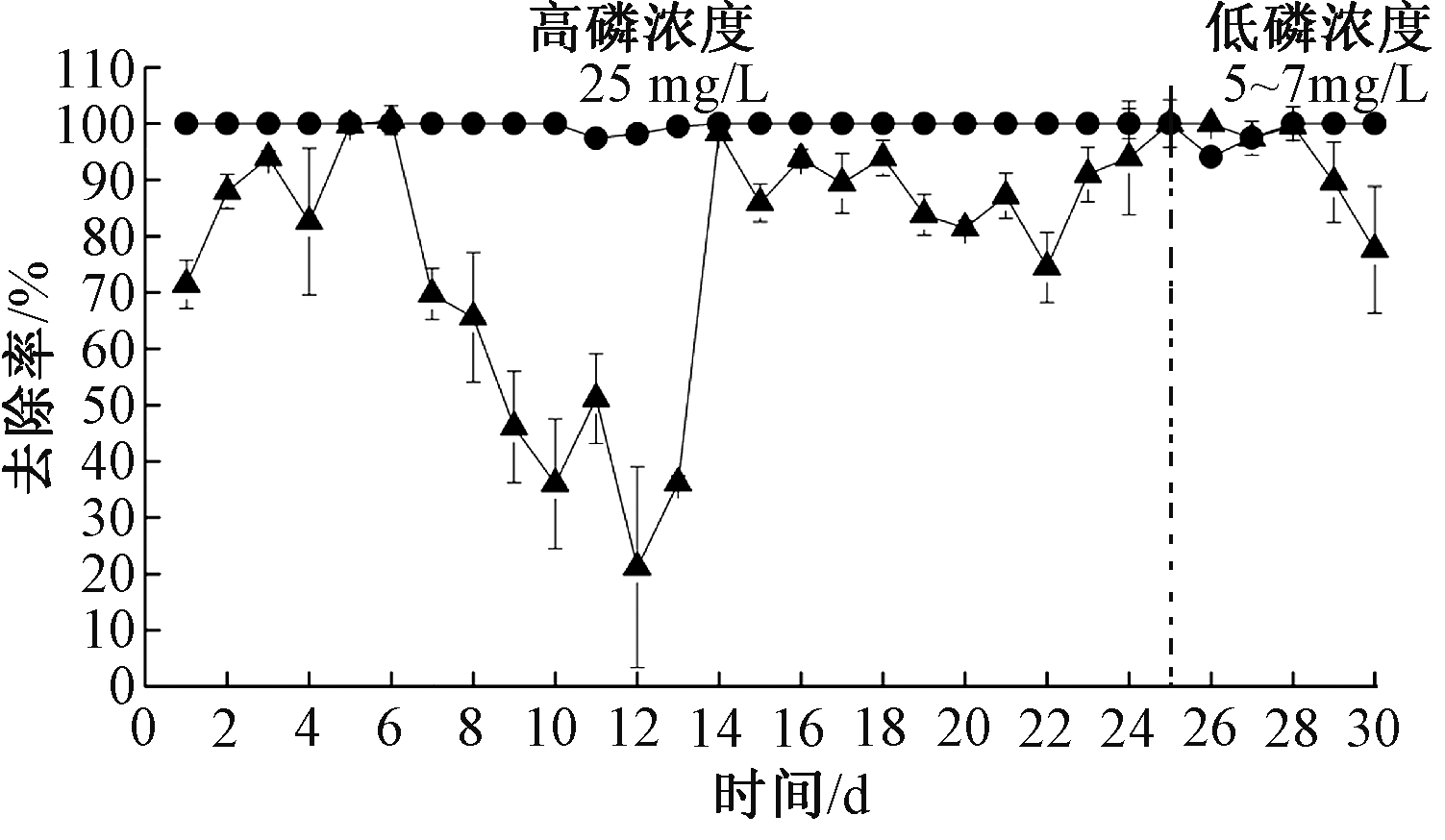
![]() —亚铁;
—亚铁;![]()
图2 低磷浓度下反应器对亚铁、硝酸盐氮去除率
Figure 2 The removal rates of ferrous iron, nitrate nitrogen in the reactor with lower phosphorus concentration
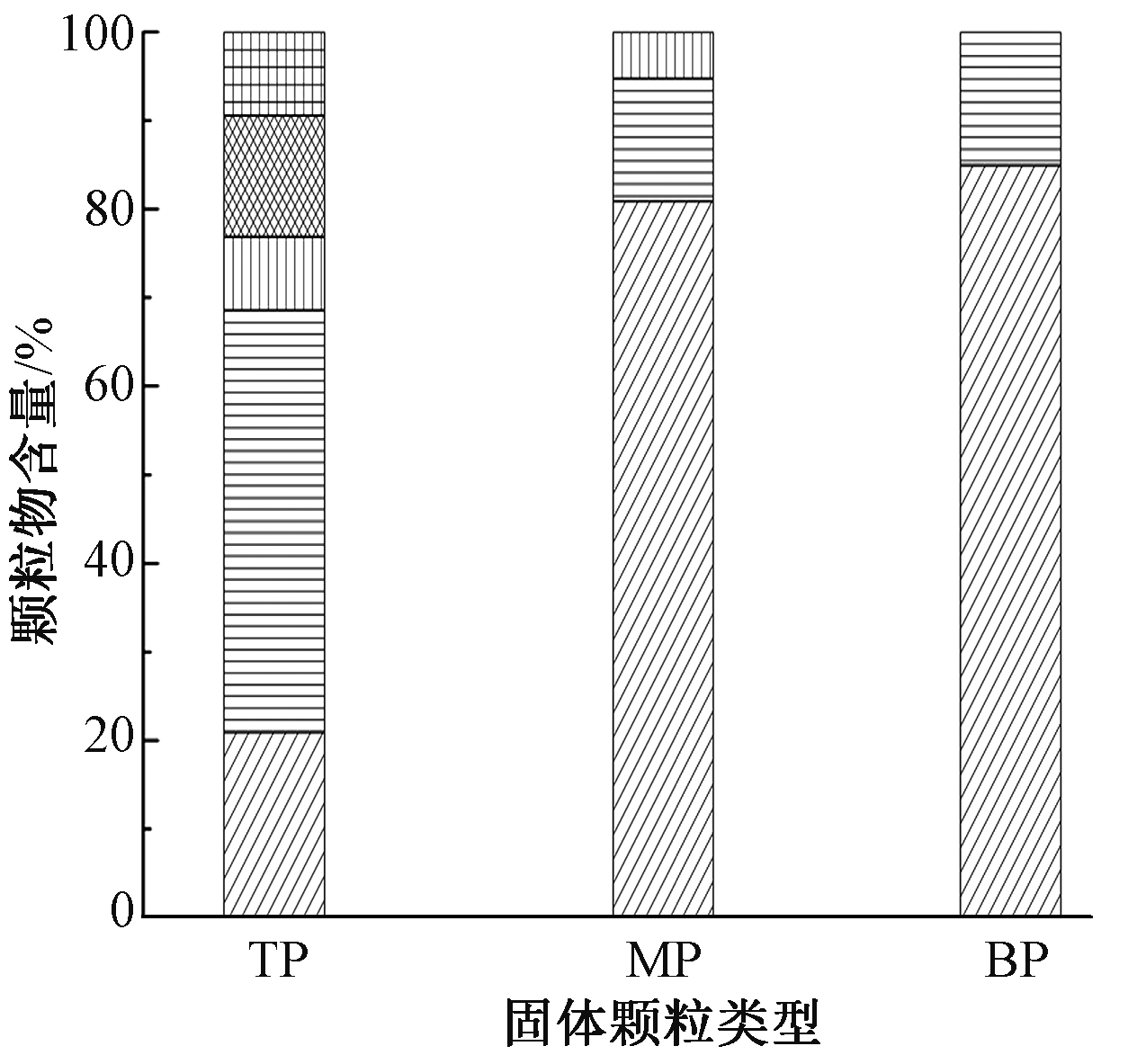
图3为反应器不同位置固体颗粒物的化学特性。反应器中生成的固体颗粒含有大量的铁和有机质,不同位置形成颗粒物中铁和有机物含量不同,总铁含量顺序为BP>MP>TP>EP,下部的固体颗粒总铁含量最高达到(851.79±128.68) g/kg;有机质含量顺序为MP>TP>BP>EP,中部固体颗粒有机质含量为(5007.8±401.95) g/kg。颗粒中的铁来源于进水中亚铁的沉降,下部固体颗粒的总铁含量最高,表明亚铁进入反应器后即可发生大量沉降,有机物主要是来源于进行NAFO反应的微生物细胞及其衰亡产物。这些颗粒具有两性电解质特性,TP、MP和BP固体颗粒的等电点均接近6,EP的等电点为8.58±0.06,是由于其中铁氧化物形态不同所致。
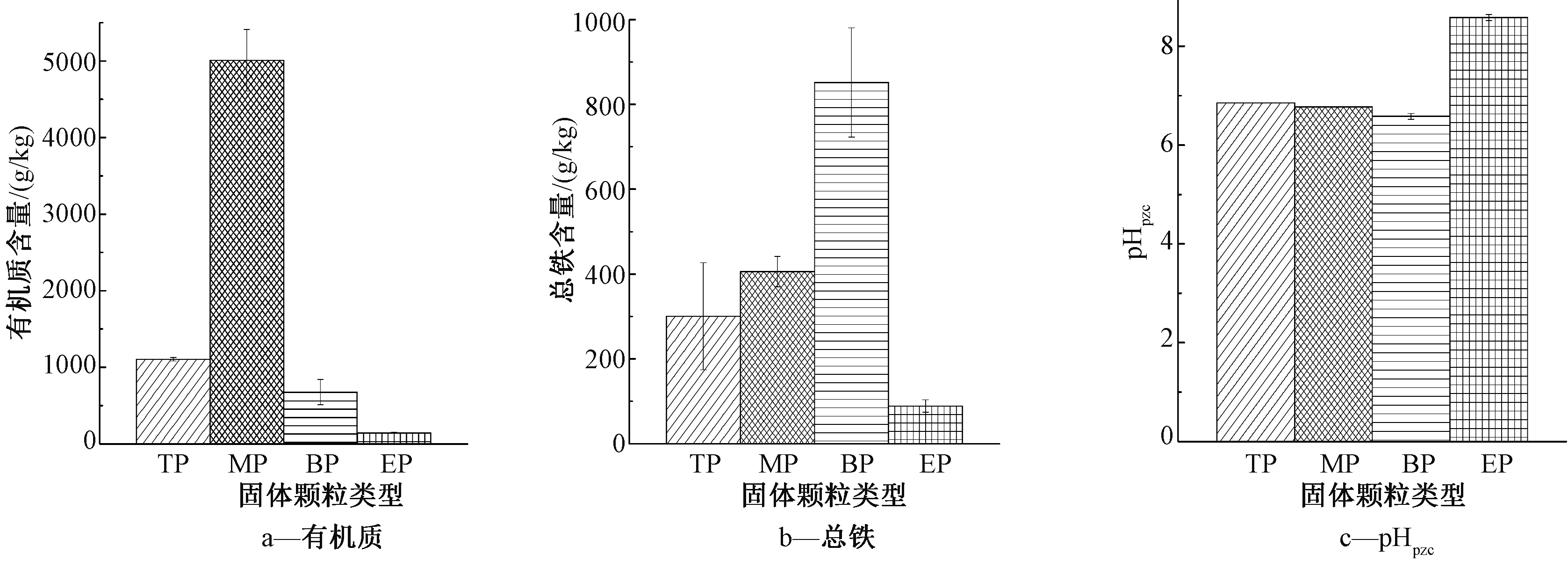
图3 反应器不同位置固体颗粒物的化学特性
Figure 3 Chemical characteristics of solid particles in different positions of the reactor
SEMs结果(图4)显示,反应器内形成的颗粒物的致密度随着高度的增加逐渐降低,下部的颗粒物比顶部更为密集,而出水固体颗粒最为疏松。虽然固体颗粒中有机质较高,但在SEM图中并未看到微生物细胞的大量存在,可能是其被铁氧化物颗粒所覆盖所致。此外,上部、中部、下部的固体颗粒组成大多为分散的方块状颗粒,表面还分布许多细小的片状颗粒,出水固体颗粒物则以细小的片状和针状的颗粒为主。
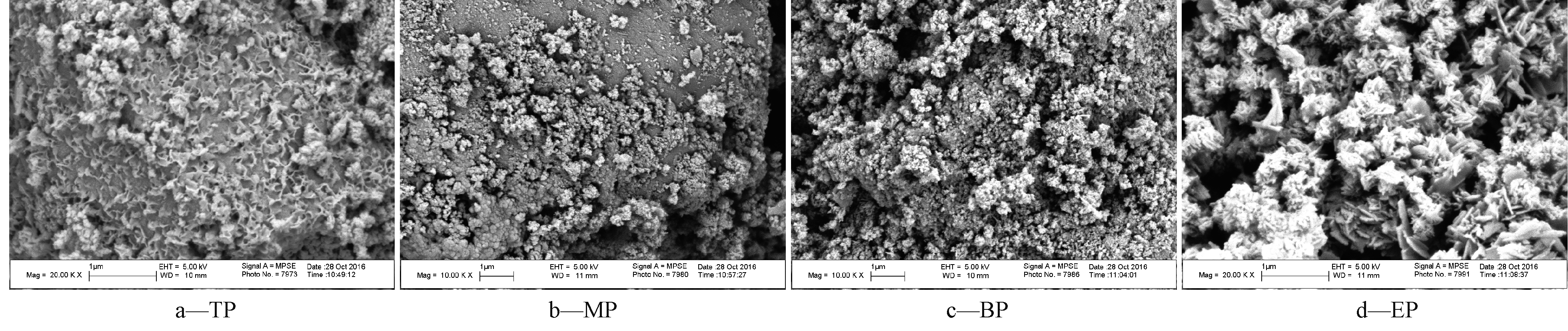
图4 反应器不同位置固体颗粒的SEMs结果
Figure 4 SEMs of solid particles in different positions of the reactor
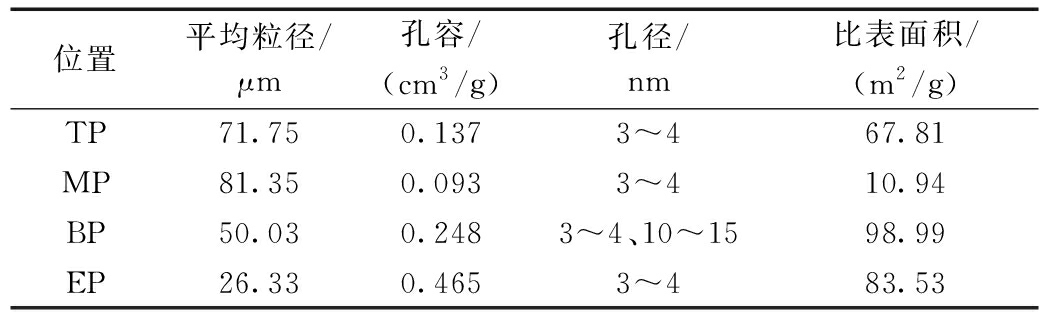
XRD结果(图5)显示,SEMs结果中发现的上、中、底部固体颗粒为具有高结晶度的铁矿物,其中上部固体颗粒主要成分为针铁矿(α-FeOOH),下部的颗粒以菱铁矿(FeCO3)为主,而中部颗粒虽同样以菱铁矿为主要成分,但其中还包含针铁矿、磁铁矿(Fe3O4)。对NAFO固体颗粒的表面分析,发现4种颗粒均属于微米级别的颗粒,孔径集中在3~4 nm,属于介孔材料,比表面积较大,下部固体颗粒比表面积最高,达到98.99 m2/g(表1)。
![]() 石英;
石英; ![]() 纤铁矿;
纤铁矿; ![]() 磁铁矿;
磁铁矿; ![]() 针铁矿;
针铁矿; ![]() 菱铁矿。
菱铁矿。
图5 反应器不同位置的固体颗粒物的XRD分析结果
Figure 5 XRD results of solid particles in different positions of the reactor
表1 反应器不同位置的固体颗粒物的结构特征
Table 1 Structural characteristics of solid particles in different positions of the reactor
位置平均粒径/μm孔容/(cm3/g)孔径/nm比表面积/(m2/g)TP71.750.1373~467.81MP81.350.0933~410.94BP50.030.2483~4、10~1598.99EP26.330.4653~483.53
FITR分析结果(图6)表明,反应器形成的固体颗粒表面均存在氧化铁、磷酸盐和有机官能团的特征峰,但不同位置的基团各有区别。可以看出:4种颗粒表面不仅含有铁氧化物相关基团,还包含乙基C—H键、叔醇O—H等有机基团,其中,下部固体颗粒表面的Fe—O键的特征峰数量明显多于其他位置,而上、中部颗粒表面的Fe—O—OH等三价铁氧化物基团的特征峰则更多。该结果进一步验证了反应器内形成的固体颗粒主要成分均为铁矿物和有机物,其中下部的矿物成分以二价铁氧化物为主,上部和中部的矿物中三价铁氧化物的含量更多[30]。此外,单独的酰胺基C![]() O峰的出现和P—O键的存在,说明了4种固体颗粒表面存在酰胺和磷酸盐基团[31]。同样,在不同位置的固体颗粒上均有表面O—H的特征峰,说明O—H基团大量存在于固体颗粒表面,但不同的是,上部固体颗粒的O—H峰的数量要多于其他颗粒,说明上部的铁矿物主要以铁的氢氧化物形式存在[32]。
O峰的出现和P—O键的存在,说明了4种固体颗粒表面存在酰胺和磷酸盐基团[31]。同样,在不同位置的固体颗粒上均有表面O—H的特征峰,说明O—H基团大量存在于固体颗粒表面,但不同的是,上部固体颗粒的O—H峰的数量要多于其他颗粒,说明上部的铁矿物主要以铁的氢氧化物形式存在[32]。
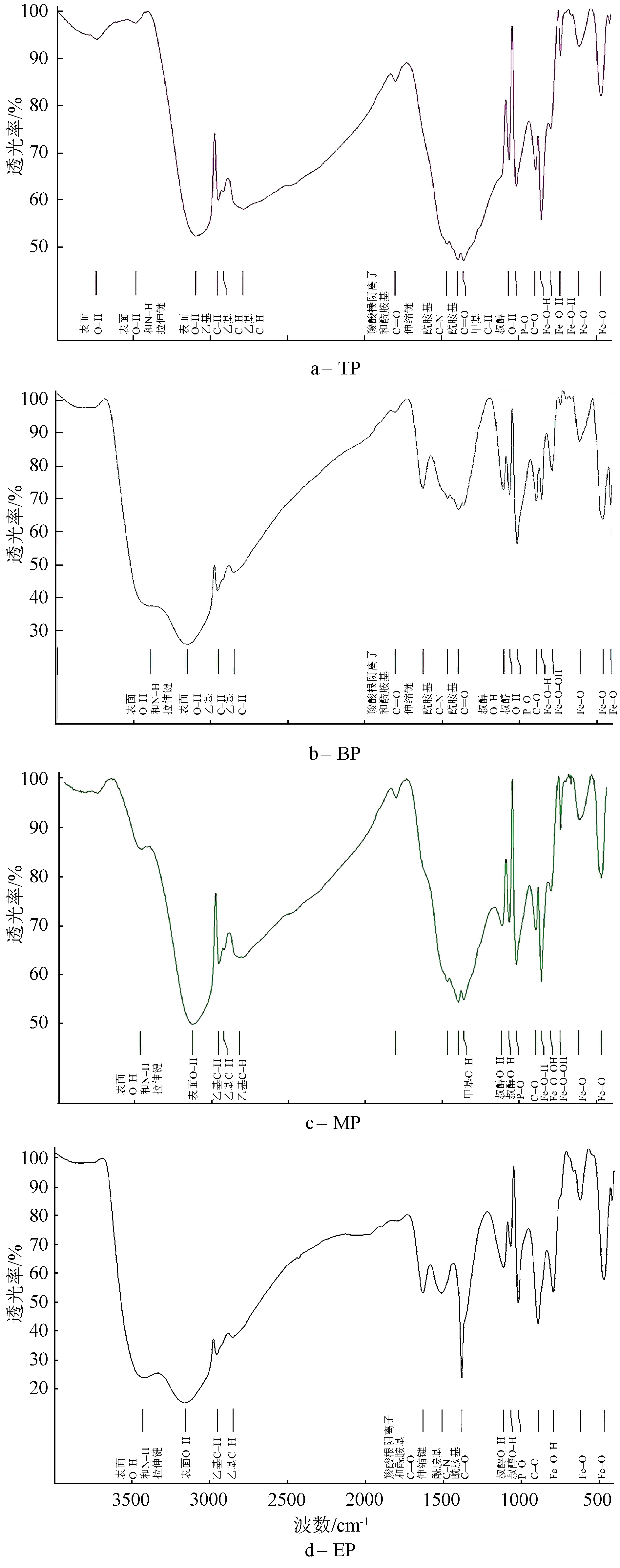
图6 反应器不同位置的固体颗粒物的傅里叶红外光谱分析结果
Figure 6 FTIR analysis of solid particles in different positions of the reactor
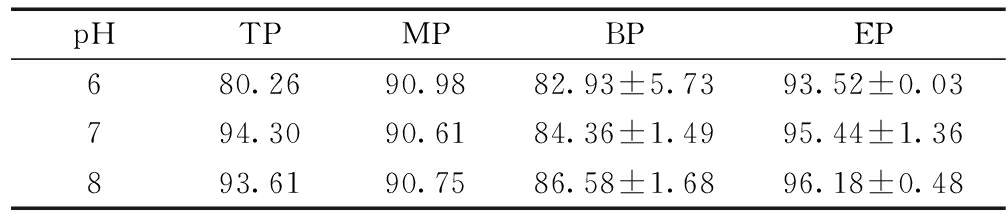
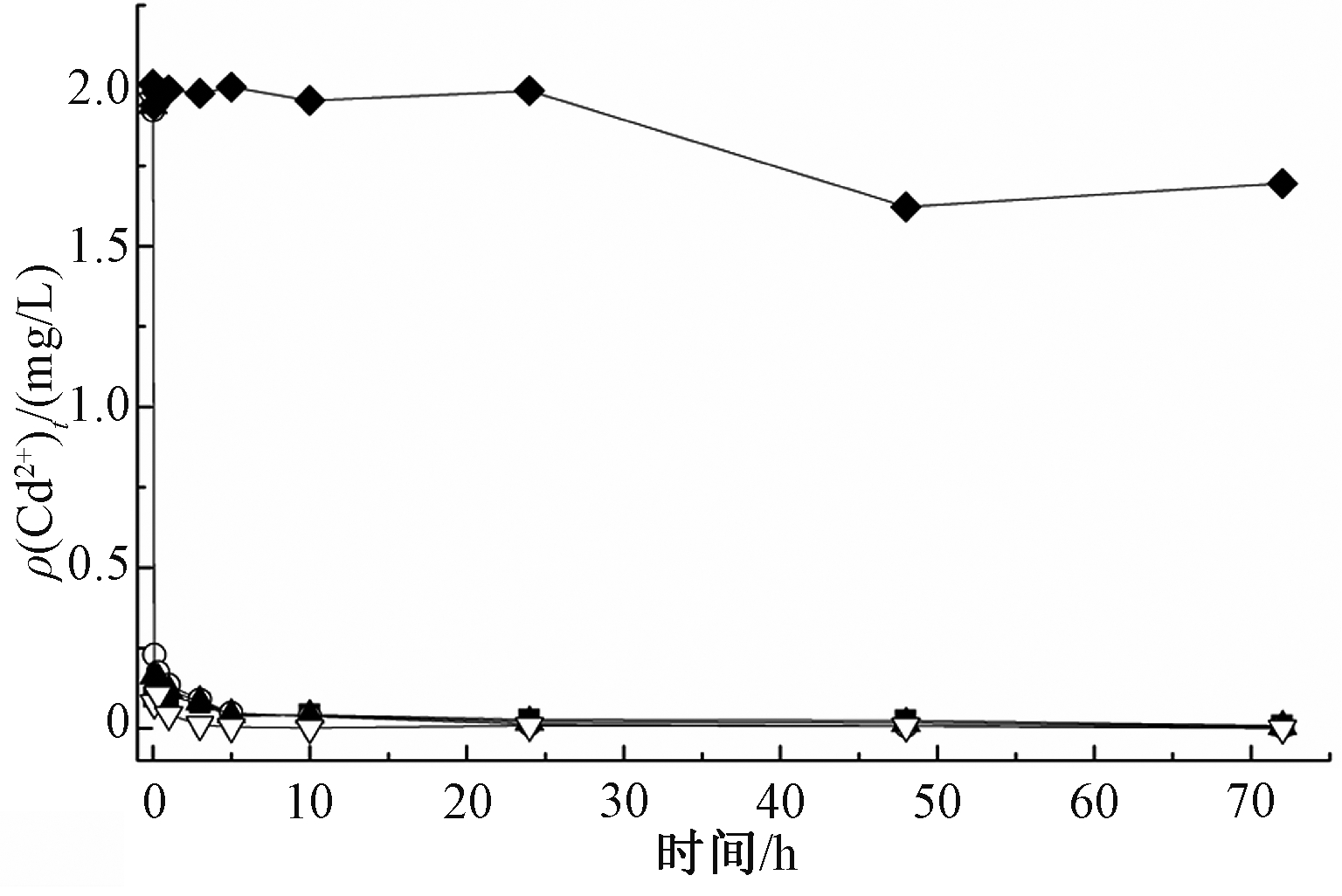
表2为不同pH值条件下固体颗粒对Cd的吸附去除率。可知:在pH为6~8时,不同位置形成的固体颗粒均可将重金属Cd有效地去除,吸附去除率为80%~97%。上部、中部、下部和出水固体颗粒吸附Cd离子的最佳pH分别为7、6、8、8;而在相同pH条件下,反应器内不同位置固体颗粒对重金属Cd的吸附去除率顺序为出水>上部>中部>下部。此外,如图7所示,4种颗粒在各自最佳pH条件下的Cd吸附过程不仅可在短时间内快速达到平衡状态,而且吸附去除率均可达到84%以上,说明反应器生成的固体颗粒具有良好的Cd吸附能力。
如表3所示,4种固体颗粒对Cd吸附动力学曲线拟合准二级动力学方程的相关系数R2均高达0.99,计算吸附容量也与实际吸附量更接近,表明固体颗粒吸附过程主要是化学吸附。其中,出水SS固体颗粒的吸附速率(k2=1.76 min-1)明显高于上部、中部和底部的固体颗粒,而底部固体颗粒的吸附速率(k2=0.16 min-1)最小。
表2 不同pH值条件下固体颗粒对Cd的吸附去除率
Table 2 Adsorption removal rate of solid particles to Cd under different pH values %
pHTPMPBPEP680.2690.9882.93±5.7393.52±0.03794.3090.6184.36±1.4995.44±1.36893.6190.7586.58±1.6896.18±0.48
![]() —TP;
—TP; ![]() —MP;
—MP; ![]() —BP;
—BP; ![]() —EP;
—EP; ![]() —CK。
—CK。
图7 最佳pH条件下Cd2+浓度随时间的变化
Figure 7 Change of Cd2+ concentration with time under the optimal pH condition
表3 反应器固体颗粒吸附Cd2+的吸附动力学拟合结果(T=30 ℃)
Table 3 Adsorption kinetics of Cd2+ adsorbed by solid particles in reactor (T=30 ℃)
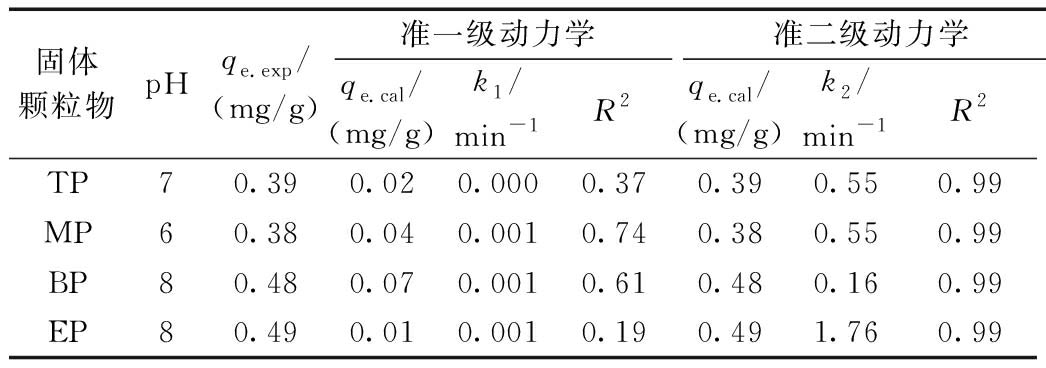
固体颗粒物pHqe.exp/(mg/g)准一级动力学准二级动力学qe.cal/(mg/g)k1/min-1R2qe.cal/(mg/g)k2/min-1R2TP70.390.020.0000.370.390.550.99MP60.380.040.0010.740.380.550.99BP80.480.070.0010.610.480.160.99EP80.490.010.0010.190.491.760.99
如表4所示,4种颗粒在最适pH下对Cd的吸附等温线能够很好地用Freundlich模型拟合,拟合系数R2较高,n值也均接近1,不仅说明固体颗粒对Cd的吸附为有利吸附,还表明该吸附过程属于多分子层吸附[33, 34]。相较之下,Langmuir模型拟合则较差,R2均低于Freundlich拟合系数,可能与本研究中镉离子浓度范围较低有关。
与序批式反应条件相比,基于NAFO过程的连续
表4 固体颗粒物吸附Cd2+的吸附等温线拟合结果(T=30 ℃)
Table 4 Adsorption isotherm fitting results of adsorption of Cd2+ on solid particles (T=30 ℃)
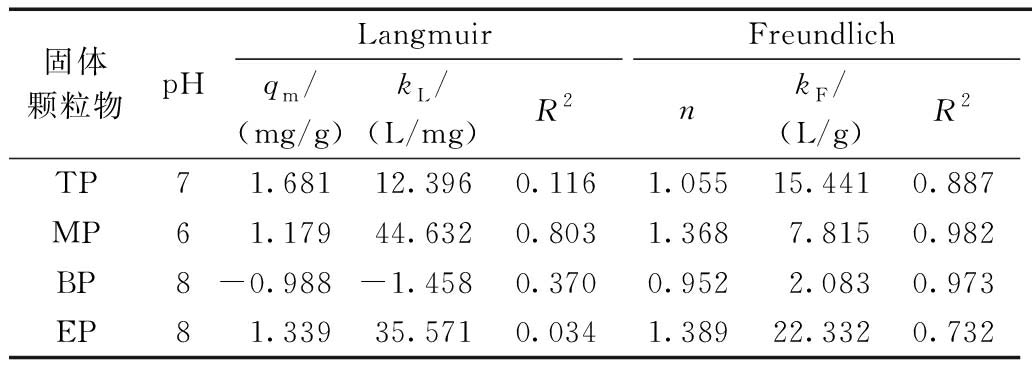
固体颗粒物pHLangmuirFreundlichqm/(mg/g)kL/(L/mg)R2nkF/(L/g)R2TP71.68112.3960.1161.05515.4410.887MP61.17944.6320.8031.3687.8150.982BP8-0.988-1.4580.3700.9522.0830.973EP81.33935.5710.0341.38922.3320.732
流式反应器中的反应条件更加复杂,生成的铁矿物类型也更加丰富。一般情况下,序批式反应是通过一次性投加反应底物和菌种来进行的,由于菌种和培养基比较固定,容易形成特定的铁矿物。例如,Xiu等[24]采用Pseudogulbenkiania sp. strain 2002进行生物铁还原反应主要生成的是纤铁矿,以及Sun等[35]通过在序批式反应瓶中添加混合菌种、硫酸亚铁和硝酸盐的组合底物,获得了以水铁矿和针铁矿为主的铁矿混合物。经过序批式NAFO反应生成的铁矿物,虽然铁氧化物纯度较高,但类型较为单一。相比之下,连续流式反应器产生的铁矿物类型则更加多样,不同位置的铁矿物组成有明显区别。其中,下部的铁矿物以菱铁矿等+2价铁氧化物为主,中部铁矿物的+2/+3价、+3价铁氧化物含量明显增加,上部铁矿物则以磁铁矿(Fe3O4)、纤铁矿(γ-FeOOH)等高价铁氧化物为主。此外有研究发现,水流速度相对较快的出水位置的固体颗粒中容易含有针铁矿等结构较松散的铁矿物,这说明在连续流式反应条件下,水流、硝酸盐氮浓度等不仅会让亚铁在反应器不同位置沉积,还会令其形成氧化程度不同的铁矿物[14]。与序批式NAFO成矿相比,连续流式反应器生成的铁矿物对Cd同样具有良好的吸附能力,这主要是其表面的Fe—O键、Fe—O—H键等所起的作用,此外表面丰富的有机官能团在吸附Cd时也有一定的贡献。
从反应器的运行情况和固体颗粒的吸附特性来看,本研究使用的连续流式反应器不仅可以脱氮,还可以作为一种Cd的高效吸附剂的生产装置。当前针对Cd的吸附剂大多昂贵,而且制造步骤烦琐,特别是化学法制备铁氧化物。而使用天然铁矿物材料进行污水处理,则需考虑对矿物材料进行精炼,以解决天然矿物由于含有硅、镁、锰等杂质而导致的可利用铁氧化物含量分布不均的问题,如吴昆明等[36]和王丹丽等[37]就分别使用高温灼烧和酸化的方法获取针对砷和锌等重金属的铁矿物吸附材料,但同样无法避免处理方法成本高等实际应用问题。相比之下,本研究中所构建的基于NAFO的生物膜反应器除了拥有良好的脱氮功能以外,其产生的铁矿物种类多样、数量多、铁氧化物含量较高、比表面积大,而且制备方法稳定、安全,成本较低,可作为铁氧化物大量制备的新途径之一。其次,除了重金属Cd以外,还有研究表明针铁矿、纤铁矿和磁铁矿等铁(氢)氧化物对双酚基丙烷(bisphenol A,BPA)、五氯硝基苯(pentachloronitrobenzene,PCN)、泰乐菌素(tylosin,TYL))等有机污染物和磷(P)、钼(Mo)、汞(Hg)等无机污染物均具有较好的吸附能力。基于NAFO过程的生物膜反应器不仅是一种高效、经济的脱氮反应器和Cd高效吸附剂的制备装置,还可作为多种污染物吸附剂的生产装置,应用于不同污水的处理[38-43]。
1)基于亚铁氧化反硝化过程的连续流式反应器具有高效的脱氮功能,去除率达到94%以上。
2)反应器不同位置沉积不同类型的含铁颗粒,都含有大量的铁和有机物,下部和中部以菱铁矿为主,上部以针铁矿为主;上部、中部和下部固体颗粒的等电点均接近6,出水固体颗粒的等电点为8.58±0.06;4种固体颗粒的孔径集中在3~4 nm,比表面积较大,而且颗粒表面除了氧化铁、磷酸盐和有机官能团之外,还包含许多有机基团。
3)不同位置形成的固体颗粒对水中Cd2+都有较高的吸附去除率,上部、中部、下部和出水固体颗粒吸附Cd离子的最佳pH分别为7、6、8、8,在各自最佳pH条件下进行吸附实验,4种固体颗粒对Cd的吸附去除率均可达到84%以上,而且吸附过程可与准二级动力学方程和Freundlich模型相拟合,说明固体颗粒对Cd的吸附主要表现为化学作用。
[1] STRAUB K L, BENZ M, SCHINK B, et al. Anaerobic, nitrate-dependent microbial oxidation of ferrous iron[J]. Applied & Environmental Microbiology, 1996, 62(4): 1458-1460.
[2] NIELSEN J L, NIELSEN P H. Microbial nitrate-dependent oxidation of ferrous iron in activated sludge[J]. Environmental Science & Technology, 1998, 32(22): 3556-3561.
[3] 王苏艳, 宋新山, 赵志淼, 等. 亚铁对水平潜流人工湿地反硝化作用的影响[J]. 环境科学学报, 2016, 36(2): 557-563.
[4] 王梦月, 马鲁铭. 催化铁强化低碳废水生物反硝化过程的探讨[J]. 环境科学, 2014, 35(7): 2633-2638.
[5] ZHOU J, WANG H Y, YANG K, et al. Autotrophic denitrification by nitrate-dependent Fe(Ⅱ) oxidation in a continuous up-flow biofilter[J]. Bioprocess & Biosystems Engineering, 2016, 39(2): 277-284.
[6] ZHOU Y, ZHANG Z Q, ZHANG J, et al. Understanding key constituents and feature of the biopolymer in activated sludge responsible for binding heavy metals[J]. Chemical Engineering Journal, 2016, 304: 527-532.
[7] 王茹, 郑平, 张萌, 等. 硝酸盐型厌氧铁氧化菌的种类、分布和特性[J]. 微生物学通报, 2015, 42(12): 2448-2456.
[8] EMERSON D, FLEMING E J, MCBETH J M. Iron-oxidizing bacteria: an environmental and genomic perspective[J]. Annual Review of Microbiology, 2010, 64(1):561-583.
[9] BAZYLINSKI D A, FRANKEL R B. Biologically controlled mineralization in Prokaryotes[J]. Reviews in Mineralogy and Geochemistry, 2003, 54(1): 217-247.
[10] 贾蓉芬,高梅影,彭先芝,等. 微生物矿化[M]. 北京: 科学出版社, 2009.
[11] MIOT J, BENZERARA K, OBST M, et al. Extracellular iron biomineralization by photoautotrophic iron-oxidizing bacteria[J]. Applied & Environmental Microbiology, 2003, 75(17): 5586-5591.
[12] ZHANG M, ZHENG P, ZENG Z, et al. Physicochemical characteristics and microbial community of cultivated sludge for nitrate-dependent anaerobic ferrous-oxidizing (NAFO) process[J]. Separation and Purification Technology, 2016, 169: 296-303.
[13] 沈东升, 李文兵, 姚俊, 等. 亚铁氧化微生物及其在环境污染修复中的作用机制[J]. 浙江大学学报(农业与生命科学版), 2011, 37(1): 112-118.
[14] 杨哲. 依赖硝酸盐型铁氧化菌与天然菱铁矿协同作用脱氮除磷研究[D]. 安徽: 合肥大学, 2016.
[15] SHENG G P, YU H Q, LI X Y. Extracellular polymeric substances (EPS) of microbial aggregates in biological wastewater treatment systems: a review[J]. Biotechnology Advances, 2010, 28(6): 882-894.
[16] 徐轶群, 顾园园, 姚婷, 等. 铁细菌胞外多聚物对铁矿物的调控形成及其环境意义[J]. 岩石矿物学杂志, 2013, 32(6): 782-788.
[17] LI Y F, LONG X X, CHONG Y X, et al. Characterization of the cell-Fe mineral aggregate from nitrogen removal employing ferrous and its adsorption features to heavy metal[J]. Journal of Cleaner Production, 2017, 156: 538-548.
[18] NIDA I, TABASSUM B, ELSAYED F A, et al. Groundwater contamination with cadmium concentrations in some West U. P. Regions, India[J]. Saudi Journal of Biological Sciences, 2018, 25: 1365-1368.
[19] LIU X M, ZHANG L B, MENG J, et al. A multi-medium chain modeling approach to estimate the cumulative effects of cadmium pollution on human health[J]. Environmental Pollution, 2018, 239: 308-317.
[20] 张福凯, 徐龙君, 张丁月. 脱灰煤基活性炭吸附处理含镉废水[J]. 环境工程学报, 2014, 8(2): 559-562.
[21] 莫京倚, 张卫民, 陈家鸿, 等. 2种不同碱度钢渣及其负载HAP吸附镉的比较[J]. 环境工程学报, 2019, 13(8): 1800-1808.
[22] SUN W J, SLERRA-ALVAREZ R, MILNER L, et al. Arsenite and ferrous iron oxidation linked to chemolithotrophic denitrification for the immobilization of arsenic in anoxic environments[J]. Environmental Science & Technology, 2009, 43(17): 6585-6591.
[23] 夏新星, 马腾, 王志强, 等. 载铁活性炭烧结滤芯的制备及其除砷性能[J]. 环境工程学报, 2019, 13(7): 1534-1540.
[24] XIU W, GUO H M, SHEN J X, et al. Stimulation of Fe(Ⅱ) oxidation, biogenic lepidocrocite formation, and arsenic immobilization by Pseudogulbenkiania sp. Strain 2002[J]. Environmental Science & Technology, 2016, 50(12): 6449-6458.
[25] HOHAMANN C, WINKLER E, MORIN G, et al. Anaerobic Fe(Ⅱ)-oxidizing bacteria show as resistance and immobilize as during Fe(Ⅲ) mineral precipitation[J]. Environmental Science & Technology, 2010, 44(1): 94-101.
[26] 任天昊, 杨琦, 李群, 等.针铁矿对废水中Cr(Ⅵ)的吸附[J]. 环境科学与技术, 2015, 38(12Q): 72-77.
[27] 李欣, 谭周亮, 周后珍, 等. 3种微生物吸附剂对低浓度Cd2+的吸附特性研究[J]. 环境科学与技术, 2011, 34(12): 7-13.
[28] 崔慧瑛, 梁成华, 杜立宇, 等. 水铁矿对As(Ⅲ)的吸附特性的研究[J]. 浙江农业学报, 2012, 24(3): 490-493.
[29] SUN J, CHILLRUD S N, MAILLOUX B J, et al. Enhanced and stabilized arsenice retention in microcosms through the microbial oxidation of ferrous iron by nitrate[J]. Chemphere, 2016, 144:1106-1115.
![]() D, JACUKOWICZ-SOBALA I, MAZUR P, et al. Water treatment residuals containing iron and manganese oxides for arsenic removal from water-Characterization of physicochemical properties and adsorption studies[J]. Chemical Engineering Journal, 2016, 294:210-221.
D, JACUKOWICZ-SOBALA I, MAZUR P, et al. Water treatment residuals containing iron and manganese oxides for arsenic removal from water-Characterization of physicochemical properties and adsorption studies[J]. Chemical Engineering Journal, 2016, 294:210-221.
[31] YANG J X, WEI W, PI S S, et al. Competitive adsorption of heavy metals by extracellular polymeric substances extracted from Klebsiella sp. J1[J]. Bioresource Technology, 2015, 196: 533-539.
[32] SARAT C T, MULDLIAR S N, VIDYASHANKAR S, et al. Defatted algal biomass as a non-conventional low-cost adsorbent: surface characterization and methylene blue adsorption characteristics[J]. Bioresource Technology, 2015, 184:395-404.
[33] 何炳林, 黄文强. 离子交换与吸附树脂[M]. 上海: 上海科技教育出版社, 1995.
[34] 赵雅兰, 易筱筠, 雷娟, 等. 基于镉吸附的花生壳酶改性研究[J]. 矿物岩石地球化学通报, 2014, 33(2): 208-213.
[35] SUN J, CHILLRUD S N, MAILLOUX B J, et al. Enhanced and stabilized arsenic retention in microcosms through the microbial oxidation of ferrous iron by nitrate[J]. Chemosphere, 2016, 144:1106-1115.
[36] 吴昆明, 郭华明, 魏朝俊. 改性磁铁矿对水体中砷的吸附特性研究[J]. 岩矿测试, 2017, 36(6): 624-632.
[37] 王丹丽, 董晓丹, 王恩德. 针铁矿对重金属离子的吸附作用[J]. 黄金, 2002, 23(2):44-46.
[38] CLEVELAND V, BINGHAM J, KAN E. Heterogeneous Fenton degradation of bisphenol a by carbon nanotube-supported Fe3O4[J]. Separation & Purification Technology, 2014, 133:388-395.
[39] LI X Y, HUANG Y, LI C, et al. Degradation of pCNB by Fenton like process using α-FeOOH[J]. Chemical Engineering Journal, 2015, 260: 28-36.
[40] 张晶, 郭学涛, 葛建华, 等. 针铁矿-腐殖酸的复合物对泰乐菌素的吸附[J]. 环境工程学报, 2016, 10(3): 1145-1151.
[41] 邵鹏辉, 唐朝春, 简美鹏, 等. 磷在磁铁矿-针铁矿混合相上的吸附[J]. 环境工程学报, 2013, 7(9): 3433-3438.
[42] DAVANT S A, COSTA D, LEF
S A, COSTA D, LEF VRE G. Molybdenum(Ⅵ) adsorption onto lepidocrocite (γ-FeOOH): in situ vibrational spectroscopy and DFT+U theoretical study[J]. The Journal of Physical Chemistry C, 2016, 120(22):11871-11881.
VRE G. Molybdenum(Ⅵ) adsorption onto lepidocrocite (γ-FeOOH): in situ vibrational spectroscopy and DFT+U theoretical study[J]. The Journal of Physical Chemistry C, 2016, 120(22):11871-11881.
[43] 鹿存房, 刘清才, 全学军. 利用污泥脱除燃煤电厂烟气中的汞[J]. 环境工程学报, 2017, 11(10): 5559-5564.