0 引 言
重金属具有难降解、可生物富集、毒性高等特征,可通过多种途径进入动植物体内,严重威胁着人类的生活和身体健康,受到人们的高度关注[1]。这些重金属离子,如铬、铜、钴、镍等往往共存于电镀、矿石开采、金属冶炼、印染、纺织、金属酸洗等行业产生的废水,如不经处理或处理不达标而随意排放,会给水环境和土壤环境带来严重的破坏和污染[2, 3]。过去多是针对单一重金属的吸附进行研究,现今如何经济有效地治理复合重金属污染,成为人们关注的热点[4-6]。原位的固化/稳定化技术是目前土壤修复技术中成本较低、易于操作、适用于大规模污染土壤的修复和治理的技术,能够在不破化土壤结构的前提下,又能达到对复合重金属污染土壤的有效修复,较其他的土壤修复技术在经济和工程应用方面具有巨大的优势[7-10]。
近些年对绿色功能化修复材料的研究普遍较多,其中生物炭来源广泛,多为农林废弃物经加工产生的1种富碳、多孔的固体物质,具有比表面积大、孔隙度高、官能团种类多等优点,并能长期停留在环境介质中,物理化学性质稳定,可以作为土壤改良剂改善土壤结构,提高作物产量[11],还可为土壤微生物提供碳源,多孔结构为微生物提供附着位点,从而提高某些微生物对特定污染物(重金属、有机污染物)的修复能力。Nie等[12]发现,在复合重金属污染的土壤中施加生物炭后,土壤微生物的种类和数量都有所增加。张杏锋等[13]实验证明,采用美洲商陆生物炭对Zn、Pb、Cr、Cu 4种重金属均具有相对较强的吸附能力。而Lu等[14]用酸性浓溴化锂水解的方法制得的生物炭,具有的多孔结构(微孔、介孔、大孔)和丰富的含氧官能团(羟基、羰基、酯基、酮基等),能够显著提高生物炭对重金属的吸附量。生物炭通过物理吸附、阳离子交换、阳离子-Ⅱ作用、氧化还原、静电吸引、沉淀和络合等多种机制,降低了重金属在土壤中的生物利用度和迁移率,减少了作物对各种重金属的富集,同时也实现了对农林废弃物的资源化利用[15]。一方面,生物炭与某些金属离子有较强的亲和力,能选择性地吸附某些+2价的金属阳离子,但是针对复合重金属,如果主要是通过生物炭简单的物理吸附或是弱结合的化学吸附,会因土壤环境变化,导致金属的二次释放,增加了土壤环境的风险[16];另一方面,生物炭有限的官能团数量也是制约其吸附量的重要原因。因此,单一的生物炭材料不能满足复杂体系污染物的治理。
纳米零价铁独特的核壳结构能够有效地对重金属进行吸附、转化和富集,其铁芯良好的供电子能力和表面的铁氢氧化合物具有吸附配位能力,两者相辅相成,使nZVI被用于去除两大类金属离子:含氧阴离子(Cr(Ⅵ)、As(Ⅴ)等)和阳离子(Cu(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)等)[17],但是其易氧化,团聚现象严重,导致利用率降低,限制了其实际应用,因此研究者们对纳米零价铁进行改性,薛嵩等[18]发现,生物炭可作为nZVI的有效载体,不仅保持其还原性能,而且增强了稳定性,极大地改善了nZVI团聚失活的现象。在土壤修复中,孟繁健等[19]制备的复合材料中的生物炭对于土壤中的铬有稳定化作用,极大地降低了生物毒性和利用度;而Mandal等[20]制备的硫化纳米零价铁负载的生物炭复合材料,对土壤中Cr(Ⅵ)和总Cr的固定化效率分别达到100%和91.94%。说明生物炭负载零价铁复合材料是1种有效且高效的固化/稳定化材料,较单一材料更具优势。王维大等[21]发现,黑炭负载零价铁后能够对复合污染土壤中铜和铬的稳定化效果、形态转化等方面优于黑炭,有效降低土壤中铜和铬的迁移性和生物有效性。由此可知,将纳米零价铁负载在比表面积大、官能团丰富、孔隙率高和稳定性好的生物炭上,实现了1+1>2的效果,从而达到对复合重金属污染土壤的快速修复。
本研究以杉木屑为原料,在不同碳化温度下得到的炭前驱体,再通过液相还原,获得以生物炭支撑纳米零价铁的复合材料,并考察了生物炭和零价铁负载生物炭对铜、钴、镍、铬4种共存重金属去除率的影响和作用机制,并证明了该修复材料具有从水溶液和污染土壤中去除重金属污染物的优异能力。
1 实验部分
1.1 材料的制备
1.1.1 生物炭
我国每年产生的农作物废弃物数量庞大,而杉木屑本身就可以作为改良剂,改良土壤的理化性质,其对重金属也有一定的吸附效果,因此本研究选择杉木屑作为生物炭材料的前驱体[22],过100目筛,在1 mol/L的NaOH溶液中处理后,振荡24 h,洗涤过滤至滤液pH呈中性,于80 ℃的烘箱中烘干后待用。将碱处理过的杉木屑分别在100,300,400,500,700 ℃的纯氮气氛围下,以5 ℃/min的升温速度热解制得生物炭,将不同碳化温度下的生物炭加入1 mol/L HCl溶液,振荡10 h,洗涤过滤至滤液pH呈中性,烘干。将材料分别命名为SM100、SM300、SM400、SM500和SM700。
1.1.2 生物炭负载纳米零价铁
将1.5 g FeSO4·7H2O溶于50 mL的脱氧水,加入0.3 g不同碳化温度下制备的生物炭后,在摇床中振荡30 min,再用0.5 mol/L NaOH和HCl调节体系的pH为4~4.5,继续振荡18 h,充分吸附Fe2+。将上述溶液通入N2 30 min后,将0.2 mol/L KBH4溶液以3~5 mL/min的滴速滴加,持续通入N2并搅拌。然后迅速用无水乙醇和脱氧水洗涤2~3遍,冷冻干燥,即得负载零价铁的生物炭材料。将改性后的样品分别命名为ZVI-SM100、ZVI-SM300、ZVI-SM400、ZVI-SM500、ZVI-SM700。
1.2 实验方法
配制4种重金属混合储备液:分别精确称取Cu(NO3)2、Ni(NO3)2、Co(NO3)2、K2Cr2O7分析纯,配制成含Cu(Ⅱ)、Ni(Ⅱ)、Co(Ⅱ)、Cr(Ⅵ) 均为500 mg/L的四元混合重金属储备液,根据实验需要进行稀释。将200 mg不同碳化温度下的原始生物炭(SM100-700)和负载零价铁的生物炭(ZVI-SM100-700)、商用纳米nZVI分别加入100 mL、pH为5.44、浓度为50 mg/L的混合溶液中,在恒温摇床[(30±2) ℃,150 r/min]下反应5,10,20,40,80,120,140,180 min时取样,再用0.22 μm的滤头过滤,置于10 mL的离心管内待测。
重金属污染土壤修复实验:取混合均匀的污染土壤,过100目筛,进行相关化学分析检测。由于土壤中的水溶性离子易被植物摄取利用,同时总Cr(Ⅵ)是土壤污染必须监测的指标,因此选取了水溶态金属离子和总Cr(Ⅵ)2个指标进行研究。检测受重金属污染土壤的原始背景值:水溶态的Cu(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)、TCr、Cr(Ⅵ)分别为0.9,0.6,0.5,500,446 mg/kg,TCr(Ⅵ)为480 mg/kg,背景值的确定取3次平行实验的均值,相对误差不超过3%。评价本研究的吸附材料对于污染土壤的修复效果,通过加入3%的材料(ZVI-SM300&ZVI-SM500),分别在1,3,9,15 d分时间点取样检测,通过对土壤中的水溶态离子和总Cr(Ⅵ)的测定,确定材料对于土壤中重金属的修复效果。
1.3 实验分析检测方法
本研究利用X射线衍射仪(X-ray diffractomer,XRD),扫描范围为10°~80°,扫描速度为10°/min,检测零价铁负载前后和反应后的物质组成和形态特点。利用X射线光电子能谱(X-ray photoelectron spectroscopy,XPS)检测样品表面<10 nm的元素组成、元素含量、化学键、元素的价态以及分子结构等方面的信息,着重了解反应前后复合材料表面的物质组成及重金属的价态变化特征。采用电感耦合等离子体发射光谱仪(inductively coupled plasma atomic emission spectrometry, ICP-OES)测定反应后重金属离子浓度,采用二苯碳酰二肼分光光度法,在波长λ=540 nm的条件下测定溶液中剩余的Cr(Ⅵ)浓度。
1.4 数据分析
本研究中除土壤背景值测定实验重复3次取均值外,其余实验均重复2次取均值。实验数据处理在Excel上完成,使用Origin作图。采用重金属去除率η作为吸附材料性能的评价指标。
![]()
(1)
式中:C0和Ce分别为吸附前后溶液中重金属离子的浓度,mg/L;η为重金属离子的去除率,%。
2 结果与讨论
2.1 Fe0负载生物炭反应前后的表征结果
2.1.1 XRD分析
为明确Fe0负载前后及反应后的物质组成和形态特征,利用XRD表征了5种碳化温度下制得的材料,除100 ℃条件下未形成富碳固体物质外,其余4种温度下均形成了无定形的生物炭材料(图1a)。生物炭在2θ为22°和43°附近出现了2个较宽的类石墨衍射峰,属于无定形石墨炭的特征峰,分别对应(002)与(100)特征晶面[18]。碳化温度在300~700 ℃内,特征晶面对应的衍射峰都较宽,说明随着温度的升高,碳材料的石墨化程度升高,尤其是随着温度的升高,700 ℃时(100)晶面对应的衍射峰强度较其他材料要强。
改性后的5种材料(图1b),均出现了2θ=44.7°的特征峰[23],证明Fe0的存在,对应的衍射峰的强度随着温度的升高而增强,表明生物炭在一定程度上增加了Fe0的结晶度,500 ℃的结晶度最高,但是700 ℃的却降低,与Qian等[24]研究的秸秆生物炭相似,石墨化程度与碳化温度呈正相关,负载Fe0的结晶度随着碳化温度的升高而增强,在700 ℃条件下结晶度有所降低,说明不同碳化温度下的生物炭对Fe0的结晶度有一定的影响。而2θ在35.6°(γ-Fe2O3)和35.45°(Fe3O4)处出现少量铁氧化物,并且随着碳化温度的升高,铁的氧化物对应的衍射峰强度升高,表明合成的Fe0活性强,部分被氧化,所以反应前会有少量铁氧化物的存在。
反应后Fe0峰强度减弱,2θ在35°附近(35.45°、35.5°、35.6°和62.2°)出现了较反应前明显的铁氧化物衍射峰(图1c),其中,2θ在35.5°出现的特征峰与文献中[23]报道的FeCr2O4(或Cr2FeO4)物质一致,表明两者之间存在氧化还原反应,形成了稳定的铁铬氧化物被吸附在材料表面,极大地降低了铬的毒性。谱图中并未出现铜、钴、镍、铁复合物的衍射峰,可能是以无定形的形式吸附于材料表面。反应后活性物质Fe0被消耗,尤其是在700 ℃时,Fe0的峰消失,而铁氧化物含量升高,除ZVI-SM700外,其他材料在反应后Fe0含量虽然降低,但峰未消失,只是结晶度发生变化,可能是在反应过程中金属离子(铜、钴、镍、铬)进入Fe0的晶格中,使Fe0结构发生变化,从而降低了结晶度。
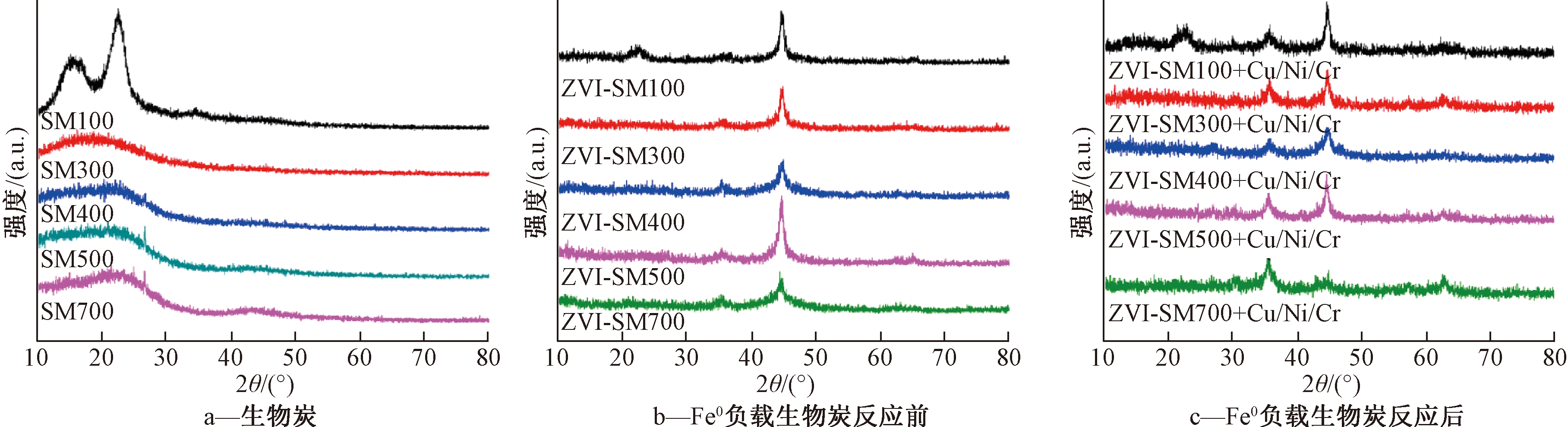
图1 生物炭与反应前后Fe0负载生物炭复合材料的XRD图谱
Figure 1 XRD patterns of biochar precursor and biochar composites loaded with zero-valent iron before and after the reaction
2.1.2 XPS分析
探究不同碳化温度下的复合材料表面元素化学组成及价态的变化,对ZVI-SM300和ZVI-SM500进行XPS分析。如图2所示:生物炭随着热解温度的升高,芳构化程度提高,C—C和C![]() O的占比降低,而C—O的占比升高,主要是由于高温会加剧缩合反应,C
O的占比降低,而C—O的占比升高,主要是由于高温会加剧缩合反应,C![]() O会被不同程度地氧化成C—O,与先前的研究一致[16, 25]。本研究中负载Fe0的生物炭,由于Fe的引入,出现了300 ℃的C
O会被不同程度地氧化成C—O,与先前的研究一致[16, 25]。本研究中负载Fe0的生物炭,由于Fe的引入,出现了300 ℃的C![]() O(6.9%)比500 ℃(8.8%)略低的现象,由于Fe(Ⅱ)的浸渍,会发生C—O—Fe键的结合,使C
O(6.9%)比500 ℃(8.8%)略低的现象,由于Fe(Ⅱ)的浸渍,会发生C—O—Fe键的结合,使C![]() O和C—O的含量降低,在KBH4还原亚铁的过程中,通过电子转移生成Fe0,再结合O1s的分峰拟合,300 ℃的Fe—O(40.5%)明显高于500 ℃(21.9%),说明低温生物炭更利于Fe(Ⅱ)与C—O的螯合,进一步提高了Fe0的负载量。
O和C—O的含量降低,在KBH4还原亚铁的过程中,通过电子转移生成Fe0,再结合O1s的分峰拟合,300 ℃的Fe—O(40.5%)明显高于500 ℃(21.9%),说明低温生物炭更利于Fe(Ⅱ)与C—O的螯合,进一步提高了Fe0的负载量。
在Fe2p的谱图中,300 ℃和500 ℃的2个材料均出现了明显的Fe0峰(707.69 eV),分别占元素Fe总含量的9.5%(300 ℃)、6.7%(500 ℃),证明合成了零价铁负载的生物炭材料。除Fe0外,Fe(Ⅱ)和Fe(Ⅲ)的特征峰表明在制备过程中,不可避免地被氧化。所有样品的Fe2p峰值均出现在724 eV和711 eV附近(图2c、2f),分别对应于Fe2p1/2与Fe2p3/2。在713.79,727.41 eV(300 ℃)与713.52,726.79 eV(500 ℃)处分别观察到Fe(Ⅲ)的特征峰,Fe(Ⅱ) 的特征结合能分别为711.05,724.43 eV(300 ℃),711.10,724.52 eV(500 ℃),本研究中Fe—C的存在与Wu等[26]研究中Fe0硫化后Fe—S的存在不同,因Fe所处化学环境不同,因而结合能存在差异。XPS检测到的Fe0的含量不高,<10%,主要是因为XPS只能探测材料表面<10 nm范围的元素分布情况[27],但是结合XRD分析,整个体相中含有较多的Fe0,一方面,说明Fe0大部分存在于生物炭内部的孔道结构中,或是被生物炭所包裹,因而表面的零价铁含量较低;另一方面,之前的报道中显示Fe0典型的核壳结构,使Fe0被铁的氧化物包裹,这样亦可有效防止Fe0被氧化。
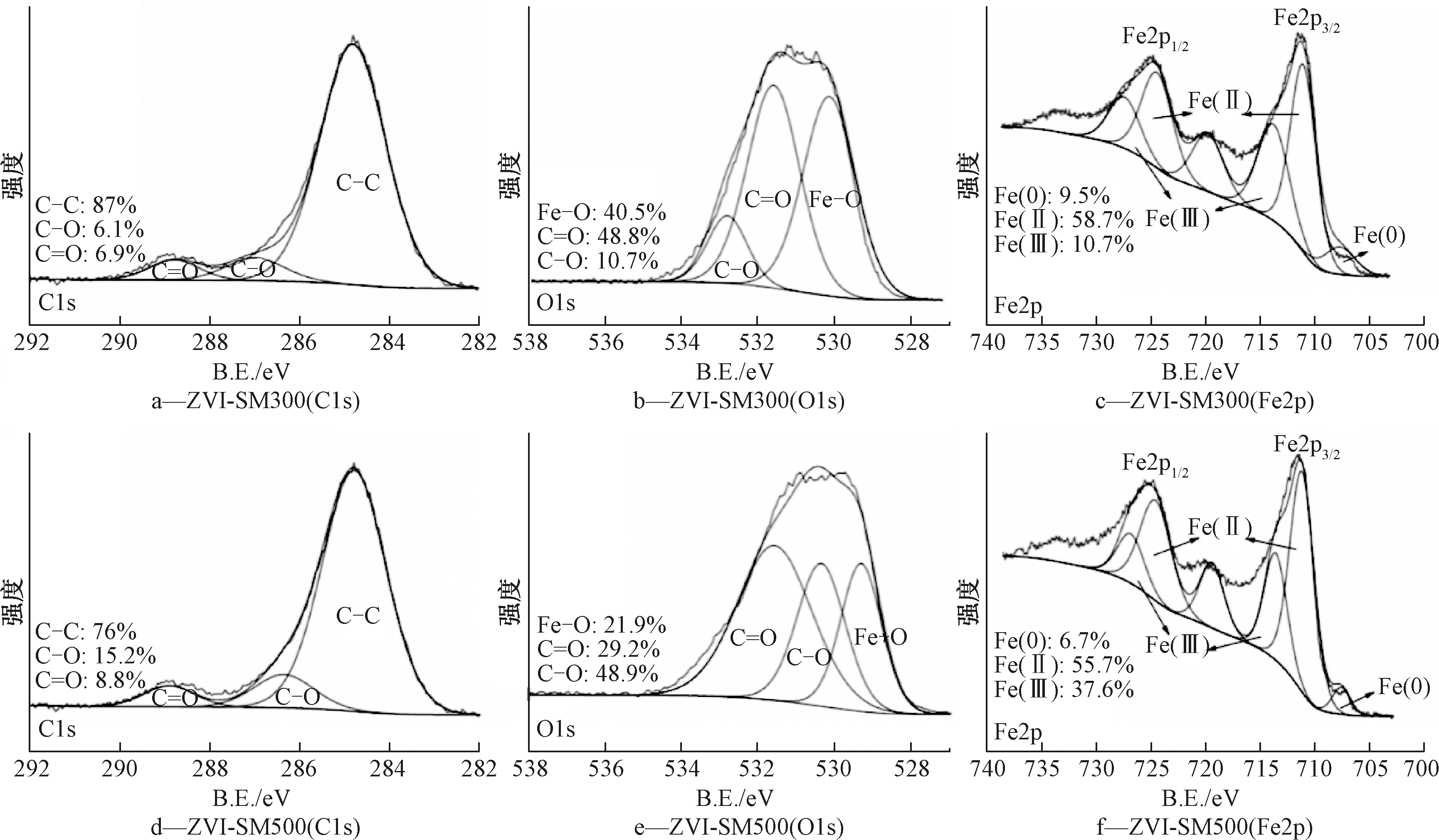
图2 ZVI-SM300和ZVI-SM 500的C1s、O1s、Fe2p结合态的XPS分析
Figure 2 XPS analysis of C1s, O1s, Fe2p binding states of ZVI-SM300 and ZVI-SM500
图3的XPS反映了反应后铁和铬的赋存形态,与反应前的Fe2p相比,Fe0的特征峰消失,Fe(Ⅲ)比例升高,Fe(Ⅱ)比例降低(表1),表明发生了氧化还原反应,Fe(Ⅱ)和 Fe0被氧化,与XRD中铁氧化物相的出现结果一致,结合Fe—O在反应前后的变化特征,从40.5%上升到49.3%(300 ℃),21.9%上升到26%(500 ℃),进一步说明Fe0和Fe(Ⅱ)作为活性物质参与了和重金属离子的反应,而对于生物炭中C—O、C![]() O反应前后的变化:C—O由原来的6.1%(15.2%)上升到10.2%(25.5%),而C
O反应前后的变化:C—O由原来的6.1%(15.2%)上升到10.2%(25.5%),而C![]() O则由6.9%(8.8%)下降到5.1%(6.1%),表明生物炭可以作为电子传递介质,通过表面某些官能团得失电子与Fe0间形成强相互作用,利于活性物质Fe0和Fe(Ⅱ)的产生。
O则由6.9%(8.8%)下降到5.1%(6.1%),表明生物炭可以作为电子传递介质,通过表面某些官能团得失电子与Fe0间形成强相互作用,利于活性物质Fe0和Fe(Ⅱ)的产生。
该复合材料对铬有较强的亲和力,反应后铬在材料表面的价态分布情况,在300 ℃时Cr2p的2个主峰(587.17 eV和577.44 eV)可拟合出4个峰,属于Cr(Ⅲ)、Cr(Ⅵ)对应的特征结合能579.65 eV和588.84 eV,其中,Cr(Ⅲ)和Cr(Ⅵ)分别占元素Cr含量的87.5%和12.5%,而500 ℃时,同300 ℃的现象相似,Cr(Ⅵ)含量降低,说明反应过程中生成了稳定的Cr(Ⅲ),其中Cr(Ⅲ)和Cr(Ⅵ)分别为79.5%和20.5%。铬的去除主要存在2个阶段:第1阶段是以吸附作用为主,比表面积大的生物炭可以在反应初始阶段进行快速吸附,随着反应时间的延长;第2阶段中被吸附在表面的Cr(Ⅵ)与活性物质发生氧化还原反应,Cr(Ⅵ)被Fe0和Fe(Ⅱ)还原成Cr(Ⅲ),再与Fe(Ⅲ)进一步反应生成铁铬的化合物,可以达到对Cr(Ⅵ)的解毒固定作用,反应中Cr(Ⅵ)的减少与含铁活性物质的降低相关,铬在反应过程中可能发生了如下反应:
![]()
(2)
![]()
(3)
xCr3++(1-x)Fe3++3H2O→(CrxFe1-x)(OH)3+3H+
(4)
最终体系中,低毒性的Cr(Ⅲ)稳定存在于材料表面,与Fe的最高氧化态形成铁铬的化合物,降低了铬的毒性,起到了钝化铬和铁的作用。
表1 Fe0负载生物炭(300,500 ℃)C1s、O1s、Fe2p、Cr2p结合态XPS分析
Table 1 XPS analysis of zero valent iron-loaded biochar (300, 500 ℃) in C1s, O1s, Fe2p, Cr2p binding states %
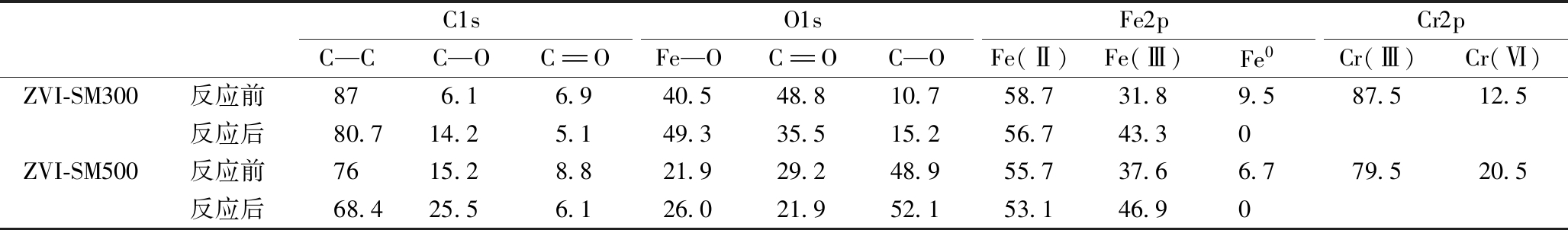
C1sO1sFe2pCr2pC—CC—OCOFe—OCOC—OFe(Ⅱ)Fe(Ⅲ)Fe0Cr(Ⅲ)Cr(Ⅵ)ZVI-SM300反应前876.16.940.548.810.758.731.89.587.512.5反应后80.714.25.149.335.515.256.743.30ZVI-SM500反应前7615.28.821.929.248.955.737.66.779.520.5反应后68.425.56.126.021.952.153.146.90
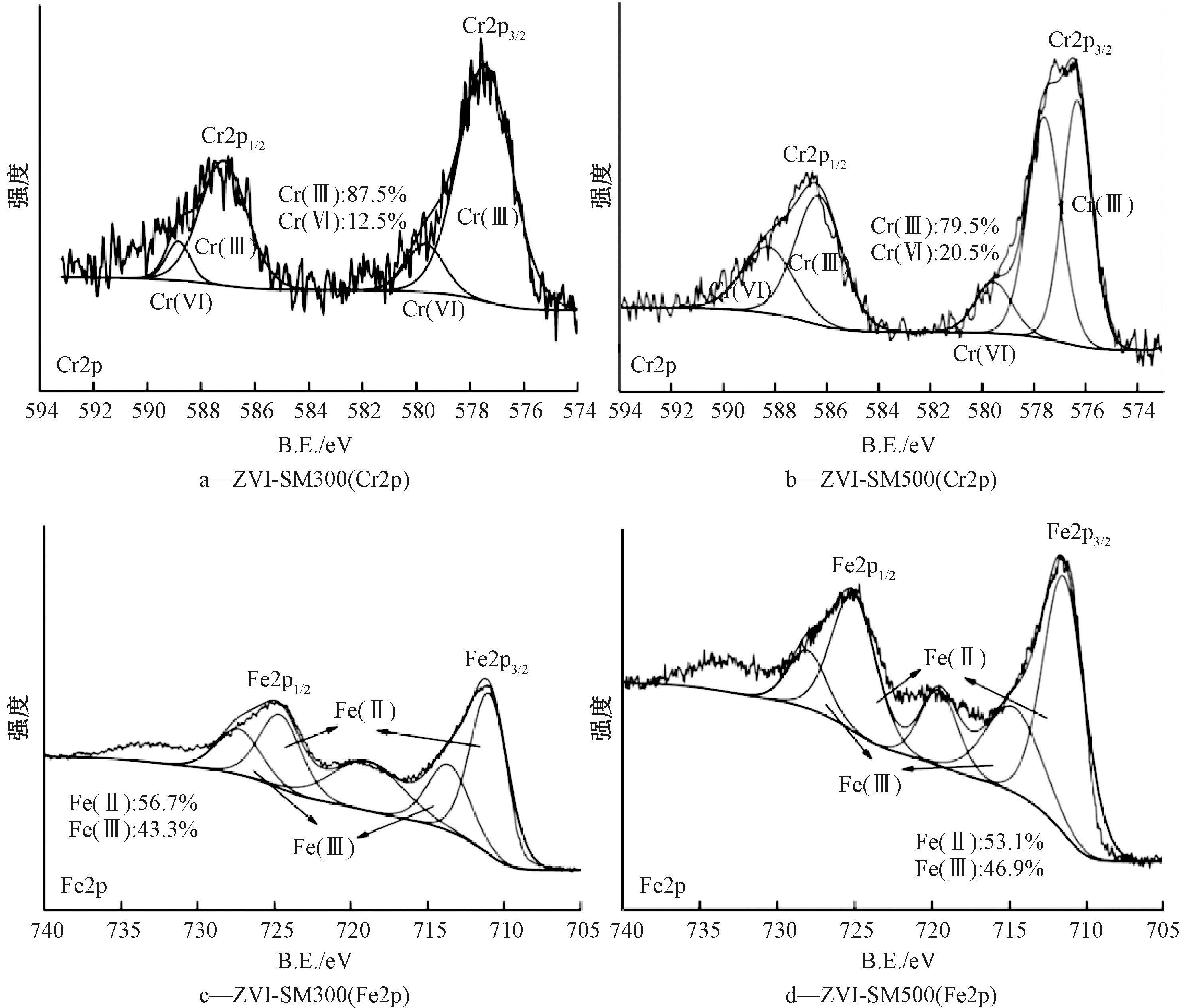
图3 ZVI-SM300和ZVI-SM 500反应后Cr2p和Fe2p结合态的XPS分析
Figure 3 XPS analysis of Cr2p and Fe2p binding states after ZVI-SM300 and ZVI-SM500 reaction
2.2 Fe0负载生物炭对重金属的吸附效果
2.2.1 水溶液体系下吸附时间对吸附效果的影响
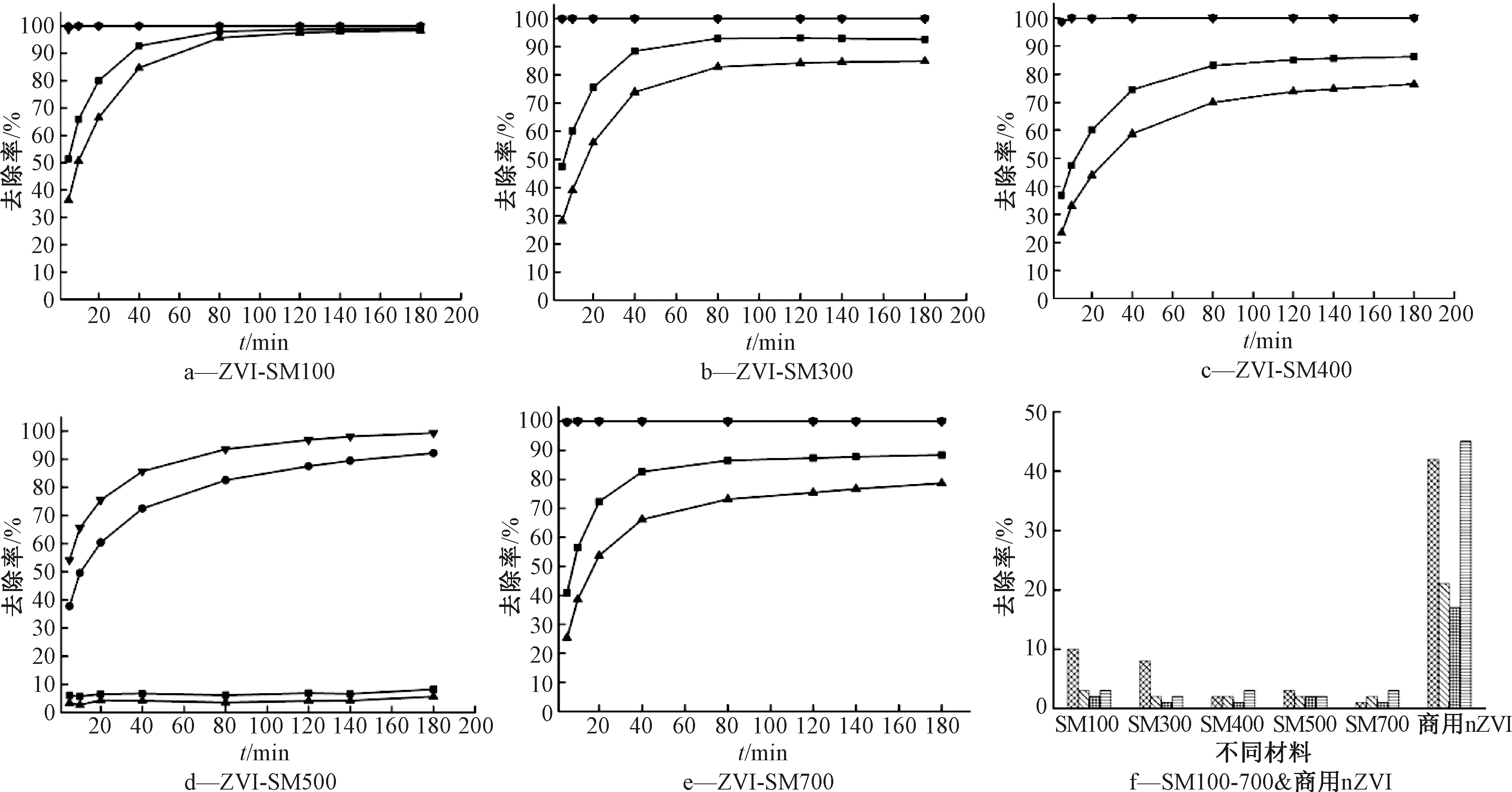
图4显示了ZVI-SM100-700、商用nZVI和SM100-700对铜、钴、镍、铬(Ⅵ)4种重金属的去除效果。负载了Fe0后的5种前驱体,对于复合重金属的去除有明显提高,特别是对于铜和铬的去除效果最为显著,在较短的时间里内能达到吸附平衡,除100 ℃的材料不能定义为生物炭外,对其他4种生物炭复合材料研究,发现碳化温度在300,400,700 ℃时,铜和铬在5 min内能达到吸附平衡,去除率高达100%,采用分光光度法检测不到Cr(Ⅵ)的存在,说明这3种材料对Cr(Ⅵ)有较好的亲和力和优先吸附的特性。温度为500 ℃时,铜和铬前40 min去除效果较好,分别为73%和86%,随着反应的进行,去除率增加变缓,在180 min后,铬和铜的去除率才能达到99%和92%,去除时间长于300,400,700 ℃的材料。结合XRD、ZVI-SM500在5种材料中,Fe0的衍射峰强度最高,相同条件下峰面积最大,说明体相中的Fe0含量最多,而XPS中显示材料表面的Fe0为 6.7%,而吸附是界面反应,材料表面的活性位点较少,反应位点成为该反应的限速步骤,导致其反应和去除速率显著下降,但是随着反应时间的延长,内部的活性位点会逐渐暴露,活性物质会逐渐释放,从而达到对复合重金属完全去除的效果。
针对ZVI-SM300和ZVI-SM500 2种材料,宏观的去除率表现为4种重金属离子的吸附竞争反应,优先吸附Cr(Ⅵ)和Cu(Ⅱ),其中Cr(Ⅵ)竞争吸附能力最强,其次是铜,然后是钴和镍,表现为铬≥铜>钴>镍,这种竞争吸附的现象可能与各种金属离子的标准还原电位有关[28],由于Co(Ⅱ)(-0.282 eV)和Ni(Ⅱ)(-0.236 eV)的电位略高于Fe0(-0.41 eV),而Cu(Ⅱ)(0.342 eV)和Cr(Ⅵ)(1.36 eV)的电位远大于Fe0,使得在反应体系中竞争吸附现象明显,尤其是在活性位点数目有限的条件下,存在氧化还原的化学吸附优于单纯的物理吸附,因此对于Cr(Ⅵ)的去除效果最为显著。同时有研究显示,Fe0还原Cr(Ⅵ)后,被氧化成铁的各种氢氧化物和氧化物(Fe(OH)2、FeOOH、[Fe(OH)]2+、[Fe(OH)3]2-、Fe3O4等)被吸附到生物炭的表面,同时对其他的金属离子存在吸附作用[21]。
![]() —Cu;
—Cu; ![]() —Co;
—Co; ![]() —Ni;
—Ni; ![]() —Cr;
—Cr; ![]() Cu;
Cu; ![]() Co;
Co; ![]() Ni;
Ni; ![]() Cr。
Cr。
图4 不同碳化温度的生物炭、商用nZVI及复合材料对复合重金属去除效果
Figure 4 Removal effect of biochar, nZVI (bar chart) and composite material (line chart) at different carbonation temperatures on the removal of composite heavy metals
负载零价铁的生物炭对于重金属的去除效率提升显著,对比4种生物炭(除SM100),经过180 min的吸附反应后,4种金属的去除率均未超过10%。而较商用nZVI在相同条件下去除率也不超过50%,表明生物炭作为载体,较为有效地分散Fe0,解决了因团聚失活的问题,同时也很好地解决了生物炭吸附量低的问题。
2.2.2 Fe0负载生物炭对污染土壤的修复
将ZVI-SM300和ZVI-SM500用于污染土壤的修复,受污染的土壤自然风干后,用20目的筛网筛土,分成4份,2个平行样,每份取20 g土,分别加入3%的2种材料,再加入10 mL去离子水,充分搅拌后,用封口膜封口防止灰尘进入,静置,分别在1,3,9,15 d取样,对样品土壤进行水溶态离子铜、钴、镍、铬的检测,以及土壤中Cr(Ⅵ)的检测,根据不同时间段测得的土壤中重金属含量的变化特征,确定材料对于污染土壤的修复效果(图5)。随着取样时间的延长,ZVI-SM300和ZVI-SM500作用后的土壤中,总Cr(Ⅵ)和水溶性Cr(Ⅵ)显著降低,在15 d后,土壤中的总Cr(Ⅵ)含量分别为0.52,7.66 mg/kg,去除率分别为99%和98%,而土壤中水溶态的Cr(Ⅵ)由446 mg/kg分别降低到0,3.3 mg/kg,对水溶态Cr(Ⅵ)的去除效果显著,而水溶性的铜、钴、镍含量均为0 mg/kg,被完全去除。对于ZVI-SM500材料前3 d的降解速率较300 ℃的材料慢,但是3 d后,去除率显著优于300 ℃的材料,即3 d就可完全去除水溶性的铜、钴、镍。2种材料对于复合重金属污染修复效果显著,尤其对Cr(Ⅵ)的还原效果很好,同时也能吸附固定其他3种二价金属阳离子(铜、钴、镍)。根据GB 15618—2008《土壤环境质量标准》Cr(Ⅵ)的安全阈值为2 mg/kg, ZVI-SM300在15 d内能使土壤中的总Cr(Ⅵ)和水溶态Cr(Ⅵ)的含量<2 mg/kg,说明该复合材料具有修复铬污染场地的潜力。
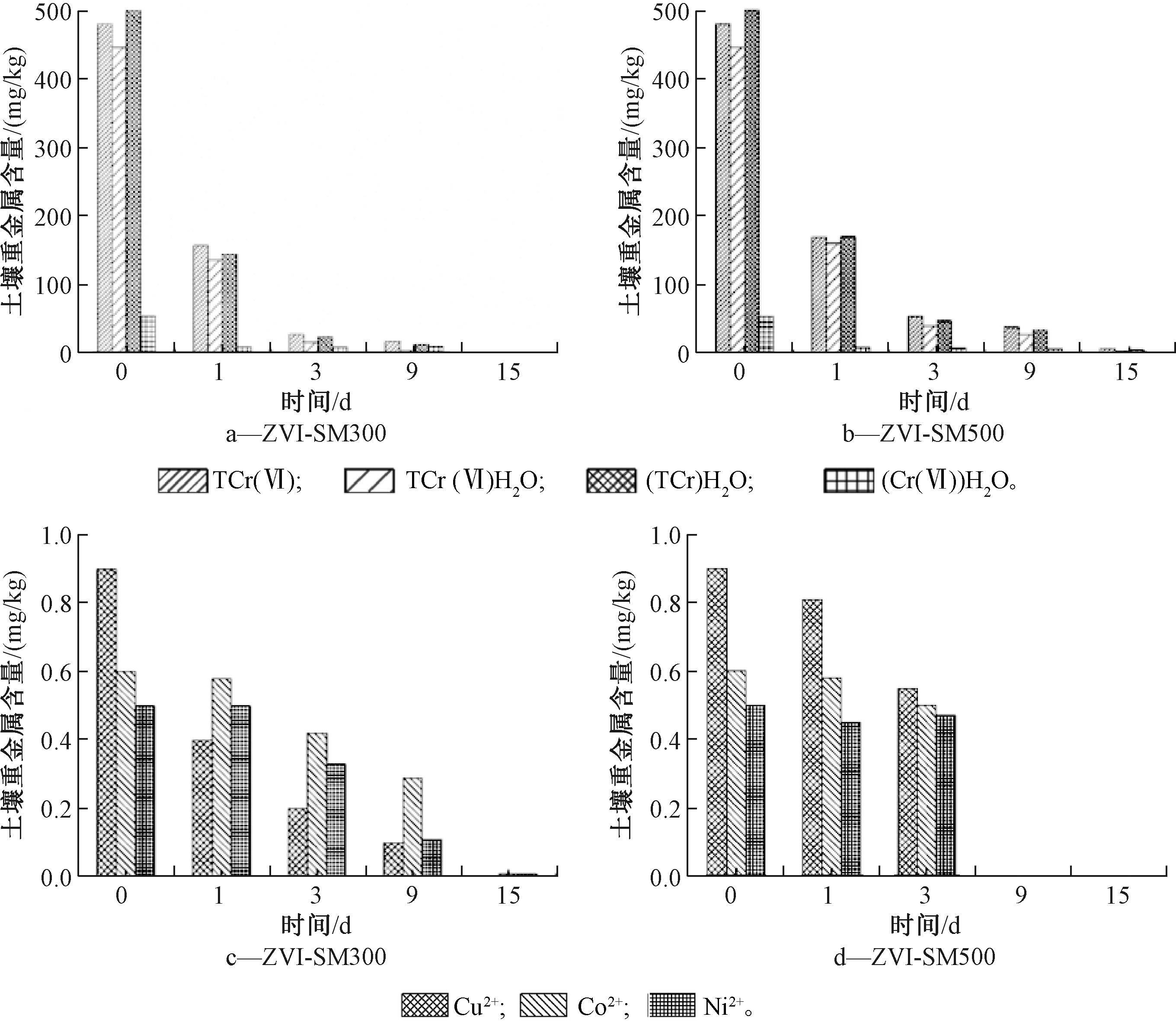
图5 ZVI-SM300& ZVI-SM500对污染土壤的修复效果
Figure 5 Remediation effect of ZVI-SM300 & ZVI-SM500 on contaminated soil
3 结 论
1)本研究合成出1种经济、高效的生物炭负载纳米零价铁的复合材料,并应用于铜、钴、镍、铬污染土壤的修复。其对复合重金属的吸附性能优于单纯的生物炭和商用nZVI,具有良好的去除水溶液中铜、钴、镍、铬重金属污染物的能力,尤其是对铬和铜有较高的亲和力和反应性,其去除率与其标准还原电位相关,表现为铬≥铜>钴>镍,除ZVI-SM500外,其余4种材料均能在5 min内达到100%的去除率,钴和镍在180 min内有超过80%的去除率。
2)分析XPS和XRD结果,吸附-还原后形成了FeCr2O4,极大地降低了铬的毒性,同时也提高了铜、钴、镍的去除率,表明Fe0的引入既提高了生物炭对重金属的吸附量,又解决了Cr(Ⅵ)毒性的问题;同时生物炭可以作为电子传递介质,通过表面官能团电子的得失与Fe0间形成强相互作用,增强了复合材料对多重金属离子的去除效果。
3)土壤修复实验结果表明:ZVI-SM300在15 d内能使土壤中的总Cr(Ⅵ)从480 mg/kg降低到0.52 mg/kg,水溶态Cr(Ⅵ)和总Cr的含量<2 mg/kg,铜、钴、镍也能达到完全去除。鉴于该复合材料对Cr(Ⅵ)的还原有很好的效果,同时也能吸附固定其他二价金属阳离子(铜、钴、镍),并且对环境友好等优点,可进一步优化,制备高效率、低成本的生物炭负载型Fe0,用于重金属污染的水体和土壤修复。
[1] DIACONU M, PAVEL L V, HLIHOR R M, et al. Characterization of heavy metal toxicity in some plants and microorganisms: a preliminary approach for environmental bioremediation[J]. New Biotechnology, 2020, 56: 130-139.
[2] WEN Q X, WANG Q, LI X Q, et al. Enhanced organics and Cu2+ removal in electroplating wastewater by bioaugmentation[J]. Chemosphere, 2018, 212: 476-485.
[3] LI X, WU Y E, ZHANG C, et al. Immobilizing of heavy metals in sediments contaminated by nonferrous metals smelting plant sewage with sulfate reducing bacteria and micro zero valent iron[J]. Chemical Engineering Journal, 2016, 306: 393-400.
[4] CHEN X, CUI J, XU X R, et al. Bacterial cellulose/attapulgite magnetic composites as an efficient adsorbent for heavy metal ions and dye treatment[J]. Carbohydrate Polymers, 2020, 229:115512.
[5] PAP S, J ![]() et al. Evaluation of the adsorption potential of eco-friendly activated carbon prepared from cherry kernels for the removal of Pb2+, Cd2+ and Ni2+ from aqueous wastes[J]. Journal of Environmental Management, 2016, 184: 297-306.
et al. Evaluation of the adsorption potential of eco-friendly activated carbon prepared from cherry kernels for the removal of Pb2+, Cd2+ and Ni2+ from aqueous wastes[J]. Journal of Environmental Management, 2016, 184: 297-306.
[6] FERRI M, CAMPISI S, SCAVINI M, et al. In-depth study of the mechanism of heavy metal trapping on the surface of hydroxyapatite[J]. Applied Surface Science, 2019, 475: 397-409.
[7] 李明, 程寒飞, 安忠义, 等. 化学淋洗与生物质炭稳定化联合修复镉污染土壤[J]. 环境工程学报, 2018, 12(3):904-913.
[8] 张志红, 陈家煜, 郭观林, 等. 稳定剂协同水泥固化/稳定化重金属污染土壤的工程特性[J]. 环境工程学报, 2017, 11(5):3172-3178.
[9] 陈亚奎, 卢滇楠. 重金属污染土壤生物修复技术研究进展与现状[C]∥2019中国环境科学学会科学技术年会论文集(第三卷), 2019: 564-568.
[10] 朱玉斌. 土壤重金属污染现状及修复技术比较[J]. 中国资源综合利用, 2017, 35(5):56-58.
[11] YU H W, ZOU W X, CHEN J J, et al. Biochar amendment improves crop production in problem soils: a review[J]. Journal of Environmental Management, 2019, 232: 8-21.
[12] NIE C, YANG X, NIAZI N K, et al. Impact of sugarcane bagasse-derived biochar on heavy metal availability and microbial activity: a field study[J]. Chemosphere, 2018, 200: 274-282.
[13] 张杏锋, 冯健飞, 姚航, 等. 美洲商陆生物炭对Zn、Pb、Cd和Cu的吸附特性分析[J].环境工程, 2019, 37(8):88-94.
[14] LU X Q, LIU X W, ZHANG W Q, et al. The residue from the acidic concentrated lithium bromide treated crop residue as biochar to remove Cr (Ⅵ)[J]. Bioresource Technology, 2020, 296: 122348.
[15] 熊静, 王蓓丽, 刘渊文, 等. 生物炭去除土壤重金属的研究进展[J].环境工程, 2019, 37(9):182-187.
[16] SHEN Z T, HOU D Y, JIN F, et al. Effect of production temperature on lead removal mechanisms by rice straw biochars[J]. Science of the Total Environment, 2019, 655: 751-758.
[17] LI S L, WANG W, LIANG F P, et al. Heavy metal removal using nanoscale zero-valent iron (nZVI): theory and application[J]. Journal of Hazardous Materials, 2017,322:163-171.
[18] 薛嵩, 钱林波, 晏井春, 等. 生物炭携载纳米零价铁对溶液中 Cr (Ⅵ) 的去除[J]. 环境工程学报, 2016, 10(6): 2895-2901.
[19] 孟繁健, 朱宇恩, 李华, 等. 改性生物炭负载nZVI对土壤Cr(Ⅵ)的修复差异研究[J]. 环境科学学报, 2017, 37(12):4715-4723.
[20] MANDAL S, PU S Y WANG X K, et al. Hierarchical porous structured polysulfide supported nZVI/biochar and efficient immobilization of selenium in the soil[J]. Science of the Total Environment, 2020, 708: 134831.
[21] 王维大, 林薇, 李玉梅, 等. 黑炭负载零价铁对复合污染土壤中铜和铬的稳定化效果及生物有效性影响[J]. 环境工程学报, 2019, 13(4):944-954.
[22] 孟李群, 张云鹏, 苏漳文, 等. 不同炭化温度下杉木生物炭产率及特性比较[J].福建林业科技,2014,41(2):38-41.
[23] LV D, ZHOU J S, CAO Z, et al. Mechanism and influence factors of chromium(Ⅵ) removal by sulfide-modified nanoscale zerovalent iron[J]. Chemosphere, 2019, 224: 306-315.
[24] QIAN L B, SHANG X, ZHANG B, et al. Enhanced removal of Cr(Ⅵ) by silicon rich biochar-supported nanoscale zero-valent iron[J]. Chemosphere, 2019, 215: 739-745.
[25] LI Z, SUN Y Q, YANG Y, et al. Biochar-supported nanoscale zero-valent iron as an efficient catalyst for organic degradation in groundwater[J]. Journal of Hazardpus Materials, 2020, 383: 121240.
[26] WU H H, WEI W X, XU C B, et al. Polyethylene glycol-stabilized nano zero-valent iron supported by biochar for highly efficient removal of Cr(Ⅵ)[J]. Ecotoxicology and Environmental Safety, 2020, 188: 109902.
[27] LI J X, ZHANG X Y, LIU M C, et al. Enhanced reactivity and electron selectivity of sulfidated zerovalent iron toward chromate under aerobic conditions[J]. Environmental Science & Technology, 2018, 52(5): 2988-2997.
[28] LING L, HUANG X Y, LI M R, et al. Mapping the reactions in a single zero-valent iron nanoparticle[J]. Environmental Science & Technology, 2017, 51(24): 14293-14300.