0 引 言
我国的水体重金属污染问题突出,水体重金属污染治理技术已经成为国内外研究的难点和热点[1-2]。生物炭吸附法作为重金属废水处理的一项重要技术,具有高效、节能、可循环利用、投资成本小和运行费用低等特点[3-4]。生物炭是热解生物质后得到的一种高含碳固体,其环境稳定性强、孔隙结构发达,表面富含羧基、酚羟基、羰基等官能团,具有较大的比表面积以及较强的离子交换能力[5-6]。利用生物炭去除水体中重金属的研究报道较多[7-8]。但不同材料、热解温度以及热解时间下得到的生物炭对重金属污染物的去除效果存在较大差异[9-10]。
美洲商陆(Phytolacca Americana L.)为多年生野生杂草,具有生物量高的特点,对土壤Cd、Zn具有很强的富集能力,可以修复重金属污染土壤[11],但是鲜见将其作为生物炭处理重金属废水的研究报道。本文以美洲商陆制备生物炭,探讨其对废水中Zn、Pb、Cd和Cu的吸附特性,并利用扫描电镜(SEM)、能谱(EDS)以及X射线衍射图(XRD)对样品结构进行表征分析,以期为应用美洲商陆生物炭处理重金属废水提供参考。
1 实验部分
1.1 高效重金属吸附材料的制备
将采集好的美洲商陆去除杂质、清洗、烘干、粉碎后置于马弗炉中炭化,炭化条件:炭化温度为450 ℃,炭化时间为5 h。将炭化后的美洲商陆生物炭过100目筛后,置于干燥器中备用。
1.2 吸附影响因素实验
1.2.1 溶液初始浓度
用Zn(NO3)·6H2O、Pb(NO3)2、Cu(NO3)2·3H2O、Cd(NO3)2·6H2O配制50,100,200,400 mg/L的Zn-Pb-Cd-Cu复合重金属溶液,在100 mL离心管中分别加入50 mL上述不同浓度的复合重金属溶液,吸附剂投加质量为0.1 g,充分混匀后加盖密封,置于温度为25 ℃、转速为180 r/min的恒温汽浴振荡器中进行振荡,振荡时间为24 h,待吸附平衡后将样品取出待测。
1.2.2 溶液pH
在一系列100 mL离心管中加入50 mL的浓度为100 mg/L的Zn-Pb-Cd-Cu复合重金属溶液,用0.1 mol/L NaOH溶液以及0.1 mol/L HNO3将溶液初始pH调为1、3、5、7、9、11,吸附剂投加质量为0.1 g,后期处理同1.2.1节。
1.2.3 吸附剂投加量
在100 mL离心管中加入50 mL的浓度为100 mg/L的复合重金属溶液,吸附剂投加质量分别为0.01,0.05,0.1,0.2 g,后期处理同1.2.1节。
1.2.4 吸附时间
在100 mL离心管中加入50 mL的浓度分别为50,100,200 mg/L的复合重金属溶液,吸附剂投加质量为0.1 g,充分混匀后加盖密封,振荡时间分别为10,30,60,120,240,480 min。待吸附平衡后将样品取出待测。
1.3 样品分析
将上述实验的样品在3000 r/min下离心5 min后,将样品取出过0.22 μm的滤膜,置于10 mL离心管中。用电感耦合等离子体质谱仪测定溶液中Zn、Pb、Cd和Cu浓度。
1.4 数据分析
每个实验重复2次,数据用平均值和标准误差表示;用Excel软件制图;用去除率和吸附量来表征吸附剂吸附能力[12],计算公式见式(1)—(2):
![]()
(1)
![]()
(2)
式中:D为吸附剂对重金属离子的去除率,%;Q为吸附剂对重金属离子的吸附量,mg/g;C0为吸附前溶液初始总重金属离子浓度,mg/L;Ce为吸附后溶液中重金属离子的浓度,mg/L;V为溶液体积,mL;W为吸附剂质量,g。
2 结果与讨论
2.1 美洲商陆生物炭对重金属的吸附效果
2.1.1 溶液重金属初始浓度对吸附效果的影响
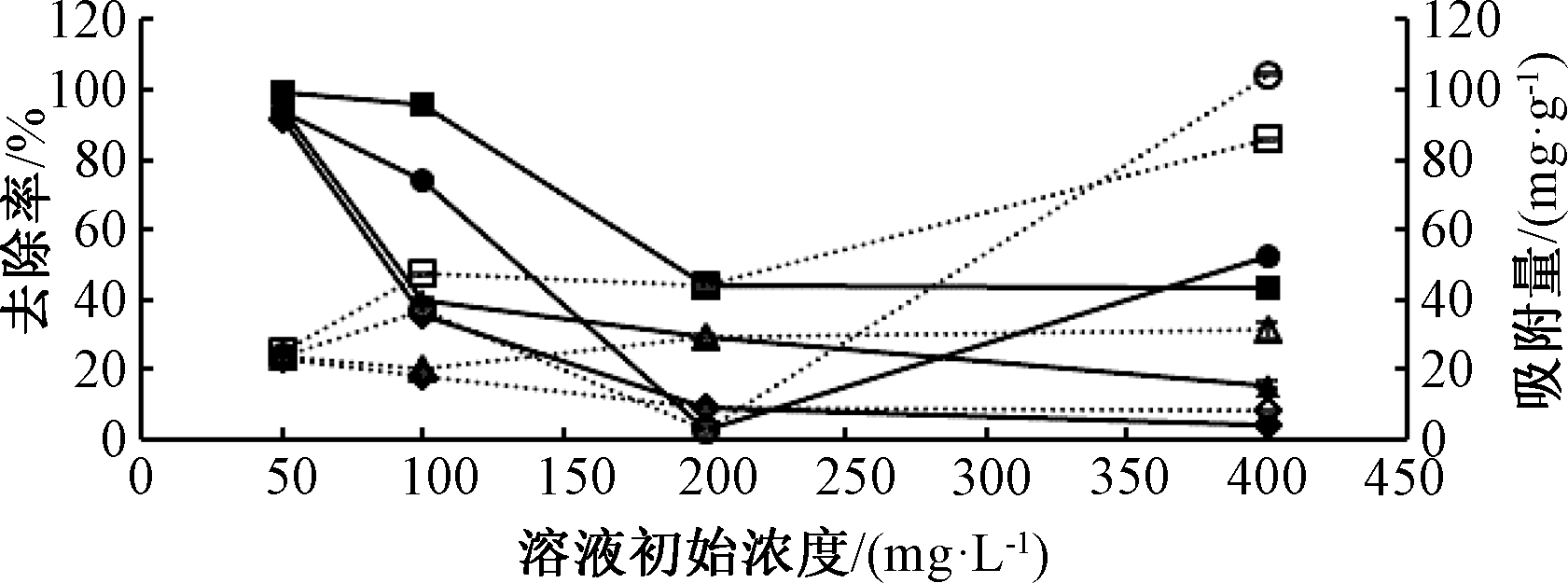
溶液初始浓度对美洲商陆生物炭吸附重金属的影响如图1所示。随着溶液初始浓度的增加,对4种重金属的去除率均呈下降趋势;对Zn、Cd的吸附量随初始浓度增加并未出现明显的变化趋势,但在初始浓度为400 mg/L时,对Pb、Cu的吸附量显著增加。原因或是生物炭的吸附位点有限,而4种重金属之间对吸附位点存在竞争关系,并且Pb、Cu具有更强的竞争力,故在高初始浓度时,生物炭对Pb、Cu具有更大的吸附量。在Zn-Pb-Cd-Cu复合重金属溶液初始浓度为50~200 mg/L时,美洲商陆生物炭对Zn、Pb、Cd和Cu的吸附量很大,分别为22.91,47.77,29.15,39.97 mg/g,显著高于同等条件下蒋新宇等[7] 报道的毛木耳子实体,其吸附材料对Zn、Pb、Cd和Cu的吸附量分别为6.30,23.56,11.78,9.91 mg/g,美洲商陆生物炭对重金属具有较强的吸附效果。
![]() —Zn去除率;
—Zn去除率; ![]() —Pb去除率;
—Pb去除率; ![]() —Cd去除率;
—Cd去除率; ![]() —Cu去除率;
—Cu去除率; ![]() …Zn吸附量;
…Zn吸附量; ![]() …Pb吸附量;
…Pb吸附量; ![]() …Cd吸附量;
…Cd吸附量; ![]() …Cu吸附量。
…Cu吸附量。
图1 溶液初始浓度对美洲商陆生物炭吸附重金属的影响
Fig.1 Effect of the initial concentration on adsorption capacity on
heavy metals by biochar
2.1.2 溶液初始pH对吸附效果的影响
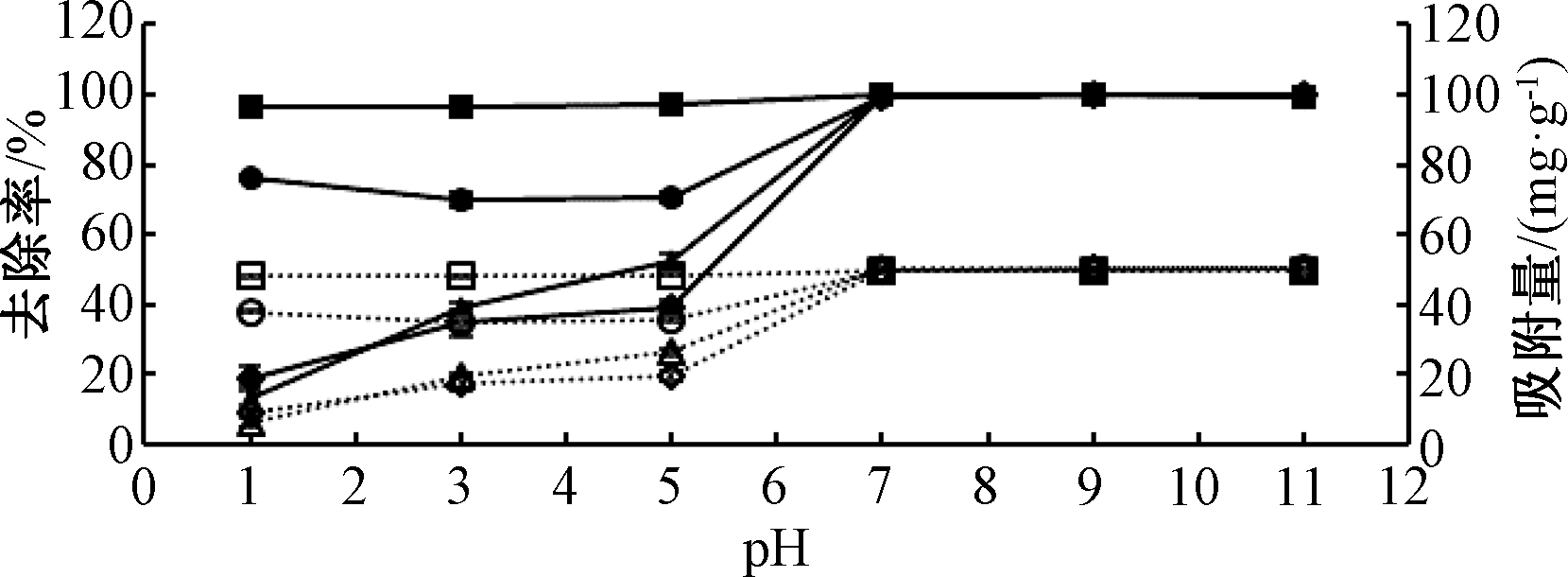
溶液的pH会通过影响重金属离子的赋存形态和生物炭表面电荷分布,影响溶液中重金属离子的吸附[4]。溶液初始pH对美洲商陆生物炭吸附重金属的影响如图2所示。生物炭对Zn、Pb、Cd和Cu的去除率和吸附量均随着溶液初始pH值增加而增加,但pH值对Pb的去除率以及吸附量影响相对较小。当pH值为7~11时,生物炭对重金属的吸附作用达到饱和稳定。研究表明,以上4种重金属离子在溶液中均以阳离子的形态存在,当溶液中的pH较低时,溶液中存在大量的H+,与溶液中的重金属离子存在竞争吸附过程,同时与吸附剂表面所带正电荷产生相斥作用[9],因此,美洲商陆生物炭在pH值较低时吸附量较低。随着溶液pH的升高,溶液中的OH-随之增多,OH-与H+的结合使得H+与重金属离子吸附生物炭表面的活性点位的竞争性降低,生物炭表面的正电荷转化为负电荷,使得其在较高pH条件下对4种重金属离子的吸附量、去除率增加[13-14]。而对Pb的吸附效果受pH值影响较小,表明Pb2+与其他离子相比,其吸附竞争力较强,在酸性条件下仍能得到有效吸附。
![]() —Zn去除率;
—Zn去除率; ![]() —Pb去除率;
—Pb去除率; ![]() —Cd去除率;
—Cd去除率; ![]() —Cu去除率;
—Cu去除率; ![]() …Zn吸附量;
…Zn吸附量; ![]() …Pb吸附量;
…Pb吸附量; ![]() …Cd吸附量;
…Cd吸附量; ![]() …Cu吸附量。
…Cu吸附量。
图2 溶液初始pH对美洲商陆生物炭吸附重金属的影响
Fig.2 Effect of initial pH on adsorption capacity on heavy metals by biochar
2.1.3 吸附剂投加量对吸附效果的影响
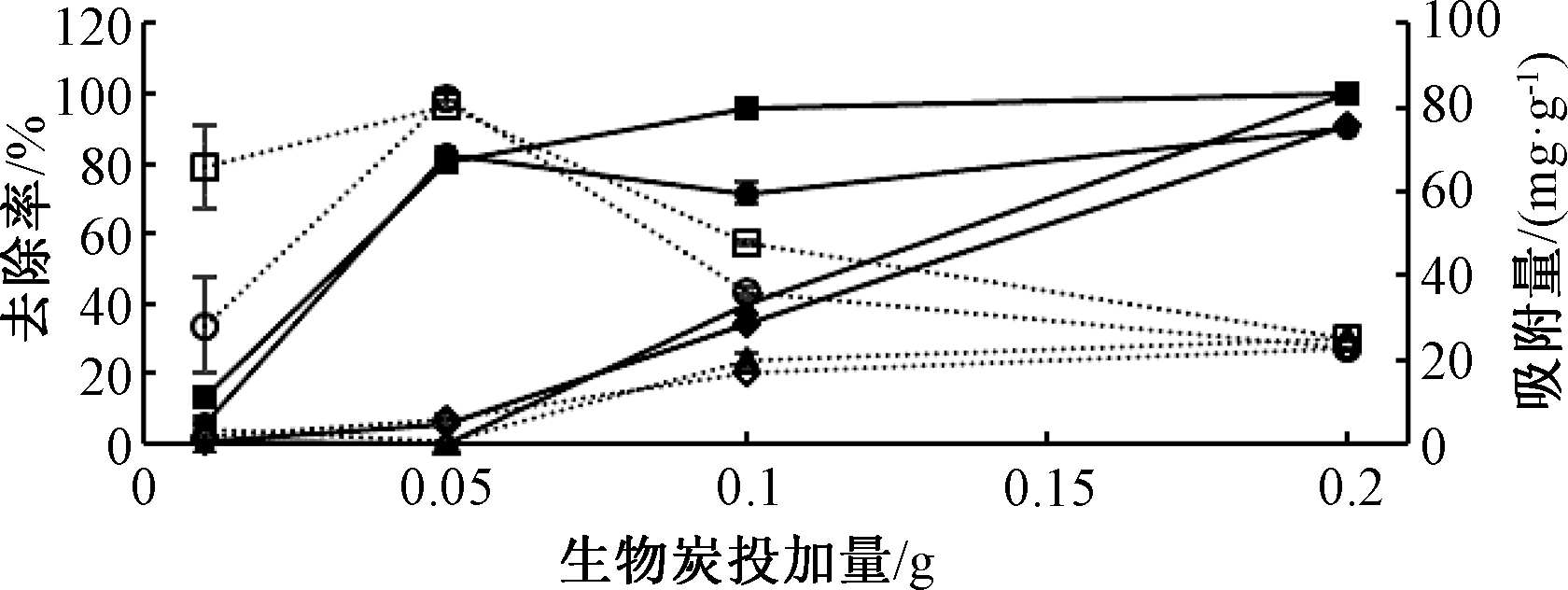
生物炭的使用剂量对其吸附效率具有显著影响,使用最佳剂量能获得最大效益[15]。一般情况下,生物炭可提供的吸附点位随着其投加量的增大而增大[16]。吸附剂投加量对美洲商陆生物炭吸附重金属的影响如图3所示。美洲商陆生物炭在吸附剂投加量为0.01,0.05,0.10 g时对Pb和Cu的吸附量最大,对Zn和Cd的吸附量较少;在吸附剂投加量为0.2 g时,生物炭对Zn和Cd的吸附量逐渐增加,对Pb和Cu的吸附量逐渐下降,总体上对Zn、Pb、Cd和Cu的吸附量相差不大。造成以上结果的原因可能是Zn、Pb、Cd和Cu均为+2价阳离子,会相互竞争吸附位点。当吸附剂投加量为0.01,005,0.10 g时,生物炭的吸附点位较少,优先吸附Pb和Cu,当吸附剂投加量增加,吸附点位增加,使生物炭对Zn和Cd亦能进行充分吸附。最终生物炭对4种金属的吸附达到平衡。
![]() —Zn去除率;
—Zn去除率; ![]() —Pb去除率;
—Pb去除率; ![]() —Cd去除率;
—Cd去除率; ![]() —Cu去除率;
—Cu去除率; ![]() …Zn吸附量;
…Zn吸附量; ![]() …Pb吸附量;
…Pb吸附量; ![]() …Cd吸附量;
…Cd吸附量; ![]() …Cu吸附量。
…Cu吸附量。
图3 吸附剂投加量对美洲商陆生物炭吸附重金属的影响
Fig.3 Effect of initial biochar dosage on its adsorption capacity on heavy
metals by biochar
2.1.4 吸附温度对吸附效果的影响
温度对美洲商陆生物炭吸附重金属的影响如图4所示,不同溶液重金属浓度下其温度效应不同。溶液重金属浓度为50 mg/g时,温度对4种重金属的吸附效果影响不明显。在100 mg/g时,温度对Pb、Cd、Cu的吸附效果影响不明显,但生物炭在45 ℃对Zn的吸附效果最好。在200 mg/g时,生物炭在25 ℃对Zn、Cd的吸附效果最好,在35 ℃对Pb、Cu的吸附效果最好。在400 mg/g时,生物炭在25 ℃对Zn、Pb、Cd和Cu的吸附效果最好。
利用Langmuir模型和Freundlich模型对上述实验数据进行拟合(表1),发现生物炭对溶液中Zn、Pb、Cd的吸附,采用Langmuir等温方程拟合较好,表明生物炭对溶液中Zn、Pb、Cd的吸附属于单分子层吸附[17-18],且Pb在溶液温度逐渐升高的过程中,KL值也不断增大,表明在吸附过程中产生了吸热反应[18]。生物炭对溶液中Cu的吸附采用Freundlich等温方程拟合更好,且4种重金属在3种温度条件下的Freundlich等温吸附方程参数1/n大多位于0.1~0.5,少部分<0.1,表明该条件下生物炭易于吸附Zn、Pb、Cd和Cu[12]。
2.1.5 吸附时间对吸附效果的影响
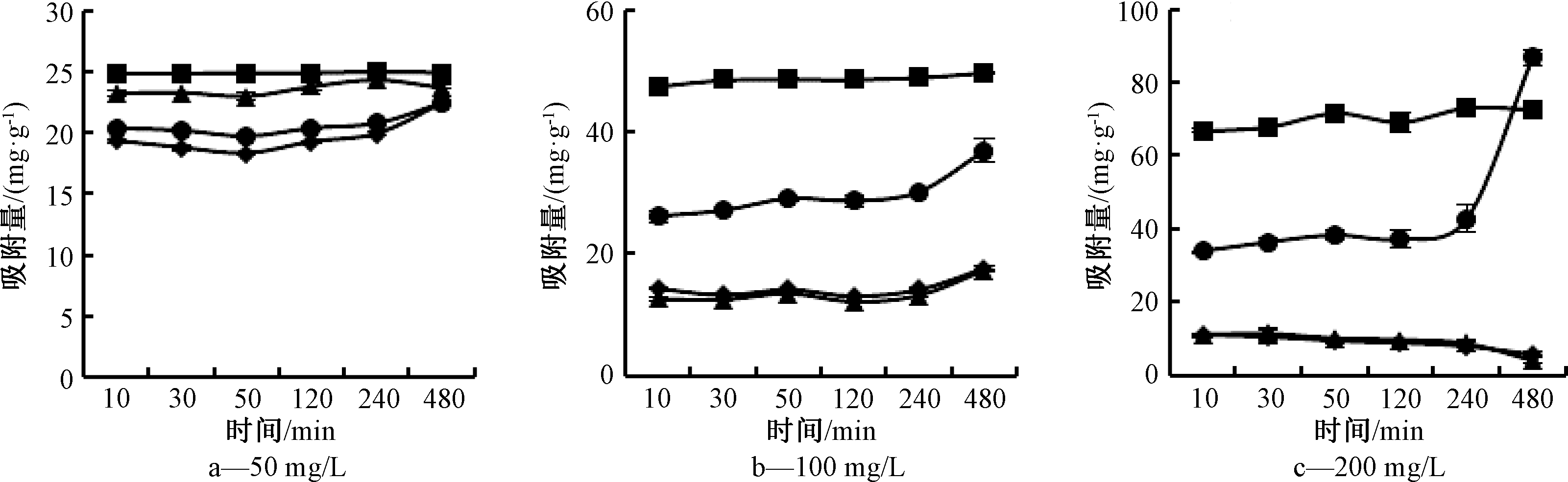
吸附时间对美洲商陆生物炭吸附重金属的影响如图5所示。在3种不同初始浓度的复合溶液中,生物炭对Zn、Pb、Cd的吸附量受吸附时间影响较小,其变化相对平缓,但在初始浓度为100 mg/L与200 mg/L的溶液中,对Cu的吸附量在吸附时间为480 min时,出现急剧增加的情况。这表明美洲商陆生物炭对Zn、Pb、Cd的吸附能在较短时间内达到吸附平衡,但对Cu的吸附反应在初始浓度较大的溶液中,会在吸附时间>240 min时出现较大的变化。
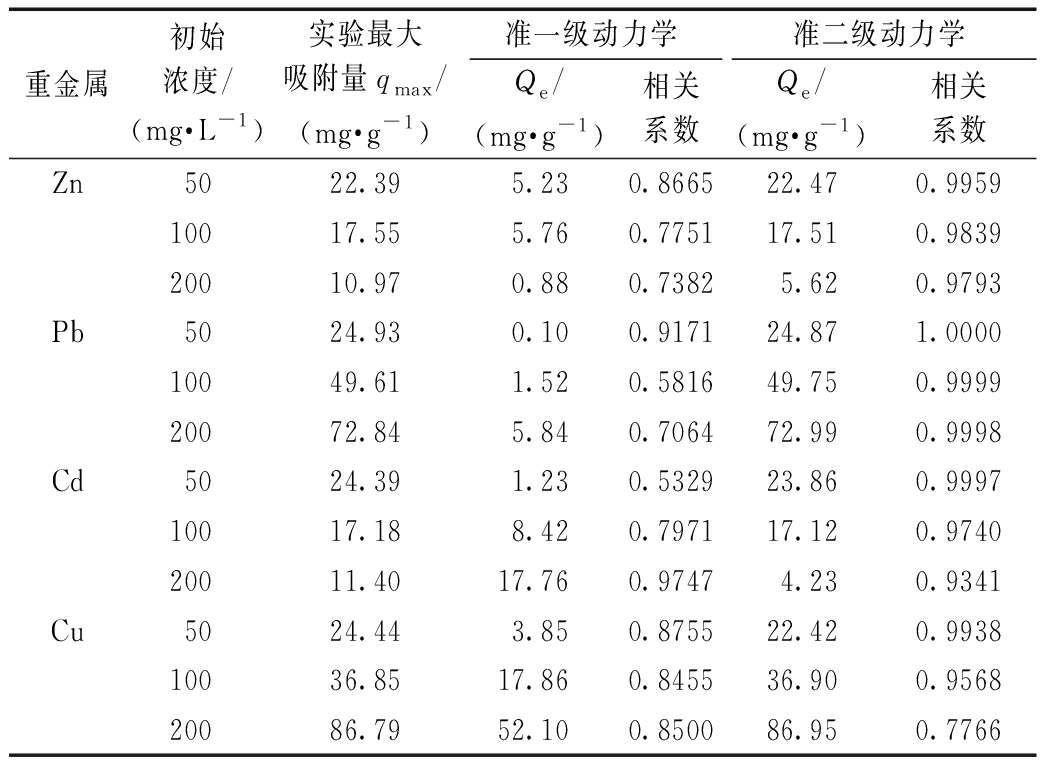
美洲商陆生物炭对Zn、Pb、Cd和Cu离子的吸附动力学模型参数及相关系数如表2所示。美洲商陆生物炭在不同浓度下对Zn、Pb、Cd和Cu的吸附数据拟合准二级动力学模型的相关系数达到0.9~1.0,模型模拟的最大吸附量与实验最大吸附量接近。以上结果表明,准二级动力学模型比准一级动力学模型能够更好地描述生物炭吸附金属离子的过程。生物炭对溶液中的重金属的吸附过程主要受化学反应的控制,且主要包括表面吸附、外部液膜扩散和颗粒内扩散等,这与谢超然利用核桃青皮生物炭吸附Cd的研究结果相似[19]。

![]() —25 ℃;
—25 ℃; ![]() —35 ℃;
—35 ℃; ![]() —45 ℃。
—45 ℃。
图4 温度对美洲商陆生物炭吸附重金属的影响
Fig.4 Effect of temperature on adsorption capacity on heavy
metals by biochar
表1 美洲商陆生物炭吸附Zn、Pb、Cd和Cu的Langmuir和Freundlich等温方程拟合参数
Table 1 Parameters of Langmuir and Freundlich isothermal model for adsorption of Zn, Pb, Cd and Cu by biochar

重金属温度/℃Langmuir等温方程拟合参数Freundlich等温方程拟合参数qm/(mg·g-1)KL/(L·mg-1)R2KF1/nR2Zn2524.570.60480.965715.36360.08820.1213356.250.28620.6806438.3861-0.75630.52614510.690.24400.7444197.5516-0.52940.4507Pb2569.930.00960.42155.75290.38110.34043588.490.01870.87673.11120.57750.76654549.750.67000.89288.36030.34940.3519Cd2531.740.46120.955911.87340.18540.34983514.060.01520.271688.8012-0.35650.12114512.670.01040.165193.2142-0.38120.0969Cu2586.200.00600.25142.61350.5350.449435112.350.01030.80011.70710.69770.878145133.330.00770.74271.34470.75160.9372
![]() —Zn;
—Zn; ![]() —Pb;
—Pb; ![]() —Cd;
—Cd; ![]() —Cu。
—Cu。
图5 吸附时间对美洲商陆生物炭吸附重金属的影响
Fig.5 Effect of reaction time on adsorption capacity on heavy metals by biochar
表2 美洲商陆生物炭对Zn、Pb、Cd和Cu离子的
吸附动力学模型及相关系数
Table 2 Parameters of the pseudo-first-order and
pseudo-second-order kinetic models for the
adsorption of Zn, Pb, Cd and Cu by biochar
重金属初始浓度/(mg·L-1)实验最大吸附量qmax/(mg·g-1)准一级动力学准二级动力学Qe/(mg·g-1)相关系数Qe/(mg·g-1)相关系数Zn5022.395.230.866522.470.995910017.555.760.775117.510.983920010.970.880.73825.620.9793Pb5024.930.100.917124.871.000010049.611.520.581649.750.999920072.845.840.706472.990.9998Cd5024.391.230.532923.860.999710017.188.420.797117.120.974020011.4017.760.97474.230.9341Cu5024.443.850.875522.420.993810036.8517.860.845536.900.956820086.7952.100.850086.950.7766
2.2 美洲商陆生物炭表征结果分析
2.2.1 扫描电镜(SEM)
生物炭前后SEM照片如图6 所示。可知:吸附前生物炭表面空隙分布较多,孔隙较为发达,且孔深较长,这表明生物炭易于吸附重金属离子,吸附后的美洲商陆生物炭表面布满絮状物质,且孔洞与吸附前相比明显减少,使其孔隙率和比表面积显著增加,可以推测出这些絮状物质是吸附后形成的重金属化合物。
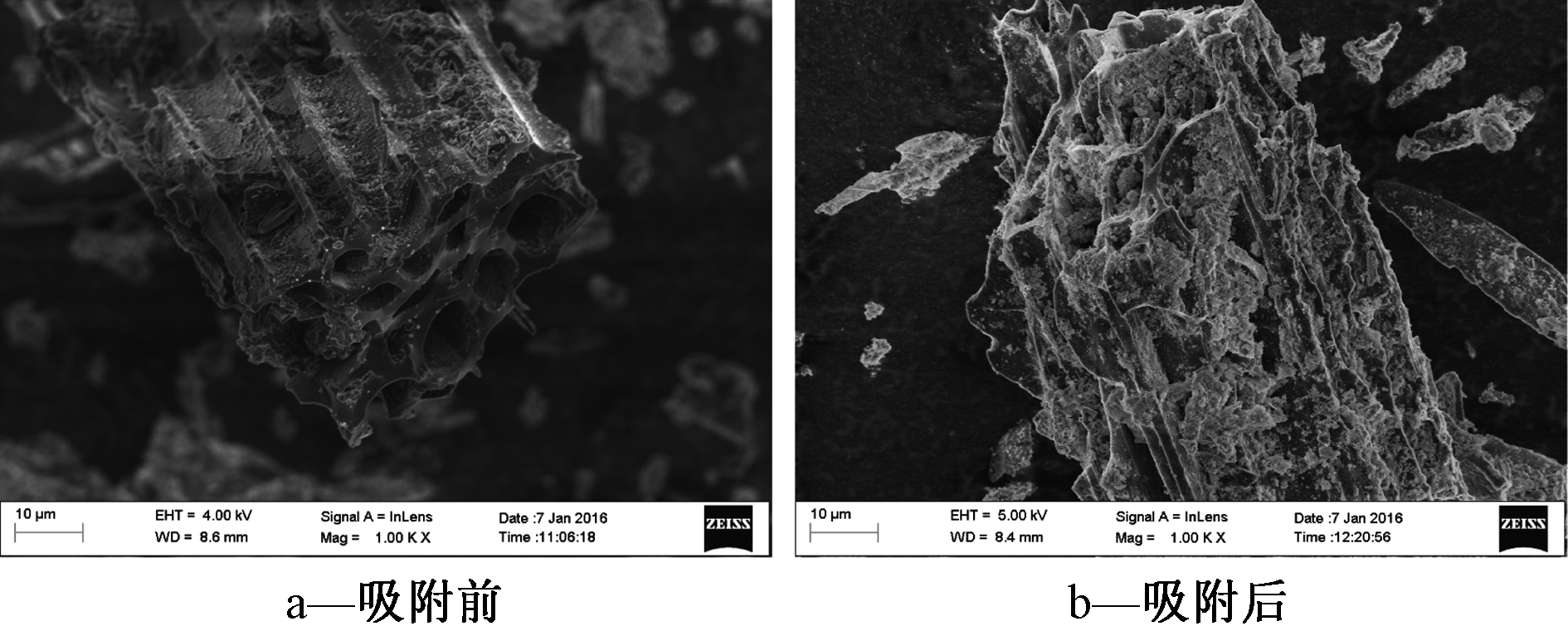
图6 吸附前后美洲商陆生物炭SEM照片
Fig.6 SEM photographs of biochar before and after adsorption
2.2.2 能谱(EDS)分析
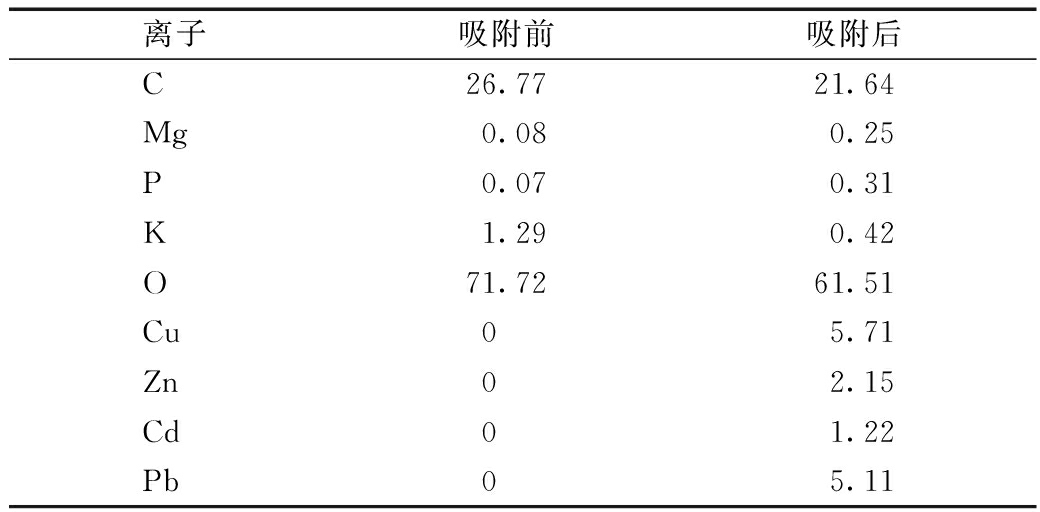
由吸附前后美洲商陆生物炭的能谱图(图7)和美洲商陆生物炭吸附前后表面离子质量分数(表3)可知:吸附前的生物炭组成的主要成分为C、K、O,吸附后的生物炭除了检测到上述元素之外,还检测到Zn、Pb、Cd、Cu。这表明生物炭较好地吸附了上述重金属。
表3 美洲商陆生物炭吸附前后表面离子质量百分比
Table 3 Surface ion mass percentage of biochar
before/after adsorption %
离子吸附前吸附后C26.7721.64Mg0.080.25P0.070.31K1.290.42O71.7261.51Cu05.71Zn02.15Cd01.22Pb05.11
2.2.3 X射线衍射图(XRD)分析
生物炭吸附前后的X射线衍射图(XRD)如图8 所示。吸附前后生物炭的衍射峰的强度发生了明显变化,吸附后生物炭出现新的衍射峰,这可能是由于所吸附的重金属之间,以及重金属与生物炭的基本组成物质之间发生反应,生成了化合物,即生物炭对溶液中重金属的去除机制主要为化学吸附。
3 结 论
1)通过溶液初始浓度不同的吸附实验发现,4种重金属对吸附位点存在竞争关系,并且Pb、Cu具有更强的竞争力。美洲商陆生物炭对重金属具有相对较强的吸附能力。
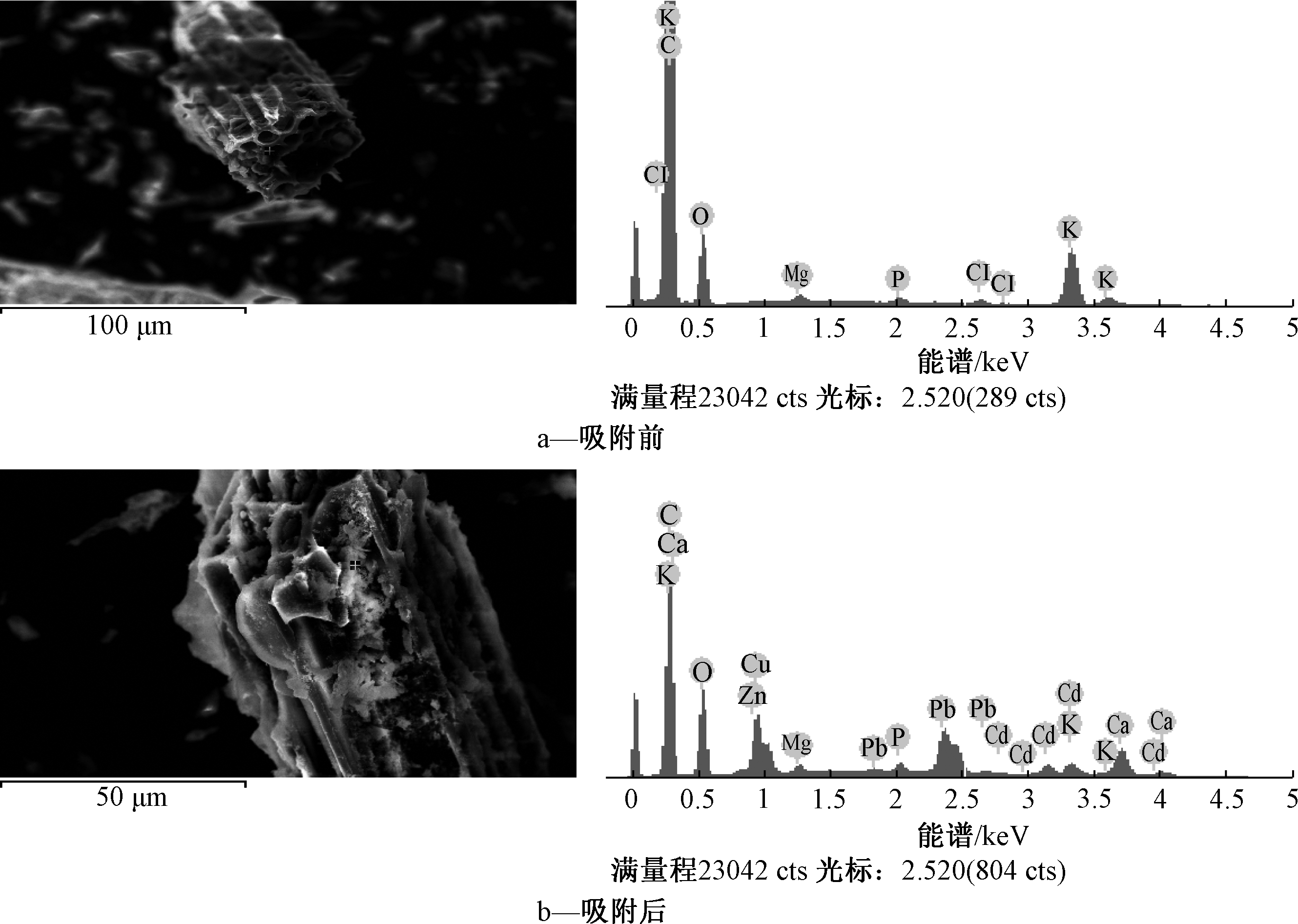
图7 吸附前后美洲商陆生物炭的能谱
Fig.7 The point scanning spectrum of biochar before and after adsorption
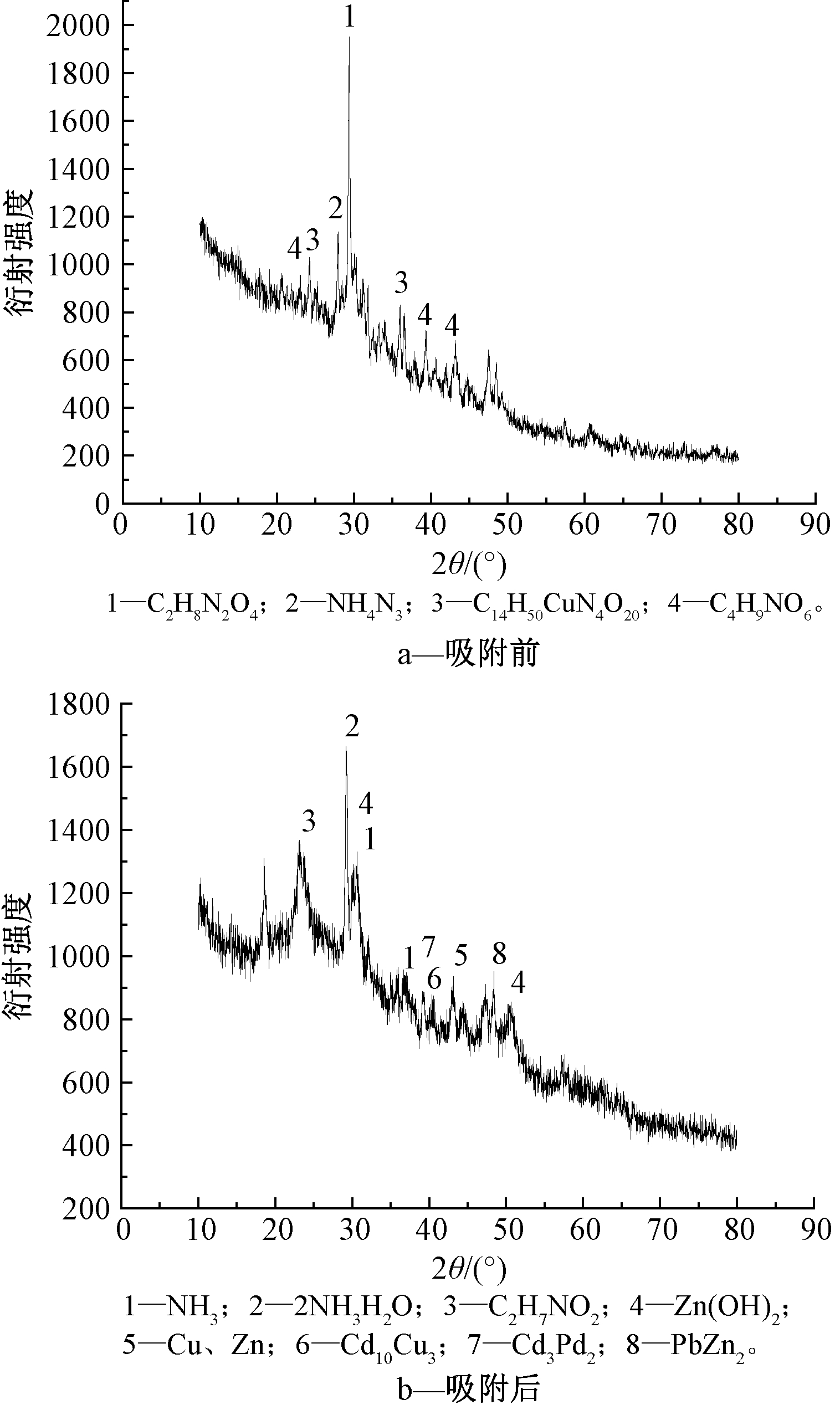
图8 美洲商陆生物炭吸附前后的XRD图
Fig.8 X-ray diffraction spectra of biochar before and after adsorption
2)通过pH不同的吸附实验发现,大量H+的存在会抑制美洲商陆生物炭对重金属的吸附,但Pb2+相对于其他离子具有更强的吸附竞争力,其吸附量受H+影响较小。
3)通过不同生物炭投加量吸附实验发现,生物炭的投加量较少时,生物炭会优先对Pb和Cu进行吸附,但随着投加量的增加对4种重金属均能进行有效吸附,去除率均接近100%。
4)将吸附温度不同的吸附数据用Langmuir模型与Freundlich模型分别进行拟合,发现美洲商陆生物炭对Zn、Pb和Cd的吸附等温线符合Langmuir等温模型;对Cu的吸附等温线符合Freundlich等温模型。将吸附时间不同的吸附数据用准一级与准二级动力学模型拟合,发现该生物炭对Zn、Pb、Cd、Cu的吸附符合准二级动力学模型。表明该生物炭在实验中对重金属的吸附以化学吸附为主。
5)通过扫描电镜(SEM)、能谱(EDS)和XRD分析发现,吸附后的美洲商陆生物炭相对于吸附前的生物炭的结构样貌发生显著改变,且吸附后的生物炭表面生成了较多的重金属化合物。
[1] He B, Yun Z J, Shi J B, et al. Research progress of heavy metal pollution in China: sources, analytical methods, status, and toxicity [J]. Chinese Science Bulletin, 2013, 58:134-140.
[2] 林雪原, 荆延德, 巩晨,等. 生物炭吸附重金属的研究进展[J]. 环境污染与防治, 2014, 36(5): 83-87.
[3] Calero M, Ianez-Rodriguez I, Perez A, et al. Neural fuzzy modelization of copper removal from water by biosorption in fixed-bed columns using olive stone and pinion shell[J]. Bioresource Technology, 2018, 252: 100-109.
[4] Kocaoba S, Arisoy M. Biosorption of cadmium(Ⅱ) and lead(Ⅱ) from aqueous solutions using Pleurotus ostreatus immobilized on bentonite [J]. Separation Science and Technology, 2018, 53, 1703-1710.
[5] Ren G M, Jin Y, Zhang C M, et al. Characteristics of Bacillus sp. PZ-1 and its biosorption to Pb(Ⅱ) [J]. Ecotoxicology and Environmental Safety, 2015, 117:141-148.
[6] 丁文川, 田秀美, 王定勇,等. 腐殖酸对生物炭去除水中Cr(Ⅵ)的影响机制研究[J]. 环境科学, 2012, 33(11): 3847-3853.
[7] 蒋新宇, 黄海伟, 曹理想,等. 毛木耳对Cd2+、Cu2+、Pb2+、Zn2+生物吸附的动力学和吸附平衡研究[J]. 环境科学学报, 2010, 30 (7): 1431-1438.
[8] 周丹丹, 吴文卫, 赵婧,等. 花生壳和松木屑制备的生物炭对Cu2+的吸附研究[J]. 生态环境学报, 2016, 25(3): 523-530.
[9] 王向前, 胡学玉, 陈窈君,等. 生物炭及改性生物炭对水环境中重金属的吸附固定作用[J]. 环境工程, 2016, 34(12): 32-37.
[10] 郑凯琪, 王俊超, 刘姝彤,等. 不同热解温度污泥生物炭对Pb2+、Cd2+的吸附特性[J]. 环境工程学报, 2016, 10(12): 7277-7282.
[11] 王爱国. 美洲商陆(Phytolacca americana L.)对Mn、Cd、Cu的积累特性和EDDS螯合诱导植物修复研究[D]. 南京: 南京农业大学, 2012.
[12] Zhang X F, Zhang X H, Chen Z G. Biosorption of Cr(Ⅵ) from aqueous solution by biochar derived from the leaf of Leersia hexandra Swartz [J]. Environmental Earth Sciences, 2017, 76: 67.
[13] 夏广洁, 宋萍, 邱宇平. 牛粪源和木源生物炭对Pb(Ⅱ)和Cd(Ⅱ)的吸附机理研究[J]. 农业环境科学学报, 2014, 33(3): 569-575.
[14] 李瑞月, 陈德, 李恋卿,等. 不同作物秸秆生物炭对溶液中Pb2+、Cd2+的吸附[J]. 农业环境科学学报, 2015, 34(5): 1001-1008.
[15] 徐楠楠, 林大松, 徐应明,等. 玉米秸秆生物炭对Cd2+的吸附特性及影响因素[J]. 农业环境科学学报, 2014, 33(5): 958-964.
[16] 刘延湘, 黄彪, 张丽. 花生壳生物炭对水中重金属Cr6+、Cu2+的吸附研究[J]. 科学技术与工程, 2017, 17(13): 81-85.
[17] He J S, Chen J P. A comprehensive review on biosorption of heavy metals by algal biomass: materials, performances, chemistry, and modeling simulation tools[J]. Bioresource Technology, 2014,160: 67-78.
[18] Harikishore D, Reddy K, Lee S M. Magnetic biochar composite: facile synthesis, characterization, and application for heavy metal removal[J]. Colloid and Surfaces A: Physicochemical and Engineering Aspects, 2014, 454: 96-103.
[19] 谢超然, 王兆炜, 朱俊民,等. 核桃青皮生物炭对重金属铅、铜的吸附特性研究[J]. 环境科学学报, 2016, 36(4): 1190-1198.